下述实验设计能够达到目的的是
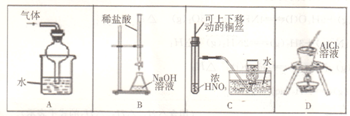

| A.吸收易溶于水的气体 | B.测定NaOH溶液浓度 |
| C.制备并收集少量NO2 | D.制取无水AlCl3 |
更新时间:2016-12-09 11:03:30
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列选项中物质的转化在一定条件下不能实现的是
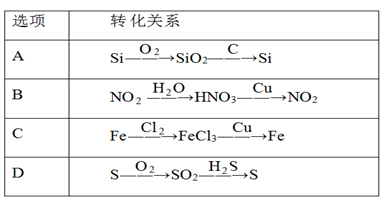

| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据实验内容、实验现象和可能的原因,下列操作和现象能够说明原因不合理的是
| 实验内容 | 实验一 |  | 实验二 |  |
| 实验现象 | 反应后溶液呈绿色,而不是蓝色 | 烧杯中溶液变为无色 | ||
| 可能的原因 | ①溶液中溶解了生成的NO2 ②溶液中c(Cu2+)大 | ③氯水中的H+与OH-反应 ④氯水中的次氯酸漂白了酚酞 | ||
| A.向实验一的绿色溶液中加水,溶液变为蓝色,说明②的原因 |
| B.向实验一的绿色溶液中通入氦气,溶液变为蓝色,说明①的原因 |
| C.向实验二的无色溶液中继续滴加NaOH溶液,溶液又变红,说明③的原因 |
| D.实验一的绿色溶液适当加热,溶液仍为绿色,说明②的原因 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
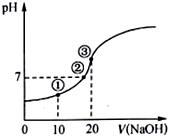
【推荐1】室温下,将0.1 mol/L NaOH溶液滴入20.00 mL 0.1 mol/L HA溶液,溶液pH随加入NaOH溶液体积的变化曲线如图所示。

其中不正确的是

其中不正确的是
| A.①点:由水电离出的c(H+)=1×10-3mol/L |
| B.②点:c(A-)>c(Na+)>c(H+)>c(OH-) |
| C.③点:c(Na+)=c(A-)>c(H+)=c(OH-) |
| D.③点加入NaOH溶液的体积小于20.00mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25°C时,用1.0 mol·L-1 NaOH溶液滴定20.00 mL c1 mol·L-1的盐酸,用0.010 mol·L-1 NaOH溶液滴定20.00 mL c2 mol·L-1的盐酸,滴定曲线如图所示。下列说法不正确的是(已知lg5=0.7)
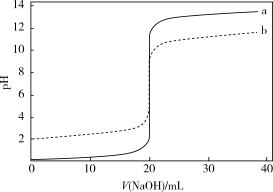

| A.曲线b表示滴定c2 mol·L-1的盐酸 |
| B.水的电离程度在V (NaOH) = 20.00 mL时最大 |
| C.滴定至pH=7时,两份溶液导电能力相同 |
| D.当1.0 mol·L-1 NaOH溶液滴定至19.98 mL时,混合溶液的pH约为3.3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验装置或操作,能达到实验目的的是
| 目的 | 测定中和反应的反应热 | 防止铁片被腐蚀 | 由 制取无水 制取无水 固体 固体 | 用盐酸测定NaOH溶液的浓度 |
| 装置或操作 | 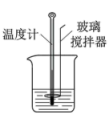 | 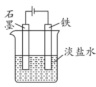 | 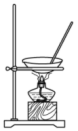 |  |
| 选项 | A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】依据物质结构与反应原理分析,下列演绎或推论不正确的是


A.通常状况下,氯化铝为分子晶体,可推知 也为分子晶体 也为分子晶体 |
| B.常温下,浓硫酸或浓硝酸能使铁钝化,可推知钴、镍也可能会钝化 |
C. 不能使酸性高锰酸钾溶液褪色,可推知 不能使酸性高锰酸钾溶液褪色,可推知 也不能使之褪色 也不能使之褪色 |
D.如图装置可以制备无水氯化镁,也可由 制备 制备 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】高纯的单晶硅是重要的半导体材料,在各种集成电路、芯片和CPU的制作中有不可代替的作用。实验室中模拟SiHCl3制备高纯硅的装置如图所示(夹持装置略去)。
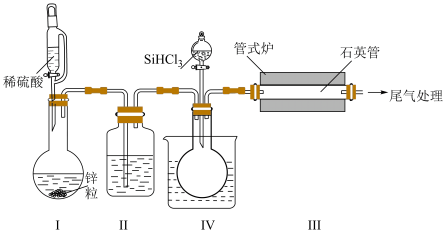
已知:电负性Cl>H>Si,SiHCl3的沸点为31.8℃,熔点为-126.5℃,在空气中易自燃,遇水会剧烈反应。
下列说法正确的是

已知:电负性Cl>H>Si,SiHCl3的沸点为31.8℃,熔点为-126.5℃,在空气中易自燃,遇水会剧烈反应。
下列说法正确的是
| A.实际实验过程中,若装置I中生成1molH2可制得1molSi |
| B.实验开始时,排尽装置中的空气是为了防止SiHCl3水解 |
| C.为提高装置Ⅳ中SiHCl3的利用率,装置Ⅲ应使用冷水浴 |
D.尾气通入NaOH溶液中,SiHCl3发生反应的化学方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列装置或仪器使用不存在错误的是
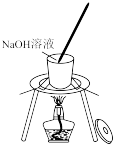 | 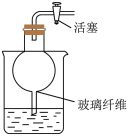 |  |  |
| A.蒸发结晶 | B.制乙炔 | C.制备蒸馏水 | D.保存 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】近日,天津大学钟澄团队制备锌镍电池的负极材料—— ,流程如下,已知:离心分离是借助于离心力,使比重不同的物质进行分离的方法,下列叙述错误的是
,流程如下,已知:离心分离是借助于离心力,使比重不同的物质进行分离的方法,下列叙述错误的是
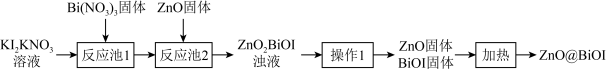
 ,流程如下,已知:离心分离是借助于离心力,使比重不同的物质进行分离的方法,下列叙述错误的是
,流程如下,已知:离心分离是借助于离心力,使比重不同的物质进行分离的方法,下列叙述错误的是
A.“反应池1”中发生的离子反应为 |
| B.“反应池1”和“反应池2”可通过搅拌加快反应 |
| C.“加热”时选择蒸发皿盛放ZnO和BiOI固体 |
| D.“操作1”可以为离心分离,用于分离固体和液体混合物 |
您最近一年使用:0次