按要求作答

更新时间:2016-12-09 11:05:35
|
【知识点】 化学实验基础
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】回答下列有关问题。
(1)某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
某同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:原溶液中所含阳离子是___________________ ,阴离子是_____________________ 。
(2)光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。
①图1中N型半导体为____________ (填“正极”或“负极”)
②该系统工作时,A极的电极反应式为___________________________________________ 。
③若A极产生7.00gN2,则此时B极产生_____________ LH2(标准状况下)。
(1)某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
| 阳离子 | K+ | Cu2+ | Fe3+ | Al3+ | Fe2+ |
| 阴离子 | Cl- | CO32— | NO3— | SO42— | SiO32— |
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:原溶液中所含阳离子是
(2)光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

图1 图2
①图1中N型半导体为
②该系统工作时,A极的电极反应式为
③若A极产生7.00gN2,则此时B极产生
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硼铁混合精矿含有硼镁石[MgBO2(OH)]、磁铁矿(Fe3O4) 、磁黄铁矿(Fe2S)、晶质铀矿(UO2)等,以该矿为原料制备MgSO4•H2O和硼酸(H3BO3)的工艺流程如下:
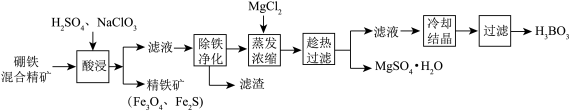
已知:UO22+在pH为4~5的溶液中生成UO2(OH)2沉淀。
回答下列问题:
(1)“酸浸”时,为了提高浸出率可采取的措施有:_______________________ (至少答两个措施),该步骤中NaClO3可将UO2转化为UO22+,则该反应的离子方程式为 ________ 。
(2)“除铁净化”需要加入______ (填化学式)把溶液pH调节至4~5,滤渣的成分是____ 。
(3)“蒸发浓缩”时,加入固体MgCl2的作用是______________________ 。
(4)铁精矿(Fe3O4、Fe2S)经过一系列加工后,可用于制备氢氧化铁固体。已知T℃Ksp[Fe(OH)3]=4.0×10-39、Ksp[Fe(OH)2]=8.0×10-16、Kw=10-a,回答下列问题:
①在T℃,假设Fe3+水解的离子方程式是:Fe3+(aq)+3H2O(l)= Fe(OH)3 (s)+3H+(aq),则该条件下Fe3+水解反应的平衡常数K=___________ (用含a的字母表示)。
②在T℃向饱和的Fe(OH)3、Fe(OH)2混合溶液中,加入少量NaOH固体(忽略溶液体积变化),则溶液中的 会
会________ (填“变大”“变小”或“不变”),请结合相关数据推理说明:____________________________ 。

已知:UO22+在pH为4~5的溶液中生成UO2(OH)2沉淀。
回答下列问题:
(1)“酸浸”时,为了提高浸出率可采取的措施有:
(2)“除铁净化”需要加入
(3)“蒸发浓缩”时,加入固体MgCl2的作用是
(4)铁精矿(Fe3O4、Fe2S)经过一系列加工后,可用于制备氢氧化铁固体。已知T℃Ksp[Fe(OH)3]=4.0×10-39、Ksp[Fe(OH)2]=8.0×10-16、Kw=10-a,回答下列问题:
①在T℃,假设Fe3+水解的离子方程式是:Fe3+(aq)+3H2O(l)= Fe(OH)3 (s)+3H+(aq),则该条件下Fe3+水解反应的平衡常数K=
②在T℃向饱和的Fe(OH)3、Fe(OH)2混合溶液中,加入少量NaOH固体(忽略溶液体积变化),则溶液中的
 会
会
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】高铁酸钾( )是一种暗紫色固体,在低温和碱性环境中稳定存在,在中性或酸性溶液中易发生分解反应,释放出氧气,同时产生一种絮凝剂。高铁酸钾(
)是一种暗紫色固体,在低温和碱性环境中稳定存在,在中性或酸性溶液中易发生分解反应,释放出氧气,同时产生一种絮凝剂。高铁酸钾( )可用于自来水的杀菌消毒和净化,一种由磁铁矿(主要成分为
)可用于自来水的杀菌消毒和净化,一种由磁铁矿(主要成分为 ,还含有少量的
,还含有少量的 、
、 、
、 等)制备高铁酸钾的过程如下图所示:
等)制备高铁酸钾的过程如下图所示:
①高铁酸钾( )难溶于醇等有机溶剂;
)难溶于醇等有机溶剂;
②25℃时部分难溶物的溶度积如下:
回答下列问题:
(1)“酸溶”后得到的滤渣的主要成分为___________ 。
(2)加入 “氧化”过程主要发生的离子方程式为
“氧化”过程主要发生的离子方程式为___________ 。
(3)根据制备过程,步骤“调 ”过程应控制
”过程应控制 范围
范围___________ (已知:氧化后镁、铝离子浓度为0.01 ,当离子浓度小于
,当离子浓度小于 时认为离子沉淀完全)。“氧化、过滤”过程中生成
时认为离子沉淀完全)。“氧化、过滤”过程中生成 ,写出该过程的离子方程式:
,写出该过程的离子方程式:___________ 。
(4) 粗产品含有
粗产品含有 、
、 等杂质,用
等杂质,用___________ 方法进行分离提纯,其提纯步骤为:将一定量的 粗产品溶于冷的3
粗产品溶于冷的3
 溶液中,过滤,将滤液置于冰水浴中,向滤液中加入饱和
溶液中,过滤,将滤液置于冰水浴中,向滤液中加入饱和 溶液,搅拌、静置、过滤,洗涤2~3次,在真空干燥箱中干燥。洗涤过程中可以选用
溶液,搅拌、静置、过滤,洗涤2~3次,在真空干燥箱中干燥。洗涤过程中可以选用___________ (填标号)。
a.蒸馏水 b.乙醇 c.氢氧化钠溶液
(5)产品纯度测定,可采用亚铬酸盐滴定法,滴定时有关反应的离子方程式为:



现称取a g高铁酸钾( )(摩尔质量为M
)(摩尔质量为M )样品溶于过量的碱性亚铬酸盐
)样品溶于过量的碱性亚铬酸盐 溶液中,充分反应后过滤,滤液在250
溶液中,充分反应后过滤,滤液在250 容量瓶中定容,每次取25.00
容量瓶中定容,每次取25.00 于锥形瓶中加入稀硫酸酸化,滴入二苯胺磺酸钠做指示剂,用c
于锥形瓶中加入稀硫酸酸化,滴入二苯胺磺酸钠做指示剂,用c 标准溶液滴定至终点,消耗标准溶液V
标准溶液滴定至终点,消耗标准溶液V ,该产品中高铁酸钾(
,该产品中高铁酸钾( )的纯度为
)的纯度为___________ (用含a、M、c、V的代数式表示)。
 )是一种暗紫色固体,在低温和碱性环境中稳定存在,在中性或酸性溶液中易发生分解反应,释放出氧气,同时产生一种絮凝剂。高铁酸钾(
)是一种暗紫色固体,在低温和碱性环境中稳定存在,在中性或酸性溶液中易发生分解反应,释放出氧气,同时产生一种絮凝剂。高铁酸钾( )可用于自来水的杀菌消毒和净化,一种由磁铁矿(主要成分为
)可用于自来水的杀菌消毒和净化,一种由磁铁矿(主要成分为 ,还含有少量的
,还含有少量的 、
、 、
、 等)制备高铁酸钾的过程如下图所示:
等)制备高铁酸钾的过程如下图所示:
①高铁酸钾(
 )难溶于醇等有机溶剂;
)难溶于醇等有机溶剂;②25℃时部分难溶物的溶度积如下:
 |  |  |  |
 | 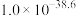 |  |  |
(1)“酸溶”后得到的滤渣的主要成分为
(2)加入
 “氧化”过程主要发生的离子方程式为
“氧化”过程主要发生的离子方程式为(3)根据制备过程,步骤“调
 ”过程应控制
”过程应控制 范围
范围 ,当离子浓度小于
,当离子浓度小于 时认为离子沉淀完全)。“氧化、过滤”过程中生成
时认为离子沉淀完全)。“氧化、过滤”过程中生成 ,写出该过程的离子方程式:
,写出该过程的离子方程式:(4)
 粗产品含有
粗产品含有 、
、 等杂质,用
等杂质,用 粗产品溶于冷的3
粗产品溶于冷的3
 溶液中,过滤,将滤液置于冰水浴中,向滤液中加入饱和
溶液中,过滤,将滤液置于冰水浴中,向滤液中加入饱和 溶液,搅拌、静置、过滤,洗涤2~3次,在真空干燥箱中干燥。洗涤过程中可以选用
溶液,搅拌、静置、过滤,洗涤2~3次,在真空干燥箱中干燥。洗涤过程中可以选用a.蒸馏水 b.乙醇 c.氢氧化钠溶液
(5)产品纯度测定,可采用亚铬酸盐滴定法,滴定时有关反应的离子方程式为:



现称取a g高铁酸钾(
 )(摩尔质量为M
)(摩尔质量为M )样品溶于过量的碱性亚铬酸盐
)样品溶于过量的碱性亚铬酸盐 溶液中,充分反应后过滤,滤液在250
溶液中,充分反应后过滤,滤液在250 容量瓶中定容,每次取25.00
容量瓶中定容,每次取25.00 于锥形瓶中加入稀硫酸酸化,滴入二苯胺磺酸钠做指示剂,用c
于锥形瓶中加入稀硫酸酸化,滴入二苯胺磺酸钠做指示剂,用c 标准溶液滴定至终点,消耗标准溶液V
标准溶液滴定至终点,消耗标准溶液V ,该产品中高铁酸钾(
,该产品中高铁酸钾( )的纯度为
)的纯度为
您最近一年使用:0次



