把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有白色沉淀生成,在所得的悬浊液中逐滴加入1mol•L﹣1HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示.试回答:
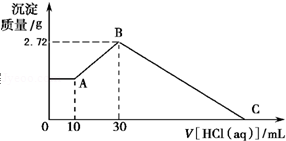
(1)从0开始到A点沉淀物的化学式为____________ ;B点沉淀物的化学式为_________ .
(2)原混合物中的MgCl2的物质的量为_____________ ,AlCl3的物质的量为___________ ,NaOH的物质的量为________ .
(3)HCl溶液在C点的体积数是________ mL.

(1)从0开始到A点沉淀物的化学式为
(2)原混合物中的MgCl2的物质的量为
(3)HCl溶液在C点的体积数是
更新时间:2016-12-09 03:08:34
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】为测定某镁铝合金的成分,取一定质量的样品,平均分为两份,一份加入足量的HCl,完全反应后收集到36.4L(S。T。P)氢气,另一份加入足量NaOH溶液,完全反应后收集到气体33.6L(S.T.P)氢气,试计算合金中铝的百分含量___________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】取50mL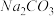 和
和 的混合溶液,加入过量的
的混合溶液,加入过量的 溶液后得到29.02g
溶液后得到29.02g
白色沉淀,用过量的稀硝酸处理后沉淀质量减少到9.32g,并有气体放出,试计算:
(1)原混合溶液中 的物质的量
的物质的量_________
(2)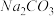 的物质的量浓度
的物质的量浓度__________
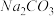 和
和 的混合溶液,加入过量的
的混合溶液,加入过量的 溶液后得到29.02g
溶液后得到29.02g白色沉淀,用过量的稀硝酸处理后沉淀质量减少到9.32g,并有气体放出,试计算:
(1)原混合溶液中
 的物质的量
的物质的量(2)
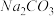 的物质的量浓度
的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】现称取一定质量的镁铝合金样品放入500mL稀硫酸中,固体全部溶解并放出气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。
(1)合金中Al的质量为___ 。
(2)NaOH溶液的物质的量浓度为___ 。
(3)稀硫酸的物质的量浓度为__ 。

(1)合金中Al的质量为
(2)NaOH溶液的物质的量浓度为
(3)稀硫酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
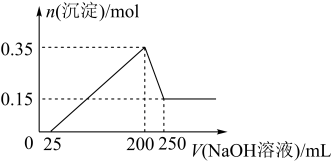
【推荐2】将一定质量的镁和铝的固体混合物投入200mL稀盐酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入的NaOH溶液体积的变化关系如图所示。
回答下列问题:
(1)写出将固体混合物投入稀盐酸中所发生的氧化还原反应的离子方程式:___________ 。
(2)写出加入NaOH溶液的体积为200~240mL时反应的离子方程式:___________ 。
(3)在反应过程中放出的气体在标准状况下的体积为___________ 。
(4)原固体混合物的质量为___________ 。
(5)所用NaOH溶液中NaOH的物质的量浓度为___________ 。

回答下列问题:
(1)写出将固体混合物投入稀盐酸中所发生的氧化还原反应的离子方程式:
(2)写出加入NaOH溶液的体积为200~240mL时反应的离子方程式:
(3)在反应过程中放出的气体在标准状况下的体积为
(4)原固体混合物的质量为
(5)所用NaOH溶液中NaOH的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中后有0.58g白色沉淀生成,在所得的浑浊液中,逐滴加入0.5mol/L盐酸,加入盐酸的体积(V)与生成沉淀的质量(W)关系如右图所示:

(1)混合物中NaOH的质量为_________________
(2)混合物中MgCl2的质量为_________________
(3)混合物中AlCl3的物质的量为_________________
(4)P点表示盐酸的体积是_________________

(1)混合物中NaOH的质量为
(2)混合物中MgCl2的质量为
(3)混合物中AlCl3的物质的量为
(4)P点表示盐酸的体积是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
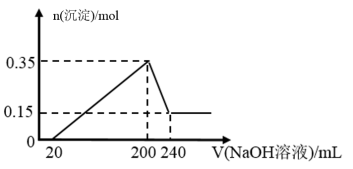
【推荐2】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16 g白色沉淀,在所得的悬浊液中逐滴加入1 mol·L-1 HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示,试回答:
(1)A点→B点反应的离子方程式为_______________________ 。
(2)原混合物中AlCl3的物质的量为______ ,NaOH的物质的量为_____ 。
(3)C点加入的HCl溶液体积为_____________ 。

(1)A点→B点反应的离子方程式为
(2)原混合物中AlCl3的物质的量为
(3)C点加入的HCl溶液体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】向100mL含有Mg2+、Al3+的溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的物质的量与加入NaOH的物质的量的关系如图所示。

(1)由此确定原溶液中一定还大量含有某阳离子,它可能是____
(2则原溶液中铝离子的物质的量浓度为__ 。
(3)下列图像中,横坐标表示加入试剂或通入气体的物质的量,纵坐标表示产生沉淀的质量,用图像的序号回答下列问题:

Ⅰ.表示向AlCl3溶液中逐渐滴加NaOH溶液的是___ ;
Ⅱ.表示向NaAlO2溶液中逐渐滴加稀盐酸的是____ ;
Ⅲ.表示向NaAlO2溶液中通入CO2的是___ ;

(1)由此确定原溶液中一定还大量含有某阳离子,它可能是
(2则原溶液中铝离子的物质的量浓度为
(3)下列图像中,横坐标表示加入试剂或通入气体的物质的量,纵坐标表示产生沉淀的质量,用图像的序号回答下列问题:

Ⅰ.表示向AlCl3溶液中逐渐滴加NaOH溶液的是
Ⅱ.表示向NaAlO2溶液中逐渐滴加稀盐酸的是
Ⅲ.表示向NaAlO2溶液中通入CO2的是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】硫铁矿在高温下被氧气氧化并产生SO2气体:4FeS2+11O2→8SO2+2Fe2O3。设空气中N2占4/5、O2占1/5,试完成下列各题:
(1)55L空气和足量FeS2完全反应后,气体体积(同温同压下,下同)变为_____ L。
(2)若所得混合气体中SO2的体积分数为0.08,则所得混合气体中O2的体积分数______ 。
(1)55L空气和足量FeS2完全反应后,气体体积(同温同压下,下同)变为
(2)若所得混合气体中SO2的体积分数为0.08,则所得混合气体中O2的体积分数
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】某蛋白质含氮16.8%,欲测定该蛋白质水溶液的浓度,作如下实验:①取该蛋白质原溶液0.50 mL,用含催化剂的热硫酸处理,使蛋白质中的有机氮全部转变为NH4+;②然后用强碱溶液处理,并用 10.00 mL,0.020 mol/L的盐酸吸收逸出的全部氨气;③再用0.010 mol/L的氢氧化钠溶液中和未反应的盐酸,消耗氢氧化钠溶液5.00mL。求每毫升该蛋白质溶液含多少毫克蛋白质 ________ ?
您最近一年使用:0次
【推荐3】硝酸是重要的氧化剂,铁、铜是生活中常见的金属.
(1)Fe与Cu混合物与65%的硝酸反应会产生大量NO2,该反应使用的硝酸的物质的量浓度为______ mol/L(已知ρ=1.4g/cm3).
(2)各为0.1mol的Cu与Fe混合物与足量的某浓度的硝酸反应产生4.48L气体(标准状况下),则该反应消耗的硝酸为______ mol.
(3)4.4gFe与Cu混合物与过量的硝酸反应,放出的气体与标准状况下的1.12L的氧气混合后通入水中恰好被完全吸收,则其中铜的质量为______ g.
(4)Fe与Cu混合物共有a mol,其中铜的物质的量分数为X,将该混合物全部投入b mol的硝酸中使其充分反应,假定硝酸的还原产物仅有NO,
①若溶液中金属离子只有Fe2+、Cu2+时,则b的取值范围是______ (用a、x表示).
②若x=0.2时,溶液Fe2+与Fe3+的物质的量相等时,在标准状况下产生NO 6.72L,求a、b的值.(写出简要的计算过程)___________
(1)Fe与Cu混合物与65%的硝酸反应会产生大量NO2,该反应使用的硝酸的物质的量浓度为
(2)各为0.1mol的Cu与Fe混合物与足量的某浓度的硝酸反应产生4.48L气体(标准状况下),则该反应消耗的硝酸为
(3)4.4gFe与Cu混合物与过量的硝酸反应,放出的气体与标准状况下的1.12L的氧气混合后通入水中恰好被完全吸收,则其中铜的质量为
(4)Fe与Cu混合物共有a mol,其中铜的物质的量分数为X,将该混合物全部投入b mol的硝酸中使其充分反应,假定硝酸的还原产物仅有NO,
①若溶液中金属离子只有Fe2+、Cu2+时,则b的取值范围是
②若x=0.2时,溶液Fe2+与Fe3+的物质的量相等时,在标准状况下产生NO 6.72L,求a、b的值.(写出简要的计算过程)
您最近一年使用:0次



