将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。
(1)NO的体积为_______ ;
(2)NO2的体积为______ 。
(1)NO的体积为
(2)NO2的体积为
15-16高一下·宁夏中卫·阶段练习 查看更多[4]
2015-2016学年宁夏中卫一中高一下第一次月考化学试卷2015-2016学年内蒙古巴彦淖尔一中高一上期末化学试卷1(已下线)【走进新高考】(人教版必修一)4.4.2氨、硝酸、硫酸——硝酸 同步练习02甘肃省天水市第一中学2020-2021学年高一下学期第一阶段考试化学(文)试题
更新时间:2016-12-09 14:34:39
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】硫酸和盐酸组成的混合液100mL,向其中加入氢氧化钡粉末4.275g,充分反应后,经过滤、洗涤、干燥,得到沉淀2.33g,同时测得滤液中OH-的浓度为0.100mol·L-1 。请分别求出原混合液中氯离子、硫酸根离子的物质的量浓度。(设溶液总体积始终不变)____
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】氧化镁在易燃材料中常被用作阻燃剂,碳酸镁高温分解法是工业上制备轻质氧化镁的常用方法。镁硅矿主要成分为Mg3(Si2O5)(OH)4和少量的Fe2O3、Al2O3等。以镁硅矿为原料制备碳酸镁晶体(MgCO3•nH2O)的生产流程如图:
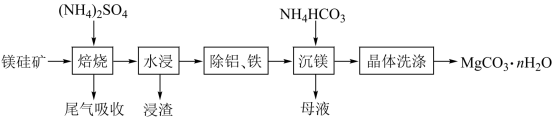
已知“焙烧”过程中的主要反应为:Mg3(Si2O5)(OH)4+5(NH4)2SO4 3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
为测定产品MgCO3•nH2O中的n值,称取15.6g产品进行充分加热至恒重,冷却,称得固体质量为4g,则n=_______ 。

已知“焙烧”过程中的主要反应为:Mg3(Si2O5)(OH)4+5(NH4)2SO4
 3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑为测定产品MgCO3•nH2O中的n值,称取15.6g产品进行充分加热至恒重,冷却,称得固体质量为4g,则n=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】已知稀硝酸和铜能发生反应,生成硝酸铜、一氧化氮气体和水。
(1)请写出该反应的化学方程式,并用双线桥法标出反应中电子转移的方向和数目。________
(2)一次实验中,某同学用过量的稀硝酸(其密度为1.08 g·mL-1,HNO3的质量分数为12%)跟一定量的铜片反应,产生了标准状况下0.56 L的一氧化氮。试计算(简要写出计算过程):
①该稀硝酸的物质的量浓度(结果保留小数点后一位);______________
②被还原的HNO3的物质的量。________________
(1)请写出该反应的化学方程式,并用双线桥法标出反应中电子转移的方向和数目。
(2)一次实验中,某同学用过量的稀硝酸(其密度为1.08 g·mL-1,HNO3的质量分数为12%)跟一定量的铜片反应,产生了标准状况下0.56 L的一氧化氮。试计算(简要写出计算过程):
①该稀硝酸的物质的量浓度(结果保留小数点后一位);
②被还原的HNO3的物质的量。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】磷及部分重要化合物的相互转化如图所示.

①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是________ ;
②不慎将白磷沾到皮肤上,可用0.2mol/LCuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol/LCuSO4溶液所能氧化的白磷的物质的量为________ .

①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是
②不慎将白磷沾到皮肤上,可用0.2mol/LCuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol/LCuSO4溶液所能氧化的白磷的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】氯气的实验室制法有多种,其中一种可以用重铬酸钾和浓盐酸制取。其变化可表述为:K2Cr2O7+14HCl (浓)=2KCl+2CrCl3+3Cl2 ↑+7H2O。
(1)请标出上述方程式的电子转移方向和数目__________ 。
(2)上述反应中被还原的元素为________ 。
(3)氧化产物与还原产物的物质的量之比为___________ 。
(4)浓盐酸在反应中显示出来的性质是________________ 。
(5)若有14.7g K2Cr2O7 发生上述反应,则转移的电子数为_____ 个, 产生的气体在标准状况下的体积为________ L。
(1)请标出上述方程式的电子转移方向和数目
(2)上述反应中被还原的元素为
(3)氧化产物与还原产物的物质的量之比为
(4)浓盐酸在反应中显示出来的性质是
(5)若有14.7g K2Cr2O7 发生上述反应,则转移的电子数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】有一硫酸和硝酸的混合溶液,取出20mL,加入足量BaCl2溶液,经过滤、洗涤、烘干后得沉淀9.32g;滤液与4mol/L的苛性钠溶液35mL恰好完全中和。试求:
(1)原混合溶液中硫酸和硝酸的物质的量浓度。__________
(2)另取10mL原溶液,加入0.96g铜粉共热,生成一氧化氮的体积为多少?(S.T.P.)__________
(3)另取10mL原溶液,加入1.92g铜粉共热,生成一氧化氮的体积为多少?(S.T.P.)__________
(4)向(3)反应后的溶液中加入多少毫升1mol/L硫酸就能将1.92g铜恰好完全溶解?__________
(1)原混合溶液中硫酸和硝酸的物质的量浓度。
(2)另取10mL原溶液,加入0.96g铜粉共热,生成一氧化氮的体积为多少?(S.T.P.)
(3)另取10mL原溶液,加入1.92g铜粉共热,生成一氧化氮的体积为多少?(S.T.P.)
(4)向(3)反应后的溶液中加入多少毫升1mol/L硫酸就能将1.92g铜恰好完全溶解?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,生成的气体为NO、 。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗
。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗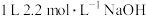 溶液和
溶液和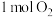 ,则生成的NO、
,则生成的NO、 的物质的量分别为
的物质的量分别为_______ 、_______ ,生成硫酸铜的物质的量为_________________ 。
 。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗
。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗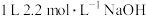 溶液和
溶液和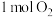 ,则生成的NO、
,则生成的NO、 的物质的量分别为
的物质的量分别为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】把2.0 mol/L Fe2(SO4)3溶液和2.0 mol/L H2SO4等体积混合(假设混合后溶液的体积等于混合前溶液的体积之和)。计算:(写出计算过程)
(1)混合液中Fe3+的物质的量浓度;
(2)混合液中H+、SO42—的物质的量浓度;
(3)向溶液中加入足量铁粉,经足够长时间后,铁粉有剩余, 求此时溶液中FeSO4的物质的量浓度。
(已知加入铁粉时先发生Fe+ Fe2(SO4)3="3Fe" SO4 反应,后发生Fe+ H2SO4="Fe" SO4+ H2)
(4)假设混和后的溶液为2L,加入一定量Fe粉后放出H2在标准状况下的体积为16.8L,求最终溶液中H+物质的量浓度。
(1)混合液中Fe3+的物质的量浓度;
(2)混合液中H+、SO42—的物质的量浓度;
(3)向溶液中加入足量铁粉,经足够长时间后,铁粉有剩余, 求此时溶液中FeSO4的物质的量浓度。
(已知加入铁粉时先发生Fe+ Fe2(SO4)3="3Fe" SO4 反应,后发生Fe+ H2SO4="Fe" SO4+ H2)
(4)假设混和后的溶液为2L,加入一定量Fe粉后放出H2在标准状况下的体积为16.8L,求最终溶液中H+物质的量浓度。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】浓硫酸和铜在加热时反应,生成SO2气体的体积为3.36L(标准状况下)。已知:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O。试计算:(写出计算过程)
CuSO4+SO2↑+2H2O。试计算:(写出计算过程)
(1)SO2气体的物质的量是多少?___
(2)参加反应的硫酸的物质的量是多少?___
(3)将生成的硫酸铜配制成500mL溶液,则该溶液中溶质的物质的量浓度是多少?___
 CuSO4+SO2↑+2H2O。试计算:(写出计算过程)
CuSO4+SO2↑+2H2O。试计算:(写出计算过程)(1)SO2气体的物质的量是多少?
(2)参加反应的硫酸的物质的量是多少?
(3)将生成的硫酸铜配制成500mL溶液,则该溶液中溶质的物质的量浓度是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将5.76 g铜粉投入30mL的浓HNO3中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,铜粉恰好与HNO3完全反应,共收集到标准状况下由NO2和NO组成的混合气体3. 36 L。
请回答下列问题:
(1)被还原的HNO3有___________ mol
(2)HNO3物质的量浓度为___________
(3)标准状况下,混合气体中NO的体积为___________ L。
请回答下列问题:
(1)被还原的HNO3有
(2)HNO3物质的量浓度为
(3)标准状况下,混合气体中NO的体积为
您最近一年使用:0次



