A、B、C、D、E、F为原子序数依次增大的短周期元素,其中A与E同主族,B与F同主族,E与F同周期,已知常温下A、E单质的状态不同,D原子的核电荷数是B原子最外层电子数的2倍,F单质是一种重要的半导体材料。下列说法正确的是
| A.原子半径由大到小的顺序是:C>D>E>F |
| B.由A、C和D三种元素组成的化合物中可能含有离子键 |
| C.F、C、B元素最高价氧化物对应的水化物的酸性依次增强 |
| D.F与D形成的化合物质地坚硬,既不与酸反应也不与碱反应 |
9-10高二·河北石家庄·阶段练习 查看更多[1]
(已下线)2010年河北正定中学高三年级第四次考试
更新时间:2016-12-09 00:31:24
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是( )
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -1 |
| A.A、B的单质与稀盐酸反应速率B>A |
| B.D、E形成的简单离子的还原性E->D- |
| C.气态氢化物的稳定性HD<H2C |
| D.E的氧化物的水化物的酸性一定比C的强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】几种短周期元素的原子半径及主要化合价如表所示,下列说法中正确的是
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
A.X,Y元素的金属性: |
B.离子半径: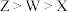 |
C.一定条件下,Z单质与W的常见单质直接生成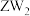 |
| D.工业上通过电解熔融的Y的氯化物来冶炼Y |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某物质结构如图所示,其中X、Y、Z、R、W分别位于3个短周期且原子序数依次增大,Y的某种同位素常用于测定文物的年代,下列说法正确的是


| A.X、Y、R、W形成的化合物对应水溶液可能呈酸性 |
| B.简单离子半径:W>Z>R |
| C.Z的氢化物的稳定性和沸点都高于Y的氢化物 |
| D.Y和W的单质均能导电 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】短周期主族元素X、Y、 Z、W的原子序数依次增大。X的气态氢化物能与其最高价含氧酸化合成盐,Z是同周期元素中原子半径最大的元素,Y和W同主族且二者可形成WY2和WY3两种物质。下列说法正确的是
| A.W的简单气态氢化物的热稳定性比Y的弱 |
| B.第一电离能: Y>X |
| C.简单离子半径: Z>Y>X |
| D.W在周期表中位于第3周期IVA族 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列物质含有离子键的是( )
| A.H2O2 | B.CO2 | C.NH3 | D.NaOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】2017年1月,南京理工大学胡炳成教授团队成功合成世界上首个高能全氮阴离子盐,全氮阴离子化学式为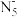 。下列关于全氮阴离子盐的说法不正确的是
。下列关于全氮阴离子盐的说法不正确的是
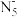 。下列关于全氮阴离子盐的说法不正确的是
。下列关于全氮阴离子盐的说法不正确的是A.每个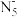 含有36个电子 含有36个电子 | B.全氮阴离子盐为离子化合物 |
| C.全氮阴离子盐既含离子键又含共价键 | D.由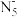 获得N2需要吸热 获得N2需要吸热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】科学家根据自然界存在的N2制取N3,其后又陆续制取出N5、含N5+的化合物及N60。N5+极不稳定,需保存在-80℃的干冰中;N5+由于其极强的爆炸性,又称为“盐粒炸弹”;N60与C60结构相似,并在受热或机械撞击后,其中积蓄的巨大能量会在瞬间释放出来。分析上述材料,下列说法中不正确的是
A. 常温下会剧烈爆炸,体积急剧膨胀,放出大量的热 常温下会剧烈爆炸,体积急剧膨胀,放出大量的热 |
| B.N60的发现开辟了能源世界的新天地,将来可能成为很好的火箭燃料 |
| C.N2、N3、N5、N5+、N60互为同素异形体 |
| D.含N5+的化合物中既有离子键又有共价键 |
您最近一年使用:0次