下列说法正确的是
| A.原子晶体中只存在非极性共价键 | B.稀有气体形成的晶体属于分子晶体 |
| C.干冰升华时,分子内共价键会发生断裂 | D.金属元素和非金属元素形成的化合物一定是离子化合物 |
2007·江苏·高考真题 查看更多[14]
陕西省西安市周至县第四中学2022-2023学年高二下学期期末考试化学试题新疆疏勒县实验学校2021-2022学年高二下学期期末考试化学试题甘肃省庆阳市第六中学2021-2022学年高二下学期期末考试化学试题新疆生产建设兵团第四师第一中学2019-2020学年高二下学期期中考试化学试题云南省开远市第二中学校2019-2020学年高二上学期期末考试化学试题云南省绿春县高级中学2019-2020学年高二上学期期末考试化学试题云南省富宁县三中2019-2020学年高二上学期期末考试化学试题云南省玉溪市景东一中2018-2019学年高二6月份考试化学试题云南省大关县一中2018-2019学年高二上学期12月考试化学试题人教版2017-2018学年高二化学选修三同步训练:第三章 晶体结构与性质2(已下线)2012-2013福建省仙游二中高二下学期第一次月考化学试卷(已下线)2012-2013年江苏泰州二中高二第一次(10月)限时作业化学试卷(已下线)2011-2012学年甘肃省甘谷一中高二下学期期中考试化学试卷2007年普通高等学校招生全国统一考试(江苏卷)化学试题
更新时间:2019-01-30 18:14:09
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】反应3Cl2+8NH3=N2+6NH4Cl常用于检验运输氯气的管道是否发生泄漏。下列表示反应中相关微粒的化学用语正确的是
A.中子数为18的氯原子: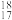 Cl Cl |
B.用电子式表示氨气分子的形成过程: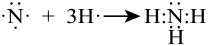 |
| C.N2的结构式:N=N |
| D.NH4Cl中有离子键和非极性键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法中错误是的
| A.单质中不存在离子键 |
| B.含有离子键的化合物一定是离子化合物 |
| C.含有共价键的化合物一定是共价化合物 |
| D.在一种物质中可能同时含有离子键、极性键和非极性键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】X、Y为第三周期元素、Y最高正价与最低负价的代数和为6,二者形成的一种化合物能以[XY4]+[XY6]-的形式存在。下列说法不正确的是
| A.简单氢化物的稳定性:X>Y |
| B.原子半径:X>Y |
| C.X和Y的单质可以发生化合反应得到XY3或XY5 |
| D.化合物[XY4]+[XY6]-中既有离子键又有共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】W、X、Y、Z均为短周期元素,W的最外层电子数是次外层的3倍,X、Y处在同一周期,X、Y的原子最外层电子数分别为1、3,Z原子的M电子层有7个电子,下列说法一定正确的是
| A.单质沸点:X>Y>Z | B.离子半径:Z->X- |
| C.Z分别与X、Y形成的化合物中均只含离子键 | D.原子序数:Z>Y>X>W |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】1828年,德国化学家维勒在制备无机盐氰酸铵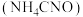 时得到了尿素
时得到了尿素 ,第一次通过人工的方法将无机物转变成有机物,打破了无机物和有机物的界限.下列关于尿素的叙述
,第一次通过人工的方法将无机物转变成有机物,打破了无机物和有机物的界限.下列关于尿素的叙述不正确 的是
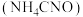 时得到了尿素
时得到了尿素 ,第一次通过人工的方法将无机物转变成有机物,打破了无机物和有机物的界限.下列关于尿素的叙述
,第一次通过人工的方法将无机物转变成有机物,打破了无机物和有机物的界限.下列关于尿素的叙述| A.尿素是人体新陈代谢的一种产物 | B.尿素与氰酸铵均属于共价化合物 |
| C.尿素与氰酸铵互为同分异构 | D.工业上用氨气和二氧化碳在高温高压下合成尿素的反应是非氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中正确的有
①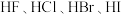 的熔沸点依次升高
的熔沸点依次升高
② 的热稳定性依次减弱
的热稳定性依次减弱
③硬度由大到小:金刚石>碳化硅>晶体硅
④分子晶体的熔点一定比金属晶体的低
⑤水结成冰,密度减小,与水分子之间能形成氢键有关
⑥金属晶体的导电性、导热性,均与自由电子有关
①
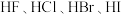 的熔沸点依次升高
的熔沸点依次升高②
 的热稳定性依次减弱
的热稳定性依次减弱③硬度由大到小:金刚石>碳化硅>晶体硅
④分子晶体的熔点一定比金属晶体的低
⑤水结成冰,密度减小,与水分子之间能形成氢键有关
⑥金属晶体的导电性、导热性,均与自由电子有关
| A.②③⑤⑥ | B.①②③⑥ | C.②③④⑤ | D.①②⑤⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述正确的有
①冰的密度小于水,是因为冰中水分子的氢键导致分子间出现较大空隙
②两种不同非金属元素原子间形成的化学键都是极性键
③氢键是共价键的一种
④一般来说,对于组成和结构相似的分子,相对分子质量越大,分子间作用力越大,熔沸点越高,所以HF、HCl、HBr、HI的沸点依次升高
⑤某化合物在熔融态时能导电,则该化合物一定是离子化合物
⑥单质分子中不存在化学键,化合物的分子中才存在化学键
⑦离子化合物中一定含有离子键,共价化合物中一定没有离子键
⑧H2O比 更稳定,是因为H2O分子间存在氢键
更稳定,是因为H2O分子间存在氢键
①冰的密度小于水,是因为冰中水分子的氢键导致分子间出现较大空隙
②两种不同非金属元素原子间形成的化学键都是极性键
③氢键是共价键的一种
④一般来说,对于组成和结构相似的分子,相对分子质量越大,分子间作用力越大,熔沸点越高,所以HF、HCl、HBr、HI的沸点依次升高
⑤某化合物在熔融态时能导电,则该化合物一定是离子化合物
⑥单质分子中不存在化学键,化合物的分子中才存在化学键
⑦离子化合物中一定含有离子键,共价化合物中一定没有离子键
⑧H2O比
 更稳定,是因为H2O分子间存在氢键
更稳定,是因为H2O分子间存在氢键| A.2项 | B.3项 | C.4项 | D.5项 |
您最近一年使用:0次



