A、B、C、D、E、F六种短周期元素,其原子序数依次增大,在所有元素中A的原子半径最小,B原子最外层电子数是次外层的2倍。A、 E同主族,D、F同主族,且D、F的原子序数之和为
A、E的原子序数之和的2倍,请回答下列问题:
(1) 写出下列元素的名称:C____________ E_____________ ;
(2) A 、C能形成多种化合物,其中C2A4的结构式为_______ (用元素符号回答,下同);
(3) 化合物E2D2中存在的化学键类型为_______________________________ ;
(4) 由A、D、E、F四种元素形成的两种化合物,在水溶液中两者反应的离子方程式为
___________________ ;
(5) B的单质可与A、D、F形成化合物的浓溶液反应,为检验所有生成物,被检验物质的顺序依次为________________________ 。
A、E的原子序数之和的2倍,请回答下列问题:
(1) 写出下列元素的名称:C
(2) A 、C能形成多种化合物,其中C2A4的结构式为
(3) 化合物E2D2中存在的化学键类型为
(4) 由A、D、E、F四种元素形成的两种化合物,在水溶液中两者反应的离子方程式为
(5) B的单质可与A、D、F形成化合物的浓溶液反应,为检验所有生成物,被检验物质的顺序依次为
10-11高三上·河南·阶段练习 查看更多[2]
更新时间:2010/12/23 16:47:53
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】按要求填空
(1)甲烷在氧气中充分燃烧的化学方程式_________
(2)甲烷的电子式_______
(3)正丁烷的分子式______
(4)用电子式表示NaCl的形成过程___________
(5)画出钠原子结构示意图_______
(1)甲烷在氧气中充分燃烧的化学方程式
(2)甲烷的电子式
(3)正丁烷的分子式
(4)用电子式表示NaCl的形成过程
(5)画出钠原子结构示意图
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】化学用语是中学化学基础知识的重要组成部分,是学习化学的重要工具。用化学用语回答下列问题:
(1)熔点最低的金属为___________ 。
(2)硫原子的结构示意图为___________ 。
(3)中子数为18的氯离子可表示为___________ 。
(4)空气中含量最多的气体的电子式为___________ 。
(5)短周期元素组成的最强的无机酸与 反应的离子方程式为
反应的离子方程式为___________ 。
(6)用电子式表示 的形成过程:
的形成过程:___________ 。
(1)熔点最低的金属为
(2)硫原子的结构示意图为
(3)中子数为18的氯离子可表示为
(4)空气中含量最多的气体的电子式为
(5)短周期元素组成的最强的无机酸与
 反应的离子方程式为
反应的离子方程式为(6)用电子式表示
 的形成过程:
的形成过程:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】CO2是一种自然界大量存在的“碳源”化合物,借助零碳能源(太阳能等)制得的H2可将CO2转化为燃料,能缓解温室效应和解决能源危机问题。
(1)硅太阳能电池可实现太阳能向电能的转化,Si在元素周期表中的位置____ 。
(2)电解水制H2,阴极电极反应式是____ 。
(3)聚乙烯亚胺捕获CO2并原位氢化为甲醇,反应历程如图1所示。____ 。
②写出生成甲醇的总反应_____ 。
(4)微生物电解池能将CO2转化为CH4,其工作原理如图2所示,写出所有生成CH4的反应_____ 。
(1)硅太阳能电池可实现太阳能向电能的转化,Si在元素周期表中的位置
(2)电解水制H2,阴极电极反应式是
(3)聚乙烯亚胺捕获CO2并原位氢化为甲醇,反应历程如图1所示。

②写出生成甲醇的总反应
(4)微生物电解池能将CO2转化为CH4,其工作原理如图2所示,写出所有生成CH4的反应

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】在研究原子核外电子排布与元素周期表的关系时,人们发现价电子排布相似的元素集中在一起。据此,人们将元素周期表分为五个区,并以最后填入电子的轨道能级符号作为该区的符号,如图所示。
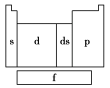
(1)在s区中,族序数最大、原子序数最小的元素,原子的价电子的电子云形状为___________ 。
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为 Fe2+:1s22s22p63s23p63d6,Fe3+:1s22s22p63s23p63d5,其中较稳定的是___________ 。
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为___________ 。
(4)在p区中,第二周期第ⅤA族元素原子的轨道表示式为___________ 。
(5)当今常用于核能开发的元素是铀和钚,它们在___________ 区中。

(1)在s区中,族序数最大、原子序数最小的元素,原子的价电子的电子云形状为
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为 Fe2+:1s22s22p63s23p63d6,Fe3+:1s22s22p63s23p63d5,其中较稳定的是
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为
(4)在p区中,第二周期第ⅤA族元素原子的轨道表示式为
(5)当今常用于核能开发的元素是铀和钚,它们在
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某微粒的结构示意图为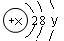 试回答:
试回答:
(1)当x-y=10时,该粒子为_____ (填“原子”或“阳离子”“阴离子”)
(2)当y=8时,该粒子可能是(写名称):____ 、____ 、____ 、____ 、_____ 。
(3)写出y=3与y=7的元素最高价氧化物对应水化物发生反应的离子方程式_______ 。
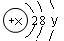 试回答:
试回答:(1)当x-y=10时,该粒子为
(2)当y=8时,该粒子可能是(写名称):
(3)写出y=3与y=7的元素最高价氧化物对应水化物发生反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】夏天时有一种叫盐汽水的饮料其中主要含有 NaCl、CO2、H2O,按要求回答:
(1)NaCl 的电子式:___________ 、所含化学键的类型为:___________ 、 用电子式表示其形成过程:___________ 。
(2)CO2 的结构式:___________ 、所含化学键的类型为:___________
(3)H2O 的电子式:___________ 、化合物类型为:___________ (离子化合物或共价化合物)
(1)NaCl 的电子式:
(2)CO2 的结构式:
(3)H2O 的电子式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】I.有下列物质:①Na2O ②NaOH ③NH4Cl ④CO2 ⑤H2S ⑥Ar
⑦H2SO4 ⑧KCl (填序号)
(1)属于离子化合物的是___________ ,属于共价化合物的是___________ 。
(2)只含有离子键的是___________ ,既含有离子键又含有共价键的是___________ 。
(3)不存在化学键的是______________ 。
Ⅱ.
(4)BBr3的熔点是-46 ℃,KBr的熔点是734 ℃,其水溶液能导电。根据熔点分析,BBr3可能属于_ 晶体,KBr可能属于__ 晶体。
(5)BaCl2是无色晶体,熔点963 ℃,沸点1 560 ℃,易溶于水,在熔化状态能导电。它可能属于__ 晶体,写出BaCl2的电子式:____ 。
(6)SiC和CO2物质中的化学键均为共价键,SiC的熔点高且硬度大,而CO2的晶体干冰却松软而且极易升华。由此可判断,CO2是____ 晶体,而SiC可能是____ 晶体。
Ⅲ.配平下列氧化还原反应方程式:
(7)______Fe+_____HNO3=______Fe(NO3)3+______NO↑+______H2O;_____ 。
(8)______MnO +_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;
+_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;_____
⑦H2SO4 ⑧KCl (填序号)
(1)属于离子化合物的是
(2)只含有离子键的是
(3)不存在化学键的是
Ⅱ.
(4)BBr3的熔点是-46 ℃,KBr的熔点是734 ℃,其水溶液能导电。根据熔点分析,BBr3可能属于
(5)BaCl2是无色晶体,熔点963 ℃,沸点1 560 ℃,易溶于水,在熔化状态能导电。它可能属于
(6)SiC和CO2物质中的化学键均为共价键,SiC的熔点高且硬度大,而CO2的晶体干冰却松软而且极易升华。由此可判断,CO2是
Ⅲ.配平下列氧化还原反应方程式:
(7)______Fe+_____HNO3=______Fe(NO3)3+______NO↑+______H2O;
(8)______MnO
 +_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;
+_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】将少量饱和FeCl3溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
甲:饱和FeCl3溶液滴加到冷水中;
乙:饱和FeCl3溶液滴加到NaOH溶液中;
丙:饱和FeCl3溶液滴加到沸水中。
(1)将丙继续加热煮沸得到红褐色透明液体,反应的化学方程式为___________ 。
(2)用最简单的方法判断丙中是否成功制备胶体,请写出相关的操作、现象和结论___________ 。
(3)向经过检验后的丙中逐滴加入稀盐酸,会出现一系列变化:
①先出现和乙中相同的现象,原因为___________ 。
②随后发生变化得到和甲相同的溶液,此反应的离子反应方程式为___________ 。
(4)向丙中加入电极通电后,Fe(OH)3胶体粒子移向___________ 极;(填“阴极”或“阳极”)
(5)可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若___________ (填实验现象),则说明该Fe(OH)3胶体中的杂质离子已经完全除去。
甲:饱和FeCl3溶液滴加到冷水中;
乙:饱和FeCl3溶液滴加到NaOH溶液中;
丙:饱和FeCl3溶液滴加到沸水中。
(1)将丙继续加热煮沸得到红褐色透明液体,反应的化学方程式为
(2)用最简单的方法判断丙中是否成功制备胶体,请写出相关的操作、现象和结论
(3)向经过检验后的丙中逐滴加入稀盐酸,会出现一系列变化:
①先出现和乙中相同的现象,原因为
②随后发生变化得到和甲相同的溶液,此反应的离子反应方程式为
(4)向丙中加入电极通电后,Fe(OH)3胶体粒子移向
(5)可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】无机化合物可根据其组成和性质进行分类。
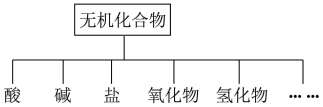
(1)上图所示的物质分类方法名称是____________ 。
(2)以钠、钾、氢、氧、碳、硫、氮中任两种或三种元素组成合适的物质,分别填在下表中的横线上:
(3)写出⑦转化为⑤的化学方程式__________ 。
(4)写出实验室由⑩制备氧气的化学方程式______ 。
(5)实验室制备⑦常用________ 和________ 反应,检验该气体的方法是________ 。

(1)上图所示的物质分类方法名称是
(2)以钠、钾、氢、氧、碳、硫、氮中任两种或三种元素组成合适的物质,分别填在下表中的横线上:
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ② | ③ ④Ba(OH)2 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(4)写出实验室由⑩制备氧气的化学方程式
(5)实验室制备⑦常用
您最近一年使用:0次








