由地壳中含量最高的金属元素和非金属组成的化合物的名称是________ ,铁红常用于制造红色油漆和涂料,它的化学式是____________ .
10-11高一上·江西九江·阶段练习 查看更多[1]
(已下线)2010年江西省九江一中高一上学期第二次月考化学试卷
更新时间:2010/12/28 10:07:40
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】下图所涉及的物质均为中学化学中的常见物质,其中C为O2、D为Cl2、E为Fe单质,其余为化合物,它们存在如下转化关系,反应中生成的水及次要产物均已略去。
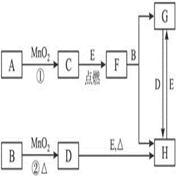
(1)写出有关物质的名称或化学式:B______ ,F______ ,H______ 。
(2)指出MnO2在相关反应中的作用:反应①中是______ 剂,反应②中是______ 剂。
(3)若反应①是在加热条件下进行,则A是______ ;若反应①是在常温条件下进行,则A是______ 。
(4)写出B与MnO2共热获得D的化学方程式:______ 。

(1)写出有关物质的名称或化学式:B
(2)指出MnO2在相关反应中的作用:反应①中是
(3)若反应①是在加热条件下进行,则A是
(4)写出B与MnO2共热获得D的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)W元素在周期表中的位置为______________ ;写出Y元素原子的价电子排布式:______________ ;
(2)由X、Z两元素可以组成A、B两种化合物,A在一定条件下可以分解成B,A的分子属于______________ (填“极性”、“非极性”)分子。
(3)一定条件下,Y的单质气体与X的单质气体充分反应生成6.8g C气体(已知n(X):n(Y)=3:1)可放出18.44 kJ热量,则该反应的热化学方程式为___________________ 。
(4)由X、Y、Z、W四种元素组成的一种离子化合物D
①已知1mol D能与足量NaOH浓溶液反应生成标准状况下44.8L气体。写出加热条件下D与NaOH溶液反应的离子方程式___________________________________ 。
②又知D既能与盐酸反应,又能与氯水反应,写出D与氯水反应的离子方程式
_________________________________________________________ 。
(5)X的单质与Z的单质在KOH的浓溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通入X的单质气体,N极通入Z的单质气体,则M极的电极反应式为_________________________________________ 。
(1)W元素在周期表中的位置为
(2)由X、Z两元素可以组成A、B两种化合物,A在一定条件下可以分解成B,A的分子属于
(3)一定条件下,Y的单质气体与X的单质气体充分反应生成6.8g C气体(已知n(X):n(Y)=3:1)可放出18.44 kJ热量,则该反应的热化学方程式为
(4)由X、Y、Z、W四种元素组成的一种离子化合物D
①已知1mol D能与足量NaOH浓溶液反应生成标准状况下44.8L气体。写出加热条件下D与NaOH溶液反应的离子方程式
②又知D既能与盐酸反应,又能与氯水反应,写出D与氯水反应的离子方程式
(5)X的单质与Z的单质在KOH的浓溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通入X的单质气体,N极通入Z的单质气体,则M极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】绿水青山就是金山银山已成为全社会的共识,保护生态社会才能持续发展。某地的河道两侧附近分别有甲、乙两个化工厂,它们排放的工业废水各含 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的四种离子,单独排放时,污染很大,且乙厂排放的废水有颜色,若将两厂污水相互混合则几乎不会造成污染。
中的四种离子,单独排放时,污染很大,且乙厂排放的废水有颜色,若将两厂污水相互混合则几乎不会造成污染。
(1)甲厂污水中含有的四种离子分别是___________ 。
(2)乙厂污水中含有的四种离子分别是___________ 。
(3)两厂污水相互混合则几乎不会造成污染是因为分别生成了___________ 、___________ 、___________ 沉淀。最终溶液中只含一种溶质,可用于作物的肥料,其化学式为___________ 。
(4)写出把有颜色离子除去的离子方程式为___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的四种离子,单独排放时,污染很大,且乙厂排放的废水有颜色,若将两厂污水相互混合则几乎不会造成污染。
中的四种离子,单独排放时,污染很大,且乙厂排放的废水有颜色,若将两厂污水相互混合则几乎不会造成污染。(1)甲厂污水中含有的四种离子分别是
(2)乙厂污水中含有的四种离子分别是
(3)两厂污水相互混合则几乎不会造成污染是因为分别生成了
(4)写出把有颜色离子除去的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】有下列物质:①过氧化钠、②氧化铝、③硅、④二氧化硅。请根据它们的用途填空:
(1)能作光导纤维的是___________ (填序号,下同)。
(2)可用于呼吸面具中作为氧气来源的是___________ 。
(3)能作耐火材料的金属氧化物是___________ 。
(1)能作光导纤维的是
(2)可用于呼吸面具中作为氧气来源的是
(3)能作耐火材料的金属氧化物是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据下列实验操作,回答问题:
(1)将在空气中久置的铝箔放在酒精灯火焰上加热,观察到的现象是_________________ ,上述变化的原因是______________ 。
(2)将用砂纸仔细打磨过的铝箔放在酒精灯火焰上加热,观察到的现象是_________________ ,上述变化的原因是____________________ 。
(3)将铝箔在氧气中点燃,观察到的现象是__________ ,反应的化学方程式是_______ 。
(1)将在空气中久置的铝箔放在酒精灯火焰上加热,观察到的现象是
(2)将用砂纸仔细打磨过的铝箔放在酒精灯火焰上加热,观察到的现象是
(3)将铝箔在氧气中点燃,观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】材料与生产、生活和科技密切相关。回答下列问题:
(1)无机非金属材料与我们的生活联系密切。我国具有独立知识产权的电脑芯片“龙芯一号”填补了我国计算机史上空白,“龙芯一号”材料的化学式为______ ;传统的无机非金属材料在日常生活中有着广泛的运用。玻璃和水泥的生产中均用到的原料的名称是____ ,其中碳酸钠在玻璃熔炉中反应的化学方程式为____________ 。
(2)金属材料的应用更是广泛。工业常用30%FeCl3溶液腐蚀绝缘板上铜箔,制造印刷电路板。腐蚀废液中含有Fe3+、Fe2+、Cu2+离子。当向腐蚀液中加入足量的Fe粉,一定不存在的离子是________ ;用实验判定腐蚀液中含有Fe2+离子______________ 。
(1)无机非金属材料与我们的生活联系密切。我国具有独立知识产权的电脑芯片“龙芯一号”填补了我国计算机史上空白,“龙芯一号”材料的化学式为
(2)金属材料的应用更是广泛。工业常用30%FeCl3溶液腐蚀绝缘板上铜箔,制造印刷电路板。腐蚀废液中含有Fe3+、Fe2+、Cu2+离子。当向腐蚀液中加入足量的Fe粉,一定不存在的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】
| 化学式 | FeO | Fe2O3 | Fe3O4 |
| 俗名 | - | ① | ② |
| 颜色状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体(有磁性) |
| 溶解性 | 难溶于水 | 难溶于水 | 难溶于水 |
| 铁元素的化合价 | ③ | ④ | ⑤ |
| 稳定性 | 不稳定 | 稳定 | 稳定 |
| 类别 | 碱性氧化物 | 碱性氧化物 | 特殊氧化物 |
| 与H+反应的离子方程式 | ⑥ | ⑦ | ⑧ |
| 与CO反应的通式 | FexOy+yCO xFe+yCO2 xFe+yCO2 | ||
| 用途 | 用作油漆、涂料、油墨和橡胶的红色颜料 | ||
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】为了探究铁、铜及其化合物的性质,某同学设计并进行了下列实验。
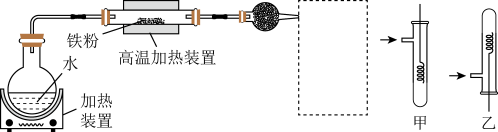
请回答:
(1)虚线框处宜选择的装置是___ (填“甲”或“乙”);实验时应将螺旋状铜丝加热,变黑后再趁热迅速伸入所制得的纯净氢气中,观察到的实验现象是___ 。
(2)硬质玻璃管中铁和水蒸气反应的化学方程式为___ (并用单线桥表示电子转移情况)。取硬质玻璃管中适量的固体,用一定浓度的盐酸溶解,滴加KSCN溶液,没有出现血红色,说明该固体中没有+3价的铁,判断结论是否正确并用文字和离子方程式说明理由___ 。

请回答:
(1)虚线框处宜选择的装置是
(2)硬质玻璃管中铁和水蒸气反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在3种物质①醋酸、②氧化铁、③氨气中,可用作红色颜料的是___________ (填序号,下同),可用做制冷剂的是__________ ,可清除水壶中水垢的是________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)常用作油漆、涂料的红色颜料(填写化学式)_________ ;
(2)写出H2O2的电子式_________ ;
(3)比较沸点:H2O___ H2S(填“>”“<”“=”),并解释原因___________________ 。
(4)Cl2可将碱性工业废水中的CN-氧化生成两种无毒物质,相应的离子方程式为___________________ 。
(1)常用作油漆、涂料的红色颜料(填写化学式)
(2)写出H2O2的电子式
(3)比较沸点:H2O
(4)Cl2可将碱性工业废水中的CN-氧化生成两种无毒物质,相应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁及其化合物在人类生活中有着极其重要的作用。完成下列填空:
(1)铁的原子结构示意图为 。由此可知,铁是第
。由此可知,铁是第_______ 周期元素,铁原子核外3d轨道上共填充了_______ 个电子。
(2)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是_______ (选填编号)。
a.Fe b.FeO c.Fe2O3 d.Fe3O4
(3)FeSO4可以用来净水、治疗缺铁性贫血等,实验室在配制FeSO4溶液时,为了防止FeSO4变质,经常向溶液中加入铁粉,其原因是_______ (用离子方程式表示)。
(4)向新配制的FeSO4溶液中,加入一定量的稀硝酸,发生如下反应:
_______Fe2++_______H++_______NO =_______Fe3++_______NO↑+_______H2O
=_______Fe3++_______NO↑+_______H2O
①配平上述反应_______ 。
②每生成0.5molNO气体,转移的电子数为_______ 。
③要检验该反应后的溶液中是否还含有Fe2+,实验方案是_______ 。
现在可以利用铁氧化物循环裂解水制备氢气,其过程如图所示:
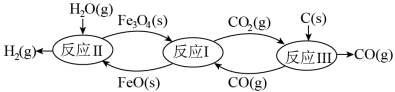
(5)写出反应Ⅲ的平衡常数表达式_______ 。
(6)写出铁氧化物循环裂解水制氢的总反应的化学方程式:_______ 。
(7)Fe3O4和CO的反应过程与温度密切相关。向某容器中加入Fe3O4与CO,当其它条件一定时,达到平衡时CO的体积百分含量随温度的变化关系如图所示。

已知:①Fe3O4+CO⇌3FeO+CO2-Q1(Q1>0)
②Fe3O4+4CO⇌3Fe+4CO2+Q2(Q2>0)
推测当温度达到570℃,平衡时CO体积百分含量最高的原因:_______ 。
(1)铁的原子结构示意图为
 。由此可知,铁是第
。由此可知,铁是第(2)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是
a.Fe b.FeO c.Fe2O3 d.Fe3O4
(3)FeSO4可以用来净水、治疗缺铁性贫血等,实验室在配制FeSO4溶液时,为了防止FeSO4变质,经常向溶液中加入铁粉,其原因是
(4)向新配制的FeSO4溶液中,加入一定量的稀硝酸,发生如下反应:
_______Fe2++_______H++_______NO
 =_______Fe3++_______NO↑+_______H2O
=_______Fe3++_______NO↑+_______H2O①配平上述反应
②每生成0.5molNO气体,转移的电子数为
③要检验该反应后的溶液中是否还含有Fe2+,实验方案是
现在可以利用铁氧化物循环裂解水制备氢气,其过程如图所示:

(5)写出反应Ⅲ的平衡常数表达式
(6)写出铁氧化物循环裂解水制氢的总反应的化学方程式:
(7)Fe3O4和CO的反应过程与温度密切相关。向某容器中加入Fe3O4与CO,当其它条件一定时,达到平衡时CO的体积百分含量随温度的变化关系如图所示。

已知:①Fe3O4+CO⇌3FeO+CO2-Q1(Q1>0)
②Fe3O4+4CO⇌3Fe+4CO2+Q2(Q2>0)
推测当温度达到570℃,平衡时CO体积百分含量最高的原因:
您最近一年使用:0次



