有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C燃烧时呈现黄色火焰,C的单质在点燃条件下与B的单质充分反应,可以得到淡黄色固态化合物,D的M层电子数为K层电子数的3倍.试根据以上叙述回答:
(1)写出元素名称:A_____ D_____ ;
(2)画出D的原子结构示意图____________ ;
(3)用电子式表示化合物C2D的形成过程___________________ .
(1)写出元素名称:A
(2)画出D的原子结构示意图
(3)用电子式表示化合物C2D的形成过程
更新时间:2016-12-09 16:01:54
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有A、B、C三种常见的短周期元素,它们的取子序数逐渐增大。A元素原子最外层电子数是次外层电子数的2倍,B元素原子最外层电子数等于其电子层数,且为C元素原子最外层电子数的一半。甲为含B的钠盐,乙为C的最高价氧化物对应的水化物,丙为含A的钠盐。 甲、乙、丙、丁四种物质之间的相互反应关系如下图:

请回答:
(1) 写出A的最高价的氧化物的电子式___________ ;C在周期表中的位置____________ 。
(2) 用有关化学用语解释丙溶液呈碱性的原因____________ 。
(3) 写出甲溶液与足量乙溶液反应的离子方程式:____________ 。

请回答:
(1) 写出A的最高价的氧化物的电子式
(2) 用有关化学用语解释丙溶液呈碱性的原因
(3) 写出甲溶液与足量乙溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C是短周期非金属元素,核电荷数依次增大。A元素原子核外有三种不同的能级且各个能级所填充的电子数相同,C是地壳中含量最多的元素。D、E是第四周期元素,其中E元素的核电荷数为29。D原子核外未成对电子数在同周期中最多。请用对应的元素符号或化学式填空:
(1)A、B、C的第一电离能由小到大的顺序为_____ 。
(2)B的氢化物易液化的原因是_______________________________________ ;
(3)已知A、C形成的化合物分子甲会造成温室效应,l mol甲中含有π键的数目为_______________ ;
(4)基态D原子的外围电子排布式为____ 。DO2Cl2熔点:-96.5℃,沸点:117℃,则固态DO2Cl2属于_____ 晶体。

(5)E的氢化物的晶胞结构如图所示,其化学式是________ 。
(1)A、B、C的第一电离能由小到大的顺序为
(2)B的氢化物易液化的原因是
(3)已知A、C形成的化合物分子甲会造成温室效应,l mol甲中含有π键的数目为
(4)基态D原子的外围电子排布式为

(5)E的氢化物的晶胞结构如图所示,其化学式是
您最近一年使用:0次
【推荐3】短周期元素A、B、C、D,A元素原子的最外层电子排布式为ms1,B元素原子的价电子排布式为ns2np2,C元素原子的最外层电子数是其电子层数的3倍,D元素原子的M电子层的p轨道中有3个未成对电子。
(1)若A为非金属元素,则A与C形成的化合物跟A与D形成的化合物相比,稳定性为_______ >_______ 。
(2)n=2时B的最高价氧化物对应的水化物与n=3时B的最高价氧化物对应的水化物相比,二者酸性_______ >________ ,验证该结论的实验是_______________________________________ 。
(3)若A元素的原子最外层电子排布式为2s1,B元素原子的价电子排布式为3s23p2,A、B、C、D四种元素的电负性由大到小的顺序是______________________ (用元素符号表示)。
(1)若A为非金属元素,则A与C形成的化合物跟A与D形成的化合物相比,稳定性为
(2)n=2时B的最高价氧化物对应的水化物与n=3时B的最高价氧化物对应的水化物相比,二者酸性
(3)若A元素的原子最外层电子排布式为2s1,B元素原子的价电子排布式为3s23p2,A、B、C、D四种元素的电负性由大到小的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知元素X、Y、Z质子数都小于18,并且质子数X+Y=Z。X原子的电子层数与核外电子总数相同,Z原子有两个电子层,最外层电子数是内层电子数的三倍,则:
(1)写出元素符号:X_______ , Y _________ ; Z的离子结构示意图为__________ 。
(2)由Y、Z组成,且质量比为7:20的化合物化学式为____________ 。
(3)X、Z可以形成两种常见化合物A和B,A中X、Z原子个数比为2 : 1,则A的摩尔质量为_____ ,实验室常用B制少量的氧气,写出化学反应方程式_____________________
(1)写出元素符号:X
(2)由Y、Z组成,且质量比为7:20的化合物化学式为
(3)X、Z可以形成两种常见化合物A和B,A中X、Z原子个数比为2 : 1,则A的摩尔质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知A、B、C、D、E都是短周期的主族元素,原子序数依次增大,其中A是空气中含量最多的元素,C是短周期中原子半径最大的元素,C与B可形成C2B和C2B2两种离子化合物,E是地壳中含量最多的金属元素。请回答下列问题:
(1)A在元素周期表中的位置为______ 。
(2)上述元素的最高价氧化物对应的水化物中碱性最强的是_____ (填化学式)。
(3)写出C2B2的电子式:_____ 。
(4)写出D的最高价氧化物对应水化物溶于稀硫酸的离子方程式:______ 。
(5)写出单质E与NaOH溶液反应的化学方程式:_____ 。
(1)A在元素周期表中的位置为
(2)上述元素的最高价氧化物对应的水化物中碱性最强的是
(3)写出C2B2的电子式:
(4)写出D的最高价氧化物对应水化物溶于稀硫酸的离子方程式:
(5)写出单质E与NaOH溶液反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】现有部分短周期主族元素的性质或原子结构如下表:
(1)元素X的一种同位素可测定文物年代,这种同位素的化学符号是___________ 。
(2)元素Y与氢元素形成一种阳离子,该阳离子为___________ 。
(3)元素Z与元素T相比,非金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ 。
a.常温下Z的单质和T的单质状态不同
b.Z的简单氢化物比T的简单氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)T的一种氧化物能使Z单质的水溶液褪色,该反应的离子方程式___________ 。
(5)T在周期表中的位置是第___________ 周期___________ 族。
| 元素编号 | 元素性质或原子结构 |
| T | M层上电子数是K层上电子数的3倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高化合价是+7价 |
(2)元素Y与氢元素形成一种阳离子,该阳离子为
(3)元素Z与元素T相比,非金属性较强的是
a.常温下Z的单质和T的单质状态不同
b.Z的简单氢化物比T的简单氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)T的一种氧化物能使Z单质的水溶液褪色,该反应的离子方程式
(5)T在周期表中的位置是第
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)相同物质的量的14C18O2与32S16O2的原子数之比为_______ ,中子数之比为_______ ,电子数之比为_______ 。
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为_______ (填代号)。
(3)利用元素周期律可预测陌生元素及物质的性质,已知Rb与Na处于同一主族,下列说法正确的是_______。
(1)相同物质的量的14C18O2与32S16O2的原子数之比为
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为_______ (填代号)。
A. | B.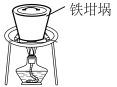 | C.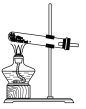 | D.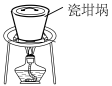 |
| A.失电子能力: Rb>Na |
| B.碱性: NaOH>RbOH |
| C.Rb比Na更易与氧气发生反应 |
| D.Rb不易与水反应放出H2 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】元素R所含的质子数与中子数相等,R的气态氢化物化学式为H2R.在标准状况下,8.5gH2R气体的体积是5.6L.
(1)求H2R的相对分子质量;
(2)推断R元素的名称;
(3)确定R在元素周期表中的具体位置.
(1)求H2R的相对分子质量;
(2)推断R元素的名称;
(3)确定R在元素周期表中的具体位置.
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】钋(Po)是一种低熔点金属,极其稀有,毒性和放射性极强。回答下列问题:
(1) Po具有放射性,经
Po具有放射性,经 衰变成稳定的铅,在衰变过程中释放一个
衰变成稳定的铅,在衰变过程中释放一个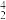 He2+,Pb的原子核中质子数为
He2+,Pb的原子核中质子数为____ ,中子数为____ ,Po元素能形成较稳定的+4价离子,wg Po4+含有的电子的物质的量为
Po4+含有的电子的物质的量为____ ;
(2)半衰期是指由大量原子组成的放射性样品中,放射性元素原子核有50%发生衰变所需的时间,已知 Po的半衰期为138天,质量为64克的
Po的半衰期为138天,质量为64克的 Po,经276天后,得到铅的质量为
Po,经276天后,得到铅的质量为____ 。
(1)
 Po具有放射性,经
Po具有放射性,经 衰变成稳定的铅,在衰变过程中释放一个
衰变成稳定的铅,在衰变过程中释放一个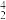 He2+,Pb的原子核中质子数为
He2+,Pb的原子核中质子数为 Po4+含有的电子的物质的量为
Po4+含有的电子的物质的量为(2)半衰期是指由大量原子组成的放射性样品中,放射性元素原子核有50%发生衰变所需的时间,已知
 Po的半衰期为138天,质量为64克的
Po的半衰期为138天,质量为64克的 Po,经276天后,得到铅的质量为
Po,经276天后,得到铅的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知X、Y、Z、W、Q、M为六种原子序数依次增大的短周期主族元素。元素W为地壳中含量最高的金属元素,元素Y与Q同主族,且Q的原子序数是Y的两倍,金属元素Z可与X组成电子总数为12的化合物ZX。请用实际推断的元素或化学式回答以下问题:
(1)M元素在周期表中的位置是:___________ 。
(2)Q的简单阴离子结构示意图:___________ 。
(3)Y与Q两者的氢化物的稳定性较强的是:___________ (填化学式);请从原子结构的角度解释其原因:___________ 。
(4)比较W、Z、Y的简单离子半径由大到小的顺序是:___________ 。
(5)元素W的单质与Z的最高价氧化物水化物反应的化学方程式:___________ 。
(6)用电子式表示ZX的形成过程:___________ 。
(7)R元素位于元素周期表第五周期,与Z同主族。下列说法正确的是:___________ 。
A.R有一种氧化物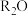 B.
B. 具有很强的氧化性
具有很强的氧化性
C.R的原子序数为37 D.R的熔沸点比Z小
E.RCl是一种白色沉淀 F.R放到水中会比Z跟水反应缓慢
(1)M元素在周期表中的位置是:
(2)Q的简单阴离子结构示意图:
(3)Y与Q两者的氢化物的稳定性较强的是:
(4)比较W、Z、Y的简单离子半径由大到小的顺序是:
(5)元素W的单质与Z的最高价氧化物水化物反应的化学方程式:
(6)用电子式表示ZX的形成过程:
(7)R元素位于元素周期表第五周期,与Z同主族。下列说法正确的是:
A.R有一种氧化物
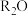 B.
B. 具有很强的氧化性
具有很强的氧化性C.R的原子序数为37 D.R的熔沸点比Z小
E.RCl是一种白色沉淀 F.R放到水中会比Z跟水反应缓慢
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】原子序数由小到大排列的四种短周期元素X、Y、Z、W四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。M元素与X同主族,与W同周期。
(1) Z、W形成的气态氢化物的稳定性为___________ >___________ ,(填化学式)写出下列元素的名称:X_______ 、W_______ ,Z、M、W三种元素离子半径由大到小的顺序是 _________ (填相应的离子符号)。
(2) 由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,写出该反应的化学反应方程式________________ ,若有19.2g铜参加反应则会生成标准状况下气体体积为________ 。
(3) 用电子式表示M2W的形成过程_____________________________________________
(4) 由M、Z两元素形成的原子个数比为1∶1化合物的电子式为__________________ ,化学键类型是__________________
(5) 由X、Y、Z、W四种元素组成的一种盐A,已知:①1molA能与足量NaOH浓溶液反应生成标准状况下22.4L气体。②A能与盐酸反应产生气体B,该气体能与溴水反应。写出A的化学式_______________________________ ,该气体B与溴水反应的离子方程式____________ 。
(1) Z、W形成的气态氢化物的稳定性为
(2) 由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,写出该反应的化学反应方程式
(3) 用电子式表示M2W的形成过程
(4) 由M、Z两元素形成的原子个数比为1∶1化合物的电子式为
(5) 由X、Y、Z、W四种元素组成的一种盐A,已知:①1molA能与足量NaOH浓溶液反应生成标准状况下22.4L气体。②A能与盐酸反应产生气体B,该气体能与溴水反应。写出A的化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。表中列出了钙元素及a~f6种元素在周期表中的位置。
(1)a的元素符号是____ ;e的最高价氧化物是____ 。
(2)c、d的最高价氧化物对应的水化物中,碱性较弱的物质是____ (写化学式)。
(3)用电子式表示c与f组成的化合物的形成过程____ 。
(4)非金属性b强于e,用原子结构解释原因____ 。
(5)下列关于f及其化合物的推断中,正确的是____ (填字母)。
a.f的最高化合价均为+7价
b.f单质的氧化性在同主族中最强
c.f的最高价氧化物对应的水化物的溶液pH<7
(6)某种牛奶的营养成分表如表所示。
①营养成分表中,所含物质质量最大的是____ 。
②已知镁能与O2、H2O反应,对比钙与镁的原子结构和在元素周期表中的位置关系,你预测金属钙的性质是____ 。
③请结合钙的化学性质判断牛奶中钙的存在形式为____ (填“单质”或“化合物”)。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | a | b | ||||||
| 3 | c | d | e | f | ||||
| 4 | Ca |
(2)c、d的最高价氧化物对应的水化物中,碱性较弱的物质是
(3)用电子式表示c与f组成的化合物的形成过程
(4)非金属性b强于e,用原子结构解释原因
(5)下列关于f及其化合物的推断中,正确的是
a.f的最高化合价均为+7价
b.f单质的氧化性在同主族中最强
c.f的最高价氧化物对应的水化物的溶液pH<7
(6)某种牛奶的营养成分表如表所示。
| 营养成分表 | ||
| 项目 | 每100g | NRV% |
| 能量 | 309kJ | 4% |
| 蛋白质 | 3.6g | 6% |
| 脂肪 | 4.4g | 7% |
| 碳水化合物 | 5.0g | 2% |
| 钠 | 65mg | 3% |
| 钙 | 120mg | 15% |
②已知镁能与O2、H2O反应,对比钙与镁的原子结构和在元素周期表中的位置关系,你预测金属钙的性质是
③请结合钙的化学性质判断牛奶中钙的存在形式为
您最近一年使用:0次



