钋(Po)是一种低熔点金属,极其稀有,毒性和放射性极强。回答下列问题:
(1) Po具有放射性,经
Po具有放射性,经 衰变成稳定的铅,在衰变过程中释放一个
衰变成稳定的铅,在衰变过程中释放一个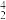 He2+,Pb的原子核中质子数为
He2+,Pb的原子核中质子数为____ ,中子数为____ ,Po元素能形成较稳定的+4价离子,wg Po4+含有的电子的物质的量为
Po4+含有的电子的物质的量为____ ;
(2)半衰期是指由大量原子组成的放射性样品中,放射性元素原子核有50%发生衰变所需的时间,已知 Po的半衰期为138天,质量为64克的
Po的半衰期为138天,质量为64克的 Po,经276天后,得到铅的质量为
Po,经276天后,得到铅的质量为____ 。
(1)
 Po具有放射性,经
Po具有放射性,经 衰变成稳定的铅,在衰变过程中释放一个
衰变成稳定的铅,在衰变过程中释放一个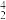 He2+,Pb的原子核中质子数为
He2+,Pb的原子核中质子数为 Po4+含有的电子的物质的量为
Po4+含有的电子的物质的量为(2)半衰期是指由大量原子组成的放射性样品中,放射性元素原子核有50%发生衰变所需的时间,已知
 Po的半衰期为138天,质量为64克的
Po的半衰期为138天,质量为64克的 Po,经276天后,得到铅的质量为
Po,经276天后,得到铅的质量为
更新时间:2019-10-30 22:27:52
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
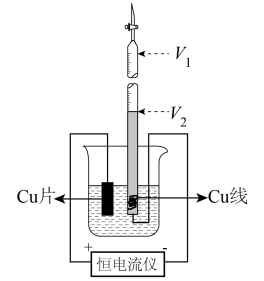
【推荐1】Cu2O主要在玻璃、搪瓷工业中作红色颜料。阿伏加德罗常数(NA)是化学中重要的物理常数。某实验小组利用下图装置电化学合成Cu2O并采用量气法测定阿伏加德罗常数的值(夹持装置略)。
实验步骤为:
Ⅱ.用砂纸打磨Cu片表面,洗涤干净,用滤纸擦干后插入烧杯内。
Ⅲ.取一段Cu线,把Cu线一端的绝缘层剥掉并弯成螺旋状,插入量气管的倒口中。
Ⅳ.将Cu片和Cu线分别连接恒电流仪的两极,进行电解实验。
Ⅴ.电解结束后,读出量气管中液面位置V2,离心分离出烧杯中的Cu2O固体,并用适量蒸馏水洗涤。
回答下列问题:
(1)量气管不采用酸式滴定管的原因是_______ 。该小组进行了多次平行实验,在每次实验中,量气管中液面位置V1应尽可能控制在同一位置,目的是_______ 。
(2)步骤Ⅱ中,Cu片打磨前,表面黑色物质的主要成分为_______ (写化学式)。
(3)步骤Ⅲ中,Cu线裸露部分应全部放在量气管内,目的是_______ 。
(4)电解时,Cu片附近首先析出白色的CuCl,进而转化为Cu2O。该条件下CuCl转化为Cu2O的离子方程式为_______ 。
(5)某次实验,电解电流为100.0mA,电解时间为722s,测量的体积折合成H2的物质的量为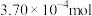 ,则NA值为
,则NA值为_______ (用科学计数法表示,保留2位小数,已知单个电子的电量约为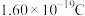 )。
)。
(6)步骤Ⅴ中,可通过检测洗出液中是否存在Cl-来判断洗涤是否完成。检测的方法是_____ 。
实验步骤为:
Ⅱ.用砂纸打磨Cu片表面,洗涤干净,用滤纸擦干后插入烧杯内。
Ⅲ.取一段Cu线,把Cu线一端的绝缘层剥掉并弯成螺旋状,插入量气管的倒口中。
Ⅳ.将Cu片和Cu线分别连接恒电流仪的两极,进行电解实验。
Ⅴ.电解结束后,读出量气管中液面位置V2,离心分离出烧杯中的Cu2O固体,并用适量蒸馏水洗涤。
回答下列问题:
(1)量气管不采用酸式滴定管的原因是
(2)步骤Ⅱ中,Cu片打磨前,表面黑色物质的主要成分为
(3)步骤Ⅲ中,Cu线裸露部分应全部放在量气管内,目的是
(4)电解时,Cu片附近首先析出白色的CuCl,进而转化为Cu2O。该条件下CuCl转化为Cu2O的离子方程式为
(5)某次实验,电解电流为100.0mA,电解时间为722s,测量的体积折合成H2的物质的量为
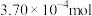 ,则NA值为
,则NA值为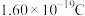 )。
)。(6)步骤Ⅴ中,可通过检测洗出液中是否存在Cl-来判断洗涤是否完成。检测的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组对化合物 (由3种元素组成)开展探究实验。
(由3种元素组成)开展探究实验。
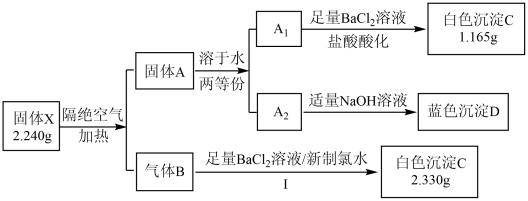
其中: 和
和 均为纯净物;
均为纯净物; 可使品红溶液褪色。请回答:
可使品红溶液褪色。请回答:
(1)白色沉淀 的化学式是
的化学式是_______ 。
(2)组成 的3种元素是
的3种元素是_______ (填元素符号)。
(3)写出步骤Ⅰ中反应的离子方程式_______ 。
(4)写出固体 隔绝空气加热分解的化学方程式
隔绝空气加热分解的化学方程式_______ 。
 (由3种元素组成)开展探究实验。
(由3种元素组成)开展探究实验。
其中:
 和
和 均为纯净物;
均为纯净物; 可使品红溶液褪色。请回答:
可使品红溶液褪色。请回答:(1)白色沉淀
 的化学式是
的化学式是(2)组成
 的3种元素是
的3种元素是(3)写出步骤Ⅰ中反应的离子方程式
(4)写出固体
 隔绝空气加热分解的化学方程式
隔绝空气加热分解的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】溶液的配制对生产和科学研究具有重要意义,回答下列问题:
I.某化学实验需要230 mL0.50 mol•L-1的Na2S2O3溶液,某同学在实验室进行配制。
(1)配制的实验步骤如下,请你帮助该同学将实验补充完整:
①用托盘天平准确称取一定质量的Na2S2O3•5H2O(M=248 g•mol-1)固体,放入烧杯,用适量蒸馏水溶解;
②冷却到室温后,将烧杯中的溶液小心地注入容量瓶中;
③用蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤液转入容量瓶中,振荡;
④继续向容量瓶中加水至液面离容量瓶颈部的刻度线_____ cm时,改用_____ 加水至刻度线;
⑤将容量瓶塞盖好,充分摇匀。
(2)配制溶液过程中需称量Na2S2O3•5H2O固体的质量为____ g(保留1位小数)。
(3)配制过程中,进行(1)中步骤②操作时,有少量溶液洒落,则配制的溶液浓度_____ (填“偏高”“偏低”或“无影响”)。
(4)若取配制好的50 mL0.50 mol•L-1Na2S2O3溶液加水稀释到250 mL,则稀释后溶液中Na2S2O3的物质的量为____ mol,物质的量浓度为_____ mol•L-1(保留两位小数)。
II.次氯酸钠溶液是常用的杀菌消毒剂,其制备方法有多种。
(5)NaClO溶液可在低温下将Cl2缓慢通入NaOH溶液中而制得,反应的离子方程式为_____ 。
(6)14.9 g NaClO溶解在水中,要使Na+数目与水分子数目之比为1∶100,则需要水的物质的量为_____ mol。
I.某化学实验需要230 mL0.50 mol•L-1的Na2S2O3溶液,某同学在实验室进行配制。
(1)配制的实验步骤如下,请你帮助该同学将实验补充完整:
①用托盘天平准确称取一定质量的Na2S2O3•5H2O(M=248 g•mol-1)固体,放入烧杯,用适量蒸馏水溶解;
②冷却到室温后,将烧杯中的溶液小心地注入容量瓶中;
③用蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤液转入容量瓶中,振荡;
④继续向容量瓶中加水至液面离容量瓶颈部的刻度线
⑤将容量瓶塞盖好,充分摇匀。
(2)配制溶液过程中需称量Na2S2O3•5H2O固体的质量为
(3)配制过程中,进行(1)中步骤②操作时,有少量溶液洒落,则配制的溶液浓度
(4)若取配制好的50 mL0.50 mol•L-1Na2S2O3溶液加水稀释到250 mL,则稀释后溶液中Na2S2O3的物质的量为
II.次氯酸钠溶液是常用的杀菌消毒剂,其制备方法有多种。
(5)NaClO溶液可在低温下将Cl2缓慢通入NaOH溶液中而制得,反应的离子方程式为
(6)14.9 g NaClO溶解在水中,要使Na+数目与水分子数目之比为1∶100,则需要水的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】有四种元素A、B、C、D,其中B2-离子与C+离子核外都有二个电子层,B原子的质子数与C原子的质子数之和等于D原子的质子数,A原子失去一个电子后变成一个质子,试回答:
(1)A、B、C、D的元素符号分别为_______ 、______ 、_______ 、_______ 。
(2)B2-的电子式为_________ ,D原子的原子结构示意图为__________ ,C+离子的结构示意图为____________ 。
(3)写出与C+具有相同电子数的五种分子(化学式):________ 、______ 、______ 、________ 、_________ 。
(1)A、B、C、D的元素符号分别为
(2)B2-的电子式为
(3)写出与C+具有相同电子数的五种分子(化学式):
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】研究物质的微观结构和元素组成,并用恰当的化学用语进行表达,能帮助我们揭示物质变化的本质,发现物质变化的规律。
(1)下图是部分元素原子或离子的结构示意图.请你仔细观察、分析,用序号填空:
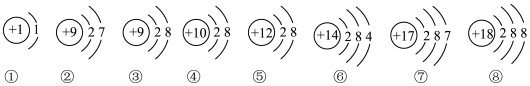
①上述粒子中,属于稀有气体元素的原子是_____________ ;
②在化学反应中容易得到电子的是_____________ ;
③属于正离子的是_____________ ;
④表示 的是
的是_____________ ;
⑤属于同一种元素的是_____________ ;
⑥属于非金属元素的是_____________ ;
⑦电子层数相同、最外层电子数也相同的粒子有_____________ .
(2)卤族元素F和 具有相似的化学性质,其原因是它们的原子具有相同的
具有相似的化学性质,其原因是它们的原子具有相同的
(3)写出铝离子的结构示意图①_____________ ,其核外能量最高的电子层符号为②___________ 。
(4)两种微粒的电子数相同,质子数不同,则它们可能是
①两种不同的原子;②两种不同的离子;③同一种元素的原子和离子;④不同元素的原子和离子
(5)在第n电子层中,当它作为原子的最外电子层时,最多容纳的电子数与 层相同,当它作为原子的次外层时,其电子数比
层相同,当它作为原子的次外层时,其电子数比 层最少能多10个,则此电子层是
层最少能多10个,则此电子层是
(6)一瓶气体经分析只含一种元素,则该气体
(7)下列物质变化过程不会破坏化学键的是
(8)下列关于化学键的说法正确的是
(9) 的电子式是
的电子式是_____________ 。
(10)请用电子式表示 的形成过程
的形成过程_____________ 。
(1)下图是部分元素原子或离子的结构示意图.请你仔细观察、分析,用序号填空:

①上述粒子中,属于稀有气体元素的原子是
②在化学反应中容易得到电子的是
③属于正离子的是
④表示
 的是
的是⑤属于同一种元素的是
⑥属于非金属元素的是
⑦电子层数相同、最外层电子数也相同的粒子有
(2)卤族元素F和
 具有相似的化学性质,其原因是它们的原子具有相同的
具有相似的化学性质,其原因是它们的原子具有相同的 | A.电子层数 | B.核外电子数 | C.最外层电子数 | D.原子半径 |
(3)写出铝离子的结构示意图①
(4)两种微粒的电子数相同,质子数不同,则它们可能是
①两种不同的原子;②两种不同的离子;③同一种元素的原子和离子;④不同元素的原子和离子
| A.①和④ | B.②和③ | C.①和③ | D.②和④ |
(5)在第n电子层中,当它作为原子的最外电子层时,最多容纳的电子数与
 层相同,当它作为原子的次外层时,其电子数比
层相同,当它作为原子的次外层时,其电子数比 层最少能多10个,则此电子层是
层最少能多10个,则此电子层是 | A.K层 | B.M层 | C.L层 | D.N层 |
(6)一瓶气体经分析只含一种元素,则该气体
| A.一定是单质 | B.可能是化合物 |
| C.可能是几种单质的混合物 | D.可能是化合物与单质的混合物 |
(7)下列物质变化过程不会破坏化学键的是
| A.水气化为水蒸气 | B.水蒸气在高温下分解为氢气和氧气 |
| C.氯化钠溶于水 | D.氯化钠熔化 |
(8)下列关于化学键的说法正确的是
| A.破坏化学键会放出能量 | B.所有物质中都存在化学键 |
| C.金属元素和非金属元素间一定形成离子键 | D.离子化合物中不一定含有金属元素 |
(9)
 的电子式是
的电子式是(10)请用电子式表示
 的形成过程
的形成过程
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)相同物质的量的14C18O2与32S16O2的原子数之比为_______ ,中子数之比为_______ ,电子数之比为_______ 。
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为_______ (填代号)。
(3)利用元素周期律可预测陌生元素及物质的性质,已知Rb与Na处于同一主族,下列说法正确的是_______。
(1)相同物质的量的14C18O2与32S16O2的原子数之比为
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为_______ (填代号)。
A. | B.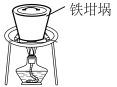 | C.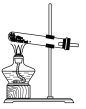 | D.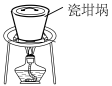 |
| A.失电子能力: Rb>Na |
| B.碱性: NaOH>RbOH |
| C.Rb比Na更易与氧气发生反应 |
| D.Rb不易与水反应放出H2 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】(1)某元素M,其离子M2+,M2+原子核核内有20个中子,核外有18个电子,则M的质子数是__________ ,质量数是_________
(2)根据下列叙述,写出微粒符号和结构示意图。
a.原子核外有2个电子层,核外有10个电子的原子________ 、______________ ;
b.质量数为24,质子数等于中子数的原子_________ 、__________________ ;
c.最外层电子数是次外层电子数的4倍的二价阴离子_________ 、_________________ 。
(3)结构示意图为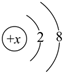 的阳离子,其电子式符号可能为
的阳离子,其电子式符号可能为________ 、________ 、________ 。
(2)根据下列叙述,写出微粒符号和结构示意图。
a.原子核外有2个电子层,核外有10个电子的原子
b.质量数为24,质子数等于中子数的原子
c.最外层电子数是次外层电子数的4倍的二价阴离子
(3)结构示意图为
 的阳离子,其电子式符号可能为
的阳离子,其电子式符号可能为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次递增,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层电子数是次外层电子数的3倍。
(1)试推断它们各是什么元素,写出它们的元素符号:A________ ,B________ ,C________ ,D________ 。
(2)画出D的离子结构示意图________ 。
(3)由这四种元素组成的三核10电子的分子为________ ,四核10电子的分子是________ 。
(1)试推断它们各是什么元素,写出它们的元素符号:A
(2)画出D的离子结构示意图
(3)由这四种元素组成的三核10电子的分子为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE在发光材料,生物医学等领域引起广泛关注。
(1)Se在元素周期表中的位置为______ ,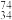 Se和
Se和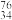 Se互为
Se互为______ ,这两种原子中子数之差的绝对值为_______ 。
(2)H2Se是一种有恶臭的气体,与H2O相比,沸点H2Se_______ H2O(填“>”或“<”,下同),原因是______ ;热稳定性:H2Se_______ H2O。
(3)较高浓度的Na2SeO2能促进细胞DNA的增殖活性,延缓细胞衰老。Na、Se、O形成的简单离子的半径由大到小的顺序为______ (填离子符号)。
(4)一种合成含Se的新型AIE分子的原料结构如图:
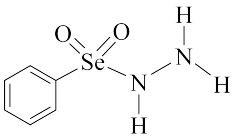
肼(N2H4)的结构与上述分子部分结构十分相似,N2H4的电子式为_______ 。
(1)Se在元素周期表中的位置为
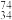 Se和
Se和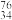 Se互为
Se互为(2)H2Se是一种有恶臭的气体,与H2O相比,沸点H2Se
(3)较高浓度的Na2SeO2能促进细胞DNA的增殖活性,延缓细胞衰老。Na、Se、O形成的简单离子的半径由大到小的顺序为
(4)一种合成含Se的新型AIE分子的原料结构如图:

肼(N2H4)的结构与上述分子部分结构十分相似,N2H4的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】表中为元素周期表的一部分,请回答下列有关问题:
(1)元素②的一种核素可测定文物年代,这种核素的符号为______ ,已知元素⑩的一种核素,其中子数为45,这种核素的符号为______ 。
(2)由元素①和④可形成18电子的化合物,该化合物的化学式为______ 。
(3)图中标出的元素的最高价氧化物对应的水化物中,酸性最强的是______ (用化学式回答),写出该水化物与⑥的最高价氧化物的水化物反应的离子方程式:______ 。
(4)将⑤、⑥、⑨单质各1mol分别投入到足量的同浓度的盐酸中,预测实验结果:______ 与盐酸反应最剧烈,______ 与盐酸反应的速度最慢;______ 与盐酸反应产生的气体最多。(均用元素符号回答)
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(2)由元素①和④可形成18电子的化合物,该化合物的化学式为
(3)图中标出的元素的最高价氧化物对应的水化物中,酸性最强的是
(4)将⑤、⑥、⑨单质各1mol分别投入到足量的同浓度的盐酸中,预测实验结果:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表显示了元素周期表中的一部分。
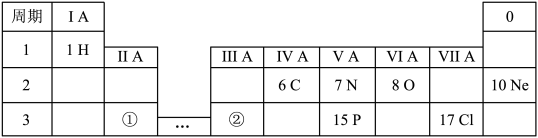
请回答下列问题:
(1)磷元素的原子序数是___________ 。
(2)属于稀有气体的是___________ (选填“ ”或“
”或“ ”)。
”)。
(3)碳元素在元素周期表的第___________ (选填“二”或“三”)周期第___________ (选填“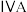 ”或“
”或“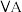 ”)族。
”)族。
(4)红棕色气体 中氮元素的化合价为
中氮元素的化合价为___________ (选填“ ”或“
”或“ ”)价。
”)价。
(5)含有共价键的单质是___________ (选填“ ”或“
”或“ ”)。
”)。
(6)已知同周期元素从左到右金属性逐渐减弱,则元素的金属性强弱:①___________ ②(选填“大于”或“小于”)。
(7)下列化学用语使用正确的是:___________ (填写字母)。
A.中子数为8的碳原子符号为 B.氯化氢的电子式为
B.氯化氢的电子式为

请回答下列问题:
(1)磷元素的原子序数是
(2)属于稀有气体的是
 ”或“
”或“ ”)。
”)。(3)碳元素在元素周期表的第
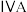 ”或“
”或“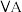 ”)族。
”)族。(4)红棕色气体
 中氮元素的化合价为
中氮元素的化合价为 ”或“
”或“ ”)价。
”)价。(5)含有共价键的单质是
 ”或“
”或“ ”)。
”)。(6)已知同周期元素从左到右金属性逐渐减弱,则元素的金属性强弱:①
(7)下列化学用语使用正确的是:
A.中子数为8的碳原子符号为
 B.氯化氢的电子式为
B.氯化氢的电子式为
您最近一年使用:0次

 价阳离子和氖原子具有相同的电子数。
价阳离子和氖原子具有相同的电子数。

