(1)甲醇是重要的化工原料,又可做燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,主要反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2= -58 kJ/mol
CH3OH(g)+H2O(g) △H2= -58 kJ/mol
③CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
已知反应①中的相关的化学键键能数据如下:
回答下列问题:
①△H3=_____ kJ/mol
②25℃,101 kPa条件下,测得16g甲醇完全燃烧释放出Q kJ的热量,请写出表示甲醇燃烧热的热化学方程式_______________
(2)25℃,将a mol·L-1氨水与b mol·L-1盐酸等体积混合后溶液呈中性,则此时溶液中c(NH4+)__________ c(Cl-)(填“>”、“<”或“﹦”);用含a、b的代数式表示该温度下NH3·H2O的电离平衡常数Kb = _________
(3)800℃时,在2L密闭容器中发生反应2NO(g)+O2(g) 2NO2(g),在反应体系中,n(NO)随时间的变化如下表所示:
2NO2(g),在反应体系中,n(NO)随时间的变化如下表所示:
①下图中表示NO2变化的曲线是___________ 用O2表示从0~2s内该反应的平均速率v=____
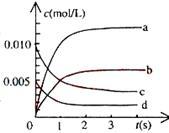
②能说明该反应已经达到平衡状态的是_______
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变
①CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2= -58 kJ/mol
CH3OH(g)+H2O(g) △H2= -58 kJ/mol③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3已知反应①中的相关的化学键键能数据如下:
化学键 | H-H | C-O | C | H-O | C-H |
E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
回答下列问题:
①△H3=
②25℃,101 kPa条件下,测得16g甲醇完全燃烧释放出Q kJ的热量,请写出表示甲醇燃烧热的热化学方程式
(2)25℃,将a mol·L-1氨水与b mol·L-1盐酸等体积混合后溶液呈中性,则此时溶液中c(NH4+)
(3)800℃时,在2L密闭容器中发生反应2NO(g)+O2(g)
 2NO2(g),在反应体系中,n(NO)随时间的变化如下表所示:
2NO2(g),在反应体系中,n(NO)随时间的变化如下表所示:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
①下图中表示NO2变化的曲线是

②能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变
更新时间:2016-12-09 16:02:26
|
【知识点】 反应热
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知1,3-丁二烯与 加成的能量-反应进程图如图所示(图中
加成的能量-反应进程图如图所示(图中 、
、 、
、 表示各步正向反应的焓变)。
表示各步正向反应的焓变)。
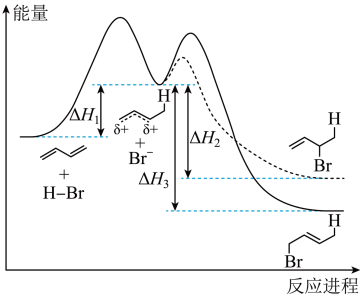
(1)反应时间越长,1,3-丁二烯与 反应得到1,2-加成产物的比例
反应得到1,2-加成产物的比例___________ (填“越大”“越小”“不变”)
(2)该反应中, 与烯烃结合的一步
与烯烃结合的一步___________ 决速步(填“是”或“否”)
(3)1,3-丁二烯与 发生1,2-加成的反应热为
发生1,2-加成的反应热为___________ 。
 加成的能量-反应进程图如图所示(图中
加成的能量-反应进程图如图所示(图中 、
、 、
、 表示各步正向反应的焓变)。
表示各步正向反应的焓变)。
(1)反应时间越长,1,3-丁二烯与
 反应得到1,2-加成产物的比例
反应得到1,2-加成产物的比例(2)该反应中,
 与烯烃结合的一步
与烯烃结合的一步(3)1,3-丁二烯与
 发生1,2-加成的反应热为
发生1,2-加成的反应热为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】汽车尾气主要含有一氧化碳、一氧化氮等物质,是造成城市空气污染的主要因素之一、请回答下列问题。
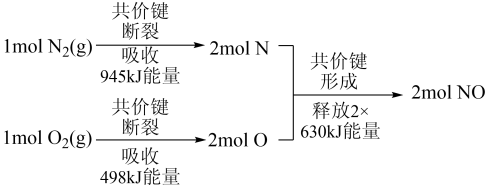
(1)氮气和氧气反应生成一氧化氮的能量变化如图所示,则由该反应生成2molNO时,应_______ (填“释放”或“吸收”)_______ kJ能量。
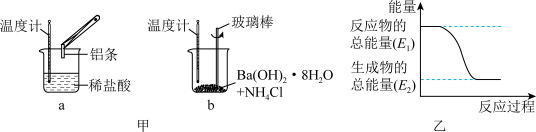
(2)某实验小组进行如图甲所示实验。请判断b中温度_______ (填“升高”或“降低”)。反应过程_______ (填“a”或“b”)的能量变化可用图乙表示。
(1)氮气和氧气反应生成一氧化氮的能量变化如图所示,则由该反应生成2molNO时,应

(2)某实验小组进行如图甲所示实验。请判断b中温度

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
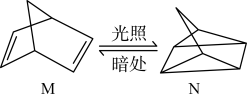
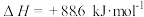
则M、N相比,较稳定的是_______ 。
(2)已知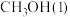 的燃烧热为726.5
的燃烧热为726.5 ,
,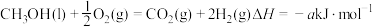 ,则a
,则a_______ 726.5(填“>”、 “<”或“=”)。
(3)使 和
和 通过灼热的炭层,生成
通过灼热的炭层,生成 和
和 ,当有
,当有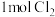 参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
参与反应时释放出145 kJ热量,写出该反应的热化学方程式:_______ 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合,在高温下煅烧,所得物质可作耐高温材料: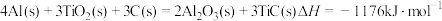 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为_______ 。
(5)已知:①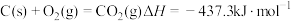
②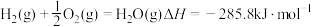
③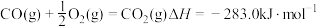
则煤的气化主要反应的热化学方程式是
_______  。
。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:

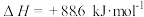
则M、N相比,较稳定的是
(2)已知
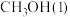 的燃烧热为726.5
的燃烧热为726.5 ,
,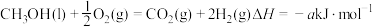 ,则a
,则a(3)使
 和
和 通过灼热的炭层,生成
通过灼热的炭层,生成 和
和 ,当有
,当有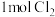 参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
参与反应时释放出145 kJ热量,写出该反应的热化学方程式:(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合,在高温下煅烧,所得物质可作耐高温材料:
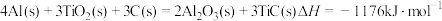 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为(5)已知:①
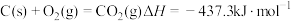
②
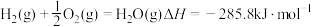
③
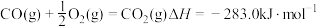
则煤的气化主要反应的热化学方程式是

 。
。
您最近一年使用:0次

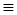 O(CO中的化学键)
O(CO中的化学键)

