碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
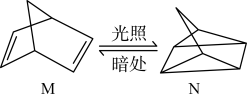
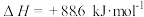
则M、N相比,较稳定的是_______ 。
(2)已知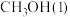 的燃烧热为726.5
的燃烧热为726.5 ,
,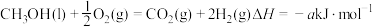 ,则a
,则a_______ 726.5(填“>”、 “<”或“=”)。
(3)使 和
和 通过灼热的炭层,生成
通过灼热的炭层,生成 和
和 ,当有
,当有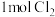 参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
参与反应时释放出145 kJ热量,写出该反应的热化学方程式:_______ 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合,在高温下煅烧,所得物质可作耐高温材料: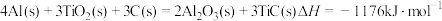 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为_______ 。
(5)已知:①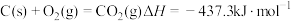
②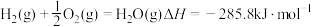
③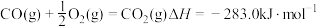
则煤的气化主要反应的热化学方程式是
_______  。
。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:

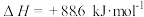
则M、N相比,较稳定的是
(2)已知
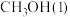 的燃烧热为726.5
的燃烧热为726.5 ,
,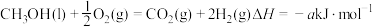 ,则a
,则a(3)使
 和
和 通过灼热的炭层,生成
通过灼热的炭层,生成 和
和 ,当有
,当有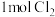 参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
参与反应时释放出145 kJ热量,写出该反应的热化学方程式:(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合,在高温下煅烧,所得物质可作耐高温材料:
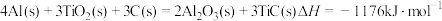 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为(5)已知:①
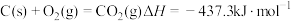
②
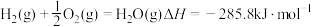
③
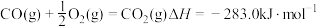
则煤的气化主要反应的热化学方程式是

 。
。
更新时间:2023/02/03 17:23:08
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】一种新型煤气化燃烧集成制氢发生的主要反应如下:
Ⅰ.

Ⅱ.

Ⅲ.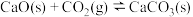

Ⅳ.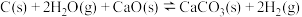
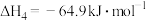
副反应:
Ⅴ.
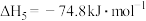
Ⅵ.
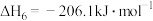
回答下列问题:
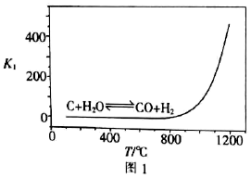
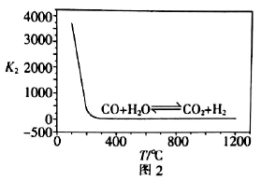
(1)已知反应Ⅰ、Ⅱ的平衡常数 、
、 随温度的变化如图1、图2所示。
随温度的变化如图1、图2所示。
①由反应Ⅴ和反应Ⅵ可知,
___________ ;反应Ⅰ的
___________ (填“ ”或“
”或“ ”)0。
”)0。
②温度小于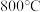 时,
时, ,原因是
,原因是___________ 。
③为提高反应Ⅱ中 的转化率,可采取的措施是
的转化率,可采取的措施是___________ (写一条)
④ 时,向密闭容器中充入
时,向密闭容器中充入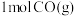 和
和 ,只发生反应Ⅱ,此时该反应的平衡常数
,只发生反应Ⅱ,此时该反应的平衡常数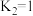 ,
, 的平衡转化率为
的平衡转化率为___________ 。
(2)从环境保护角度分析,该制氢工艺中设计反应Ⅲ的优点是___________ 。
(3)起始时在气化炉中加入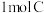 、
、 及
及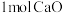 ,在
,在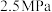 下,气体的组成与温度的关系如图3所示。
下,气体的组成与温度的关系如图3所示。
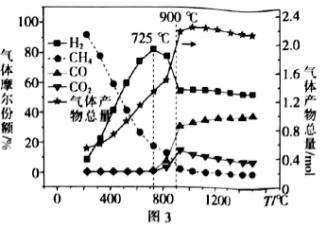
①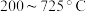 时,
时, 的量不断减少的原因是
的量不断减少的原因是___________ 。
②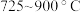 时,
时, 的物质的量分数快速减小,其原因是
的物质的量分数快速减小,其原因是___________ 。
③制氢生产中控制温度为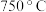 左右,不采用
左右,不采用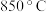 以上温度的原因是
以上温度的原因是___________ 。
Ⅰ.


Ⅱ.


Ⅲ.
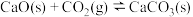

Ⅳ.
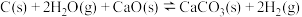
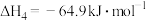
副反应:
Ⅴ.

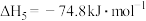
Ⅵ.

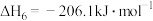
回答下列问题:
(1)已知反应Ⅰ、Ⅱ的平衡常数
 、
、 随温度的变化如图1、图2所示。
随温度的变化如图1、图2所示。

①由反应Ⅴ和反应Ⅵ可知,


 ”或“
”或“ ”)0。
”)0。②温度小于
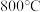 时,
时, ,原因是
,原因是③为提高反应Ⅱ中
 的转化率,可采取的措施是
的转化率,可采取的措施是④
 时,向密闭容器中充入
时,向密闭容器中充入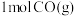 和
和 ,只发生反应Ⅱ,此时该反应的平衡常数
,只发生反应Ⅱ,此时该反应的平衡常数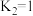 ,
, 的平衡转化率为
的平衡转化率为(2)从环境保护角度分析,该制氢工艺中设计反应Ⅲ的优点是
(3)起始时在气化炉中加入
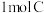 、
、 及
及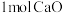 ,在
,在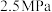 下,气体的组成与温度的关系如图3所示。
下,气体的组成与温度的关系如图3所示。
①
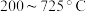 时,
时, 的量不断减少的原因是
的量不断减少的原因是②
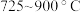 时,
时, 的物质的量分数快速减小,其原因是
的物质的量分数快速减小,其原因是③制氢生产中控制温度为
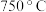 左右,不采用
左右,不采用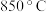 以上温度的原因是
以上温度的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.请写出下列反应的离子方程式:
(1)往 溶液中滴加浓烧碱并加热:
溶液中滴加浓烧碱并加热:___________ 。
(2)往 溶液中滴加稀盐酸溶液:
溶液中滴加稀盐酸溶液:___________ 。
(3)将 气体与
气体与 充分发生反应:
充分发生反应:___________ 。
(4) 溶液中通入少量
溶液中通入少量 气体:
气体:___________ 。
(5)往 溶液中通入少量
溶液中通入少量 :
:___________ 。
Ⅱ.请按要求完成下列热化学知识小题(能量数据均为常温常压下的测定值):
(6)将 氢气与足量氧气充分反应生成液态水,放出
氢气与足量氧气充分反应生成液态水,放出 的热量。则表示氢气燃烧热的热化学方程式为:
的热量。则表示氢气燃烧热的热化学方程式为:___________ 。
(7)将含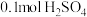 的稀硫酸溶液与足量稀
的稀硫酸溶液与足量稀 溶液迅速反应,测得放出
溶液迅速反应,测得放出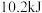 的热量。则表示该反应的热化学方程式为:
的热量。则表示该反应的热化学方程式为:___________ 。
(8)已知反应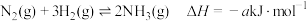 ;
; 、
、 键能分别为
键能分别为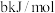 、
、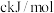 ,则
,则 的键能为
的键能为___________  (用含a、b、c的式子表示)。
(用含a、b、c的式子表示)。
(9)已知:
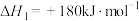

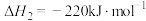
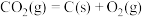
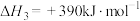
则反应 的
的
___________  。
。
(1)往
 溶液中滴加浓烧碱并加热:
溶液中滴加浓烧碱并加热:(2)往
 溶液中滴加稀盐酸溶液:
溶液中滴加稀盐酸溶液:(3)将
 气体与
气体与 充分发生反应:
充分发生反应:(4)
 溶液中通入少量
溶液中通入少量 气体:
气体:(5)往
 溶液中通入少量
溶液中通入少量 :
:Ⅱ.请按要求完成下列热化学知识小题(能量数据均为常温常压下的测定值):
(6)将
 氢气与足量氧气充分反应生成液态水,放出
氢气与足量氧气充分反应生成液态水,放出 的热量。则表示氢气燃烧热的热化学方程式为:
的热量。则表示氢气燃烧热的热化学方程式为:(7)将含
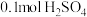 的稀硫酸溶液与足量稀
的稀硫酸溶液与足量稀 溶液迅速反应,测得放出
溶液迅速反应,测得放出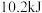 的热量。则表示该反应的热化学方程式为:
的热量。则表示该反应的热化学方程式为:(8)已知反应
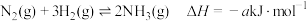 ;
; 、
、 键能分别为
键能分别为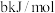 、
、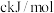 ,则
,则 的键能为
的键能为 (用含a、b、c的式子表示)。
(用含a、b、c的式子表示)。(9)已知:

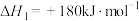

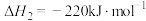
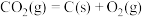
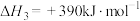
则反应
 的
的
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知部分物质的摩尔燃烧焓(298K,101kPa)如表所示,按要求填空。
(1)写出表示葡萄糖燃烧热的热化学方程式:___________ 。
(2) 的
的
___________ kJ⋅mol-1。
(3)乙烷和辛烷的关系是互为___________ (填“同素异形体”“同系物”或“同分异构体”)。
(4)写出一种鉴别乙醇溶液和葡萄糖溶液的方法:___________ 。
(5)乙醇汽油为添加了10%(乙醇的体积分数)乙醇的汽油,假设乙醇汽油中只含有乙醇和异辛烷两种物质,乙醇的密度约为0.80g⋅mL-1,异辛烷的密度约为0.70g⋅mL-1。___________ ,1L此种乙醇汽油完全燃烧生成 和
和 时放出的热量约为
时放出的热量约为___________ kJ(保留到小数点后1位)。
| 名称 | 氢气 | 乙烯 | 乙烷 | 葡萄糖 | 乙醇 | 辛烷 |
| 化学式 |  |  |  |  |  | 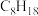 |
 /(kJ·mol⁻¹) /(kJ·mol⁻¹) | -285.8 | -1411.0 | -1599.8 | -2800 | -1366.8 | -5443.0 |
(2)
 的
的
(3)乙烷和辛烷的关系是互为
(4)写出一种鉴别乙醇溶液和葡萄糖溶液的方法:
(5)乙醇汽油为添加了10%(乙醇的体积分数)乙醇的汽油,假设乙醇汽油中只含有乙醇和异辛烷两种物质,乙醇的密度约为0.80g⋅mL-1,异辛烷的密度约为0.70g⋅mL-1。
①异辛烷的结构简式为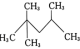 ,其用系统命名法命名为
,其用系统命名法命名为
 和
和 时放出的热量约为
时放出的热量约为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列问题。
(1)如图 和CO(g)反应生成
和CO(g)反应生成 和NO(g)过程中能量变化图,该反应物的总焓
和NO(g)过程中能量变化图,该反应物的总焓___________ 生成物的焓(填“小于”或“大于”)。请写出 和CO反应的热化学方程式
和CO反应的热化学方程式___________ ;

(2)有如下三个热化学方程式:
 △H1=akJ/mol
△H1=akJ/mol
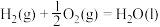 △H2=bkJ/mol
△H2=bkJ/mol
 △H3=ckJ/mol
△H3=ckJ/mol
①请写出b、c的关系式___________ ;判断c___________ 0(填“>”或“<”)。
②试比较
___________  (填“>”或“<”)。
(填“>”或“<”)。
(1)如图
 和CO(g)反应生成
和CO(g)反应生成 和NO(g)过程中能量变化图,该反应物的总焓
和NO(g)过程中能量变化图,该反应物的总焓 和CO反应的热化学方程式
和CO反应的热化学方程式
(2)有如下三个热化学方程式:
 △H1=akJ/mol
△H1=akJ/mol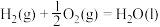 △H2=bkJ/mol
△H2=bkJ/mol △H3=ckJ/mol
△H3=ckJ/mol①请写出b、c的关系式
②试比较

 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知下列反应的能量变化示意图。
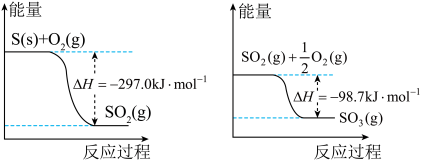
(1)1molS(g)与O2(g)完全反应生成SO2(g),反应的ΔH___ -297.0kJ·mol-1(填“>”或“<”)
(2)写出S(s)与O2(g)反应生成SO3(g)的热化学方程式___ 。

(1)1molS(g)与O2(g)完全反应生成SO2(g),反应的ΔH
(2)写出S(s)与O2(g)反应生成SO3(g)的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电高效燃料电池,充一次电可连续使用一个月。如图是一个电化学过程的示意图。

请填空:
(1)充电时:原电池的负极与电源______ 极相连。B极的电极反应式为_______ 。
(2)放电时,负极的电极反应式为_______ 。
(3)在此过程中若完全反应,乙池中A极的质量升高648 g,则甲池中理论上消耗O2______ L(标准状况下)。
(4)若在常温常压下,1g CH3OH燃烧生成CO2和液态H2O时放出热量22.68 kJ,则表示该反应的热化学方程式为_______

请填空:
(1)充电时:原电池的负极与电源
(2)放电时,负极的电极反应式为
(3)在此过程中若完全反应,乙池中A极的质量升高648 g,则甲池中理论上消耗O2
(4)若在常温常压下,1g CH3OH燃烧生成CO2和液态H2O时放出热量22.68 kJ,则表示该反应的热化学方程式为
您最近一年使用:0次



