下列关于化学键的说法正确的是
| A.离子化合物中一定存在离子键,可能存在共价键 |
| B.由金属元素和非金属元素组的化学键一定是离子键 |
| C.非极性键只存在于双原子单质分子中 |
| D.NH4Cl是一种共价化合物 |
更新时间:2016-07-15 16:12:24
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法中正确的是
①离子化合物中一定有离子键,可能有共价键
②离子化合物熔融状态下都可以导电
③非金属单质中不含离子键,一定只含有共价键
④稳定性:CH4>SiH4,沸点:CH4>SiH4
⑤NaCl 和 HCl 溶于水破坏相同的作用力
⑥非极性键可能存在于非金属单质中,也可能存在于离子化合物或共价化合物中
①离子化合物中一定有离子键,可能有共价键
②离子化合物熔融状态下都可以导电
③非金属单质中不含离子键,一定只含有共价键
④稳定性:CH4>SiH4,沸点:CH4>SiH4
⑤NaCl 和 HCl 溶于水破坏相同的作用力
⑥非极性键可能存在于非金属单质中,也可能存在于离子化合物或共价化合物中
| A.①②⑥ | B.①③④⑥ | C.③④⑤⑥ | D.①④⑤ |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列反应过程中,同时有离子键和共价键的断裂和形成的是
| A.3NO2+H2O==2HNO3+NO |
| B.2Na2O2+2H2O==4NaOH+O2↑ |
| C.8NH3+3Cl2==6NH4Cl+N2 |
| D.2NH3+CO2+H2O==(NH4)2CO3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法不正确的是( )
| A.区别离子化合物和共价化合物的方法是看其熔融状态下是否能够导电 |
| B.含有π键的化合物与只含σ键的化合物的化学性质不同 |
| C.N的电子排布式写成1s22s22px22py1,它违背了泡利原理 |
| D.金属钠的晶体采用体心立方堆积,每个晶胞含2个原子,配位数为8 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】前三周期主族元素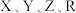 的原子序数依次增大,
的原子序数依次增大, 是地壳中含量最高的元素,
是地壳中含量最高的元素, 的氢化物常用于标记玻璃容器,
的氢化物常用于标记玻璃容器, 的最外层电子数为
的最外层电子数为 的最外层电子数的三倍
的最外层电子数的三倍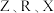 的最外层电子数呈等差数列。下列叙述错误的是
的最外层电子数呈等差数列。下列叙述错误的是
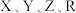 的原子序数依次增大,
的原子序数依次增大, 是地壳中含量最高的元素,
是地壳中含量最高的元素, 的氢化物常用于标记玻璃容器,
的氢化物常用于标记玻璃容器, 的最外层电子数为
的最外层电子数为 的最外层电子数的三倍
的最外层电子数的三倍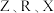 的最外层电子数呈等差数列。下列叙述错误的是
的最外层电子数呈等差数列。下列叙述错误的是A.原子半径: | B.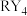 分子具有正四面体结构 分子具有正四面体结构 |
C.与氢形成的共价键键能: | D.Z与Y形成的化合物为离子化合物 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列物质中,含有离子键的是
| A.CO2 | B.HCl | C.H2SO4 | D.NH4Cl |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列物质中,不是离子化合物的是
| A.HCl | B.NaOH | C.NH4Cl | D.Na2CO3 |
您最近一年使用:0次




