一定条件下,对于可逆反应X(g)+3Y(g)  2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.06 mol·L-1,则下列判断正确的是
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.06 mol·L-1,则下列判断正确的是
 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.06 mol·L-1,则下列判断正确的是
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.06 mol·L-1,则下列判断正确的是| A.c1∶c2=3∶1 |
| B.X、Y的转化率不相等 |
| C.c 1的取值范围为0 mol·L-1<c1<0.14 mol·L-1 |
| D.平衡时,Y和Z的生成速率之比为3∶2 |
更新时间:2016-07-22 17:58:06
|
【知识点】 化学平衡
相似题推荐
单选题
|
适中
(0.65)
【推荐1】对于反应2NO(g)+O2(g)=2NO2(g) ΔH=-116.4 kJ·mol-1,下列说法正确的是
| A.该反应能够自发的原因是ΔS > 0 |
| B.工业上使用合适的催化剂可提高NO2的生产效率 |
| C.升高温度,该反应v(逆)增大,v(正)减小,平衡向逆反应方向移动 |
| D.2 mol NO(g)和1 mol O2(g)中所含化学键能总和比2 mol NO2(g)中大116.4 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在起始温度均为T℃、容积均为1L的密闭容器X(恒温)、Y(绝热)中均加入0.1molA和0.4molB,发生反应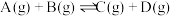 △H<0,X、Y容器中A的转化率随时间的变化关系如图所示。下列说法不正确的是
△H<0,X、Y容器中A的转化率随时间的变化关系如图所示。下列说法不正确的是

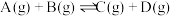 △H<0,X、Y容器中A的转化率随时间的变化关系如图所示。下列说法不正确的是
△H<0,X、Y容器中A的转化率随时间的变化关系如图所示。下列说法不正确的是
| A.曲线M表示容器Y中A的转化率变化 |
B.容器Y在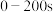 内的化学反应速率为 内的化学反应速率为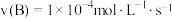 |
C.P点与Q点平衡常数: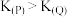 |
D.T℃时,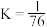 |
您最近一年使用:0次

 可将有机氯化工业的副产品
可将有机氯化工业的副产品 转化为
转化为 。在0.2
。在0.2 、反应物起始物质的量比
、反应物起始物质的量比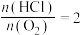 条件下,不同温度时
条件下,不同温度时 ,能增大反应速率。已知反应II:
,能增大反应速率。已知反应II: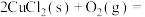
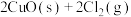
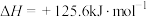 ;反应III:
;反应III:
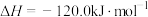 。下列说法正确的是
。下列说法正确的是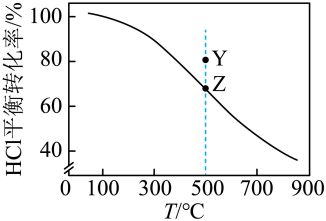
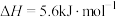
 ,可使Z点移动到Y点
,可使Z点移动到Y点

