下面六个图中,横坐标为某溶液中加入某物质的量,纵坐标为生成沉淀的量。从A—F中选择符合表中各题要求的序号填入表中:


| 溶 液 | 加入的物质 | 答案序号 |
| ⑴饱和石灰水 | CO2 | |
| ⑵AlCl3溶液 | 过量NH3 | |
| ⑶含少量NaOH的NaAlO2 | 过量CO2 | |
| ⑷含少量NaOH的NaAlO2 | 逐滴加稀盐酸 | |
| ⑸MgCl2、AlCl3混合液 | 逐滴加NaOH至过量 | |
| ⑹NaOH溶液 | 逐滴加AlCl3至过量 |
16-17高三上·陕西西安·阶段练习 查看更多[2]
更新时间:2016-12-09 17:01:50
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】以橄榄石(主要成分是Mg9FeSi5O20)等为原料生产硅胶、碱式碳酸镁[Mg2(OH)2CO3]的部分工艺流程如下图所示:
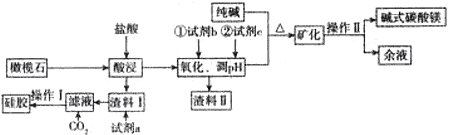
(1)Mg9FeSi5O20中铁元素的化合价为 ,为提高镁的浸出率,可采用的两种主要措施是 渣料II的成分是 。
(2)若试剂b是氯碱工业中的某种气体产物,写出加入b后反应的离子方程式 。试剂c的用途是调节溶液的pH,比较恰当的物质是 (写化学式,后同),余液中溶质的主要成分是 。
(3)操作I的名称是 ,写出生成碱式碳酸镁(同时有气体生成)的离子方程式 。

(1)Mg9FeSi5O20中铁元素的化合价为 ,为提高镁的浸出率,可采用的两种主要措施是 渣料II的成分是 。
(2)若试剂b是氯碱工业中的某种气体产物,写出加入b后反应的离子方程式 。试剂c的用途是调节溶液的pH,比较恰当的物质是 (写化学式,后同),余液中溶质的主要成分是 。
(3)操作I的名称是 ,写出生成碱式碳酸镁(同时有气体生成)的离子方程式 。
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】下图为实验室某浓盐酸试剂瓶标签上的有关信息,试根据标签上的有关数据,回答下列问题(一)(二):(计算结果保留一位小数)

(一).(1)浓盐酸中HCl的物质的量浓度为________ mol·L-1。
(2) 量取________ mL浓盐酸加水稀释就得到500 mL、0.4mol·L-1的稀盐酸。
(二).取该浓盐酸10g与某MgCl2溶液90g混合,向混合溶液中逐滴加入10%的NaOH溶液,生成的沉淀的质量与加入的NaOH溶液质量关系如下图所示。

回答下列问题
(1)A点溶液的溶质化学式为_______________ 。
(2)与MgCl2反应的溶质氢氧化钠的质量为__________ g。
(3)恰好沉淀完全时,C点所得溶液中溶质的质量分数为______________________ 。

(一).(1)浓盐酸中HCl的物质的量浓度为
(2) 量取
(二).取该浓盐酸10g与某MgCl2溶液90g混合,向混合溶液中逐滴加入10%的NaOH溶液,生成的沉淀的质量与加入的NaOH溶液质量关系如下图所示。

回答下列问题
(1)A点溶液的溶质化学式为
(2)与MgCl2反应的溶质氢氧化钠的质量为
(3)恰好沉淀完全时,C点所得溶液中溶质的质量分数为
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐3】镁铝碱式酸盐[MgaAlb(OH)c(CO3)d·xH2O]阻燃剂具有阻燃、消烟、填充等功能,是一种不溶于水的新型无机阻燃剂。
(1)将MgaAlb(OH)c(CO3)d·xH2O表示成氧化物形式______________ 。
(2)为确定镁铝碱式碳酸盐的组成,进行如下实验:准确称取15.050g样品进行灼烧至恒重,生成CO20.560L(已换算成标准状况下)。分析测得残留物中MgO为6.000g,Al2O3为2.550g,通过计算确定该镁铝碱式碳酸盐的化学式________ 。(写出计算过程)
(3)该镁铝碱式碳酸盐可以由MgCl2、NaAlO2、NaOH和Na2CO3反应制备,制备的化学方程式为__________ 。
(1)将MgaAlb(OH)c(CO3)d·xH2O表示成氧化物形式
(2)为确定镁铝碱式碳酸盐的组成,进行如下实验:准确称取15.050g样品进行灼烧至恒重,生成CO20.560L(已换算成标准状况下)。分析测得残留物中MgO为6.000g,Al2O3为2.550g,通过计算确定该镁铝碱式碳酸盐的化学式
(3)该镁铝碱式碳酸盐可以由MgCl2、NaAlO2、NaOH和Na2CO3反应制备,制备的化学方程式为
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】(1)下列各组反应若产生等物质的量的氮氧化物,转移电子数多少的关系正确的是( )
①NO2和H2O ②氧化炉中NH3和O2 ③Fe和HNO3(稀) ④碳和浓HNO3
A.④>②>①>③ B.②>④>③>① C.②>③>①>④ D.②>①>③>④
(2)往Al与NaOH溶液反应后的溶液中滴入NaHCO3溶液,产生白色沉淀,写出离子方程式_____ 。
(3)氰化钠(NaCN)是剧毒化学品。氰化钠泄漏到水体中,可用ClO2处理,生成两种无色无味无毒的气体。写出用ClO2处理氰化钠废水的离子方程式_____ 。
(4)同样浓度下,醋酸和氨水的电离程度相同,但氢氧化铝可以完全溶于醋酸,却不能溶于氨水,问这能说明氢氧化铝的什么性质?_________ 。
(5)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是_____________ 。
①NO2和H2O ②氧化炉中NH3和O2 ③Fe和HNO3(稀) ④碳和浓HNO3
A.④>②>①>③ B.②>④>③>① C.②>③>①>④ D.②>①>③>④
(2)往Al与NaOH溶液反应后的溶液中滴入NaHCO3溶液,产生白色沉淀,写出离子方程式
(3)氰化钠(NaCN)是剧毒化学品。氰化钠泄漏到水体中,可用ClO2处理,生成两种无色无味无毒的气体。写出用ClO2处理氰化钠废水的离子方程式
(4)同样浓度下,醋酸和氨水的电离程度相同,但氢氧化铝可以完全溶于醋酸,却不能溶于氨水,问这能说明氢氧化铝的什么性质?
(5)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图。
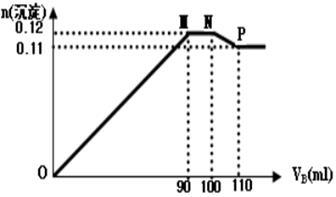
(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)____________________
(2)从90 mL至100 mL之间加入10 mL B溶液时发生的离子反应方程式①_________________ ;②________________ ;并由此可以分析出溶液B中Na2SO4与NaOH物质的量浓度之比为________________ 。
(3)通过计算分析可知:
B溶液中NaOH物质的量浓度为_____________ mol/L;
A溶液中FeCl3物质的量浓度为______________ mol/L。

(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)
(2)从90 mL至100 mL之间加入10 mL B溶液时发生的离子反应方程式①
(3)通过计算分析可知:
B溶液中NaOH物质的量浓度为
A溶液中FeCl3物质的量浓度为
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐3】现有一定量铝粉和铁粉的混合物与一定体积稀硝酸充分反应,反应过程中无气体放出(硝酸的还原产物是NH4NO3)。在反应结束后的溶液中,逐滴加入2mol∙L-1的NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量的关系如图所示。
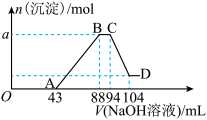
(1)写出OA段反应的离子方程式:____________________________ 。
(2)B点时溶液中含有溶质的化学式为____________ 。
(3)a的数值为__________ 。
(4)原硝酸溶液中HNO3的物质的量为__________ mol。

(1)写出OA段反应的离子方程式:
(2)B点时溶液中含有溶质的化学式为
(3)a的数值为
(4)原硝酸溶液中HNO3的物质的量为
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】向100 mL BaCl2、AlCl3、FeCl3的混合溶液A中逐滴加入Na2SO4和NaOH的混合溶液B,产生沉淀的物质的量n和加入溶液B的体积关系如下图所示:
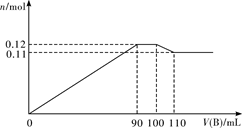
(1)当加入110 mL B溶液时,溶液中的沉淀是___________ (填化学式)。
(2)溶液B中Na2SO4和NaOH的物质的量浓度之比是___________ 。当B溶液加到90 mL~100 mL这一段时间中,所发生的离子反应方程式是____________________ 。
(3)将A、B溶液中各溶质的物质的量浓度(c)填入下表中。

(1)当加入110 mL B溶液时,溶液中的沉淀是
(2)溶液B中Na2SO4和NaOH的物质的量浓度之比是
(3)将A、B溶液中各溶质的物质的量浓度(c)填入下表中。
| 溶质 | Na2SO4 | NaOH | BaCl2 | AlCl3 | FeCl3 |
| c/mol·L-1 |
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图。

(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)____________________
(2)从90 mL至100 mL之间加入10 mL B溶液时发生的离子反应方程式①_________________ ;②________________ ;并由此可以分析出溶液B中Na2SO4与NaOH物质的量浓度之比为________________ 。
(3)通过计算分析可知:
B溶液中NaOH物质的量浓度为_____________ mol/L;
A溶液中FeCl3物质的量浓度为______________ mol/L。

(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)
(2)从90 mL至100 mL之间加入10 mL B溶液时发生的离子反应方程式①
(3)通过计算分析可知:
B溶液中NaOH物质的量浓度为
A溶液中FeCl3物质的量浓度为
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】根据所学知识回答下列问题:
(1)A 与NaOH 溶液反应,有如下转化关系(若产物中有水生成则省略,未表示出来)。
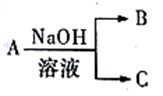
①若A 为常见金属单质,C 为气体,写出向B溶液中通入过量CO2 反应的离子方程式:_______________ ;
②若A 为空气的成分之一,能造成温室效应,当向100 mL1mol/L NaOH 溶液中通入1.344 L 气体(标准状况下)充分反应后,生成B和C 的物质的量之比为______ (B的摩尔质量大于C);
③若A 为AlCl3,写出A 与NaOH 按物质的量之比3 :10 混合时发生反应的离子方程式:______________ 。
(2)氯化铁溶液可用于腐蚀印刷铜电路板,请写出相关的离子方程式:______________ ,如何检验溶液中的铁离子已经完全反应: ______________ 。
(3)现有AlCl3 和FeCl3 混合溶液,其中A13+ 和Fe3+ 的物质的量之和为0.1mol,向此溶液中加入80 mL浓度为4mol/L 的NaOH 溶液,使其充分反应,设原混合溶液中A13+ 的物质的量与A13+ 和Fe3+ 的总物质的量的比值为x。当最终生成的沉淀中只有Fe(OH)3时,x 的取值范围是______ ,请在图中画出沉淀总量(mol)随x(0→1.0)变化的曲线:______________

(1)A 与NaOH 溶液反应,有如下转化关系(若产物中有水生成则省略,未表示出来)。

①若A 为常见金属单质,C 为气体,写出向B溶液中通入过量CO2 反应的离子方程式:
②若A 为空气的成分之一,能造成温室效应,当向100 mL1mol/L NaOH 溶液中通入1.344 L 气体(标准状况下)充分反应后,生成B和C 的物质的量之比为
③若A 为AlCl3,写出A 与NaOH 按物质的量之比3 :10 混合时发生反应的离子方程式:
(2)氯化铁溶液可用于腐蚀印刷铜电路板,请写出相关的离子方程式:
(3)现有AlCl3 和FeCl3 混合溶液,其中A13+ 和Fe3+ 的物质的量之和为0.1mol,向此溶液中加入80 mL浓度为4mol/L 的NaOH 溶液,使其充分反应,设原混合溶液中A13+ 的物质的量与A13+ 和Fe3+ 的总物质的量的比值为x。当最终生成的沉淀中只有Fe(OH)3时,x 的取值范围是

您最近半年使用:0次



