短周期元素W、X、Y、Z、M原子序数依次增大,元素W的一种核素的中子数为0,X的原子最外层电子数是次外层的2倍,Z与M同主族,Z2-电子层结构与氖原子相同。
(1)M在元素周期表中的位置是__________________________ 。
(2)化合物p由W、X、Y、M四种元素组成。已知向p溶液中加入FeCl3溶液,溶液变血红色;向p溶液中加入NaOH溶液并加热可放出使湿润的红色石蕊试纸变蓝的气体。p的化学式为_____________ 。
(3)由X、Y、Z三种元素可组成摩尔质量为84g·mol-1的物质q,且q分子中三种元素的原子个数之比为1:1:1。已知q分子中各原子均达到8电子稳定结构,且分子中不含双键,但含极性键和非极性键,q分子的结构式为_____________________ 。
(4)(XY)2的性质与Cl2相似,(XY)2与NaOH溶液常温下反应的离子方程式为________ 。
(5)常温下,1molZ3能与Y的最简单氢化物反应,生成一种常见的盐和1molZ2,该反应的化学方程式为____________________________________________ 。
(1)M在元素周期表中的位置是
(2)化合物p由W、X、Y、M四种元素组成。已知向p溶液中加入FeCl3溶液,溶液变血红色;向p溶液中加入NaOH溶液并加热可放出使湿润的红色石蕊试纸变蓝的气体。p的化学式为
(3)由X、Y、Z三种元素可组成摩尔质量为84g·mol-1的物质q,且q分子中三种元素的原子个数之比为1:1:1。已知q分子中各原子均达到8电子稳定结构,且分子中不含双键,但含极性键和非极性键,q分子的结构式为
(4)(XY)2的性质与Cl2相似,(XY)2与NaOH溶液常温下反应的离子方程式为
(5)常温下,1molZ3能与Y的最简单氢化物反应,生成一种常见的盐和1molZ2,该反应的化学方程式为
更新时间:2016-12-09 17:07:22
|
相似题推荐
【推荐1】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:A元素基态原子的价电子排布式为nsnnpn,B元素基态原子中的未成对电子数是同周期中最多的,C元素原子最外层电子数是电子层数的3倍,D元素原子半径是第三周期元素中最大的,E元素价电子层中的未成对电子数为4。请回答下列问题:
(1)写出C元素基态原子的电子排布式:__ ,E2+价电子的轨道表示式:__ ,AC两元素形成的原子个数比为1:1的化合物的电子式__ ,B单质的结构式__ 。
(2)CD两元素形成的原子个数比为1:1的化合物的电子式__ ,该化合物中存在的化学键类型有___ 。
(3)这5种元素中电负性最大的元素是__ (填元素符号),A、B、C三种元素的第一电离能由大到小的顺序为__ (填元素符号)。A、B、C三种元素的氢化物的稳定性由大到小的顺序为__ (用化学式表示)。
(1)写出C元素基态原子的电子排布式:
(2)CD两元素形成的原子个数比为1:1的化合物的电子式
(3)这5种元素中电负性最大的元素是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)__________ 。
(2)X与Y能形成多种化合物,其中相对分了质量是26的分子中,结构式:_______ 。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:
 (在水溶液中进行)
(在水溶液中进行)
其中,C是溶于水显酸性的气体;D是淡黄色固体。写出D的电子式:______ 。
①如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式为______ 。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性,由A转化为B的离子方程式为_______ 。
(1)五种元素原子半径由大到小的顺序是(写元素符号)
(2)X与Y能形成多种化合物,其中相对分了质量是26的分子中,结构式:
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:
 (在水溶液中进行)
(在水溶液中进行)其中,C是溶于水显酸性的气体;D是淡黄色固体。写出D的电子式:
①如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式为
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性,由A转化为B的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如图是元素周期表的一部分,回答下列问题:

(1)元素④⑦⑧形成的简单离子,其离子半径由小到大的顺序为___________ (用离子符号表示)。
(2)推测⑤不可能具有的性质是___________(填字母)。
(3)用电子式表示①与③形成18e-化合物的电子式___________ 。
(4)由②、⑨组成的化合物分子中,②、⑨原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物和一种碱性气体,写出该反应的化学方程式:___________ 。
(5)在含有①、⑥、⑦简单阳离子的100mL溶液中,逐滴滴加5mol/L的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:

①沉淀减少时发生的离子方程式:___________ 。
②a点的数值为:___________ mL。

(1)元素④⑦⑧形成的简单离子,其离子半径由小到大的顺序为
(2)推测⑤不可能具有的性质是___________(填字母)。
A.最高正化合价为 |
B.气态氢化物稳定性比 弱 弱 |
| C.最高价氧化物对应水化物的酸性比硝酸强 |
| D.单质在常温下可与氢气化合 |
(4)由②、⑨组成的化合物分子中,②、⑨原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物和一种碱性气体,写出该反应的化学方程式:
(5)在含有①、⑥、⑦简单阳离子的100mL溶液中,逐滴滴加5mol/L的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:

①沉淀减少时发生的离子方程式:
②a点的数值为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】臭氧是一种强氧化剂可与碘化钾水溶液发生反应生成氧气和单质碘。向反应后的溶液中滴入酚酞,溶液变为红色。
(1)试写出该反应的化学方程式(Ⅰ):_____ 。
(2)该反应体系中还伴随着化学反应(Ⅱ):I2(aq) + I-(aq) I3-(aq)。反应Ⅱ的平衡常数表达式为:
I3-(aq)。反应Ⅱ的平衡常数表达式为:____ 。
(3)根据如图,计算反应Ⅱ中3-18s内用I2表示的反应速率为_____ 。

(4)为探究Fe2+对上述O3氧化I-反应的影响,将O3通入含Fe2+和I-的混合溶液中。试预测因Fe2+的存在可能引发的化学反应(请用文字描述,如:“碘离子被臭氧氧化为碘单质”)①______ 。② _____ ;该反应的过程能显著降低溶液的pH,并提高反应(Ⅰ)中Ⅰ-的转化率,原因是:____ 。
(5)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢铁中的硫转化为H2SO3,然后以淀粉为指示剂,用一定浓度的I2溶液进行滴定。综合上述各步反应及已有知识,可推知氧化性强弱关系正确的是____ (填序号)。
a. Fe3+> I2 b. O3> Fe3+ c. I2> O2 d. I2>SO42-
(1)试写出该反应的化学方程式(Ⅰ):
(2)该反应体系中还伴随着化学反应(Ⅱ):I2(aq) + I-(aq)
 I3-(aq)。反应Ⅱ的平衡常数表达式为:
I3-(aq)。反应Ⅱ的平衡常数表达式为:(3)根据如图,计算反应Ⅱ中3-18s内用I2表示的反应速率为

(4)为探究Fe2+对上述O3氧化I-反应的影响,将O3通入含Fe2+和I-的混合溶液中。试预测因Fe2+的存在可能引发的化学反应(请用文字描述,如:“碘离子被臭氧氧化为碘单质”)①
(5)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢铁中的硫转化为H2SO3,然后以淀粉为指示剂,用一定浓度的I2溶液进行滴定。综合上述各步反应及已有知识,可推知氧化性强弱关系正确的是
a. Fe3+> I2 b. O3> Fe3+ c. I2> O2 d. I2>SO42-
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】有机合成中常用的钯/活性炭催化剂若长期使用,会被铁、有机化合物等杂质污染而失去活性,成为废催化剂。一种由废催化剂制取PdCl2的工艺流程如下:

(1)“焙烧1”通入空气的目的是________________ 。
(2)甲酸在反应中被氧化为二氧化碳,写出甲酸与PdO反应的化学方程式__________ 。
(3)加入浓氨水的过程中,需要控制溶液的pH为8~9,实验室中检测溶液pH的简单方法是_________________ 。
(4)写出“焙烧2”发生反应的化学方程式:_____________________________ 。
(5)Pd中加入王水的反应可以表示为:Pd+HCl+HNO3 → A+B↑+H2O(未配平)。其中B为无色有毒气体,该气体在空气中不能稳定存在;A中含有三种元素,其中Pd元素的质量分数为42.4%,H元素的质量分数为0.8%。则A的化学式为:____________ 。

(1)“焙烧1”通入空气的目的是
(2)甲酸在反应中被氧化为二氧化碳,写出甲酸与PdO反应的化学方程式
(3)加入浓氨水的过程中,需要控制溶液的pH为8~9,实验室中检测溶液pH的简单方法是
(4)写出“焙烧2”发生反应的化学方程式:
(5)Pd中加入王水的反应可以表示为:Pd+HCl+HNO3 → A+B↑+H2O(未配平)。其中B为无色有毒气体,该气体在空气中不能稳定存在;A中含有三种元素,其中Pd元素的质量分数为42.4%,H元素的质量分数为0.8%。则A的化学式为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】“建设生态文明是中华民族永续发展的千年大计。”控制和治理 、
、 是解决光化学烟雾、减少酸雨的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:
是解决光化学烟雾、减少酸雨的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:
(1) 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为_______ 。
(2)NO和 的处理。已除去
的处理。已除去 的硝酸尾气可用NaOH溶液吸收,主要反应如下:
的硝酸尾气可用NaOH溶液吸收,主要反应如下:
 、
、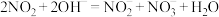
①吸收后的溶液经浓缩、结晶、过滤,得到 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是 ;吸收后排放的尾气中含量较高的氮氧化物是
;吸收后排放的尾气中含量较高的氮氧化物是_______ (填化学式)。
②Cu与适量浓硝酸反应生成0.9mol氮的氧化物(NO、 、
、 ),这些氧化物恰好能被500mL2mol⋅L-1NaOH溶液完全吸收,得到
),这些氧化物恰好能被500mL2mol⋅L-1NaOH溶液完全吸收,得到 和
和 的混合溶液,若参加反应的铜为51.2g,则生成
的混合溶液,若参加反应的铜为51.2g,则生成_______ mol 。
。
③在100mL稀 和稀
和稀 组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol·L-1.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中
组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol·L-1.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中 的物质的量浓度最大值为
的物质的量浓度最大值为_______ (反应前后溶液体积变化忽略不计)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。 和
和 ,其离子方程式为
,其离子方程式为_______ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是_______ 。
(4)吸收工厂烟气中的 ,能有效减少
,能有效减少 对空气的污染。
对空气的污染。
①富氧煅烧燃煤产生的低浓度的 可以在炉内添加
可以在炉内添加 通过以下方式脱除:
通过以下方式脱除:_______ 。
②氨水吸收 。当通入
。当通入 至溶液
至溶液 左右时,主要反应的离子方程式为
左右时,主要反应的离子方程式为_______ 。
已知:溶液中 、
、 ,
, 的物质的量分数随pH的分布如图所示。
的物质的量分数随pH的分布如图所示。
 、
、 是解决光化学烟雾、减少酸雨的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:
是解决光化学烟雾、减少酸雨的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:(1)
 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为(2)NO和
 的处理。已除去
的处理。已除去 的硝酸尾气可用NaOH溶液吸收,主要反应如下:
的硝酸尾气可用NaOH溶液吸收,主要反应如下: 、
、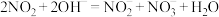
①吸收后的溶液经浓缩、结晶、过滤,得到
 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是 ;吸收后排放的尾气中含量较高的氮氧化物是
;吸收后排放的尾气中含量较高的氮氧化物是②Cu与适量浓硝酸反应生成0.9mol氮的氧化物(NO、
 、
、 ),这些氧化物恰好能被500mL2mol⋅L-1NaOH溶液完全吸收,得到
),这些氧化物恰好能被500mL2mol⋅L-1NaOH溶液完全吸收,得到 和
和 的混合溶液,若参加反应的铜为51.2g,则生成
的混合溶液,若参加反应的铜为51.2g,则生成 。
。③在100mL稀
 和稀
和稀 组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol·L-1.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中
组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol·L-1.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中 的物质的量浓度最大值为
的物质的量浓度最大值为(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。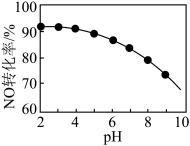
 和
和 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是
(4)吸收工厂烟气中的
 ,能有效减少
,能有效减少 对空气的污染。
对空气的污染。①富氧煅烧燃煤产生的低浓度的
 可以在炉内添加
可以在炉内添加 通过以下方式脱除:
通过以下方式脱除: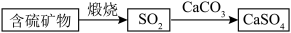
②氨水吸收
 。当通入
。当通入 至溶液
至溶液 左右时,主要反应的离子方程式为
左右时,主要反应的离子方程式为已知:溶液中
 、
、 ,
, 的物质的量分数随pH的分布如图所示。
的物质的量分数随pH的分布如图所示。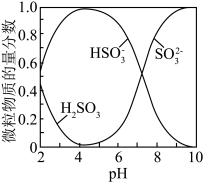
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】X、Y、Z、W为原子序数依次增大的四种短周期主族元素,其中X、Z同族,W、Z同周期, Y是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,W的最高正价与最低负价代数和为6。
(1)X元素的名称是________ 。该元素在周期表中的位置为_________
(2)Y元素符号是___________ Y元素的原子结构示意图为_________
(3)X、Y、Z三种元素按原子半径由大到小的顺序排列为___________ (用元素符号填空)
(4)X、Y、Z、W四种元素的最高价氧化物对应的水化物酸性最强的是_____________
碱性最强的是________________ (用化学式填空)
(5)写出 Y元素的最高价氧化物对应的水化物和W元素的最高价氧化物对应的水化物反应的离子方程式_________________________________________
(1)X元素的名称是
(2)Y元素符号是
(3)X、Y、Z三种元素按原子半径由大到小的顺序排列为
(4)X、Y、Z、W四种元素的最高价氧化物对应的水化物酸性最强的是
碱性最强的是
(5)写出 Y元素的最高价氧化物对应的水化物和W元素的最高价氧化物对应的水化物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E 五种短周期元素(A、B、C、D、E 分别代表元素符号),它们的原子序数依次增大; A 是元素周期表中原子半径最小的元素;B 元素最高价氧化物对应的水化物与其氢化物反应生成一种盐 X;D 与 A 同主族,且与 E 同周期;E 元素原子的最外层电子数是其次外层电子数的 3/4 倍;C 与 E 同 主族。请回答下列问题:
(1)X 的化学式_____ 。
(2)下列各项中,能说明元素 C 比 E 非金属性强的事实有_____ (填序号).
① 氢化物 H2E 的酸性比 H2C 强
② 氢化物 H2C 的热稳定性比 H2E 强
③ 氢化物 H2E 的水溶液放置在空气中会变浑浊
④ C 与 E 组成化合物,C 显负价
(3)将由 BC 和 BC2组成的混合气体通入如图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强。

已知(i)浓硝酸能将气体 BC 氧化成 BC2,而稀硝酸不能氧化 BC。
(ii)NaOH 溶液与 BC2反应的化学方程式为:2NaOH+2BC2═NaBC2+NaBC+H2O,NaOH 溶液与 BC 气体不反应。 装置②、③中盛放的药品依次是_______ 、______________ .
(4)通入混合气体之前,应先通入一段时间某另外一种气体,试推测先通入的该气体可以是__________ (填 一种气体的化学式)。
(1)X 的化学式
(2)下列各项中,能说明元素 C 比 E 非金属性强的事实有
① 氢化物 H2E 的酸性比 H2C 强
② 氢化物 H2C 的热稳定性比 H2E 强
③ 氢化物 H2E 的水溶液放置在空气中会变浑浊
④ C 与 E 组成化合物,C 显负价
(3)将由 BC 和 BC2组成的混合气体通入如图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强。

已知(i)浓硝酸能将气体 BC 氧化成 BC2,而稀硝酸不能氧化 BC。
(ii)NaOH 溶液与 BC2反应的化学方程式为:2NaOH+2BC2═NaBC2+NaBC+H2O,NaOH 溶液与 BC 气体不反应。 装置②、③中盛放的药品依次是
(4)通入混合气体之前,应先通入一段时间某另外一种气体,试推测先通入的该气体可以是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】现有前四周期的 A、B、C、D、E、F、G 七种元素,原子序数依次增大。A 元素的价电子构型为 nsnnpn+1;C 元素为最活泼的非金属元素;D 元素核外有三个电子层,最外层电子数是核外电子总数的 ;E 元素正三价离子的 3d 轨道为半充满状态;F 元素基态原子的 M 层全充满,N 层没有成对电子,只有一个未成对电子;G 元素与 A 元素位于同一主族,其某种氧化物有剧毒。
;E 元素正三价离子的 3d 轨道为半充满状态;F 元素基态原子的 M 层全充满,N 层没有成对电子,只有一个未成对电子;G 元素与 A 元素位于同一主族,其某种氧化物有剧毒。
(1)A、B、C 三种元素的电负性由小到大的顺序为___________ (用元素符号表示)
(2)C 元素的电子排布图为___________
(3)F 元素位于元素周期表的___________ 区,其基态原子的电子排布式为___________
(4)G 元素可能的性质___________
A.其单质可作为半导体材料 B.其电负性大于 P
C.其原子半径大于 Ge D.其第一电离能小于 Se
(5) I1(D)___________ I1(Al)(填“>”或“<”,下同),其原因是___________
 ;E 元素正三价离子的 3d 轨道为半充满状态;F 元素基态原子的 M 层全充满,N 层没有成对电子,只有一个未成对电子;G 元素与 A 元素位于同一主族,其某种氧化物有剧毒。
;E 元素正三价离子的 3d 轨道为半充满状态;F 元素基态原子的 M 层全充满,N 层没有成对电子,只有一个未成对电子;G 元素与 A 元素位于同一主族,其某种氧化物有剧毒。(1)A、B、C 三种元素的电负性由小到大的顺序为
(2)C 元素的电子排布图为
(3)F 元素位于元素周期表的
(4)G 元素可能的性质
A.其单质可作为半导体材料 B.其电负性大于 P
C.其原子半径大于 Ge D.其第一电离能小于 Se
(5) I1(D)
您最近一年使用:0次



