用 CuSO4·5H2O晶体,配制0.2 mol/L的CuSO4溶液480 mL。
(1)实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少_____________ 。
(2)容量瓶使用前应___________ 。
(3)应用托盘天平称取CuSO4·5H2O晶体的质量为___________ g。
(4)配制溶液时有以下几个操作:①溶解、②摇匀、③洗涤并转移、④冷却、⑤称量、⑥转移溶液、⑦定容、⑧装瓶贴标签,则正确的操作顺序是________________ (填序号)。
(5)下列操作对所配溶液的浓度偏高的有________ (填序号)
①硫酸铜晶体失去了部分结晶水
②用“左码右物”的称量方法称量晶体并使用了游码
③硫酸铜晶体不纯,其中混有杂质
④称量硫酸铜晶体时所用砝码生锈
⑤容量瓶未经干燥就使用
⑥转移液体时不小心洒落了一滴在容量瓶的外面
⑦定容时俯视刻线
⑧摇匀后,凹液面低于刻度线未做任何处理
(1)实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少
(2)容量瓶使用前应
(3)应用托盘天平称取CuSO4·5H2O晶体的质量为
(4)配制溶液时有以下几个操作:①溶解、②摇匀、③洗涤并转移、④冷却、⑤称量、⑥转移溶液、⑦定容、⑧装瓶贴标签,则正确的操作顺序是
(5)下列操作对所配溶液的浓度偏高的有
①硫酸铜晶体失去了部分结晶水
②用“左码右物”的称量方法称量晶体并使用了游码
③硫酸铜晶体不纯,其中混有杂质
④称量硫酸铜晶体时所用砝码生锈
⑤容量瓶未经干燥就使用
⑥转移液体时不小心洒落了一滴在容量瓶的外面
⑦定容时俯视刻线
⑧摇匀后,凹液面低于刻度线未做任何处理
更新时间:2016-12-09 17:12:29
|
【知识点】 仪器使用与实验安全
相似题推荐
解答题-实验探究题
|
容易
(0.94)
【推荐1】NaCl和NaClO在酸性条件下可发生反应:ClO- + Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况。
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质。写出化学反应方程式:_________________________________ 。
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分,从而判断该消毒液是否变质。
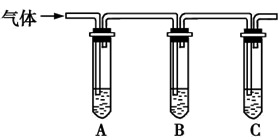
限选试剂:98%浓硫酸、1%品红溶液、1.0 mol·L-1 KI-淀粉溶液、1.0 mol·L-1NaOH溶液、澄清石灰水、饱和NaCl溶液。
请完成下列实验方案。
(3)用滴定法测定消毒液中NaClO的浓度。实验步骤如下:
①量取 25.00 mL消毒液放入锥形瓶中,加入过量的a mol·L-1 Na2SO3溶液b mL。
②滴定分析。将c mol·L-1的酸性KMnO4溶液装入______ (填“酸式”或“碱式”)滴定管中滴定,使KMnO4和剩余的Na2SO3发生反应。当溶液由无色变成浅红色,且半分钟内红色保持不褪去时,停止滴定,记录数据。重复滴定实验3次,测得平均消耗酸性KMnO4溶液V mL;滴定过程中涉及的反应有:NaClO+Na2SO3=NaCl+Na2SO4 ;2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O。
③计算。消毒液中NaClO的浓度为__ mol·L-1(用含a、b、c、V的代数式表示)。
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质。写出化学反应方程式:
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分,从而判断该消毒液是否变质。

限选试剂:98%浓硫酸、1%品红溶液、1.0 mol·L-1 KI-淀粉溶液、1.0 mol·L-1NaOH溶液、澄清石灰水、饱和NaCl溶液。
请完成下列实验方案。
| 所加试剂 | 预期现象和结论 |
| 向试管A中加足量①; 试管B中加1%品红溶液; 试管C中加②。 | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊,则消毒液部分变质; ③ ④ |
①量取 25.00 mL消毒液放入锥形瓶中,加入过量的a mol·L-1 Na2SO3溶液b mL。
②滴定分析。将c mol·L-1的酸性KMnO4溶液装入
③计算。消毒液中NaClO的浓度为
您最近半年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐2】在烧杯或试管里进行固体物质的溶解时,为了加快溶解速度,常采用的方法有_______ 、_______ 、_______ 等。
您最近半年使用:0次