某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性和强挥发性。他们参观生产过程后,绘制了如图装置简图。
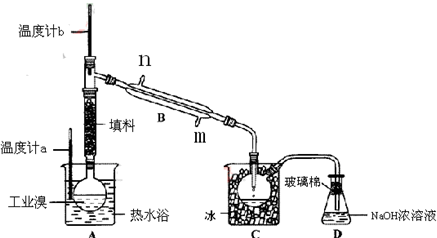
请你参与分析讨论:
(1)图中仪器B的名称:_____ ,冷却水从_____ 进,_____ 出。
(2)烧杯A的作用_____________ ,C中冰的作用是_____ 。

请你参与分析讨论:
(1)图中仪器B的名称:
(2)烧杯A的作用
19-20高一·浙江·期中 查看更多[1]
(已下线)【新东方】高一化学二轮班期中诊断试题卷 B1
更新时间:2020-07-09 12:17:20
|
相似题推荐
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐1】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
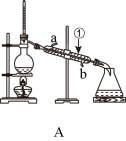


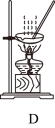
(1)装置C中玻璃仪器的名称为_______ 。
(2)从碘水中分离出I2,选择装置_______ (填代表装置图的字母,下同),该分离方法的名称为_______ 、 _______ 。
(3)从氯化钾溶液中得到氯化钾固体,选择装置_______ ;除去自来水中的Cl-等杂质,选择装置_______ 。
(4)装置A中①的名称是_______ ,进水的方向是从_______ 口进水,加入沸石或碎瓷片的目的是_______ ,温度计水银球的位置为_______ 。



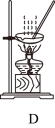
(1)装置C中玻璃仪器的名称为
(2)从碘水中分离出I2,选择装置
(3)从氯化钾溶液中得到氯化钾固体,选择装置
(4)装置A中①的名称是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐2】碘化钠可用作甲状腺肿瘤防治剂、祛痰剂和利尿剂等,实验室用NaOH、单质碘和水合肼(N2H4·H2O)为原料制备碘化钠。已知:水合肼易被空气氧化。回答下列问题:
(1)水合肼的制备
①制取次氯酸钠和氢氧化钠的混合液。盛装氢氧化钠溶液的仪器名称是__ ,正确的连接顺序为__ (按气流方向,用小写字母表示)。
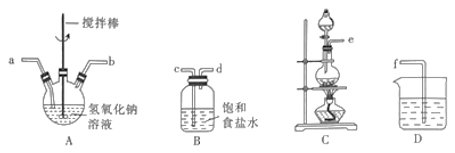
②将尿素滴入次氯酸钠和氢氧化钠的混合液中,发生反应CO(NH2)2+NaClO+2NaOH=N2H4·H2O+NaCl+Na2CO3,反应中作氧化剂的是__ [填“NaClO”或“CO(NH2)2”]。
(2)碘化钠的制备
I.向锥形瓶中加入40mL6mol·L-1NaOH溶液,搅拌、冷却,加入25.4g单质碘,打开恒温磁力搅拌器,保持60~70℃至反应完全;
II.继续加入稍过量的N2H4·H2O,还原生成的NaIO和NaIO3,得到NaI溶液,同时释放出一种空气中主要成分的气体;
III.将溶液蒸发浓缩、冷却结晶过滤、洗涤、干燥,得产品25.5g。
①步骤I反应完全的现象是__ 。
②步骤II中IO-参与反应的离子方程式为__ 。
③实验发现,水合肼实际用量比理论值偏高,可能的原因是__ 。
④测定产品中NaI含量的实验步骤如下:
a.称取10.00g产品并溶解,在500mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中,然后加入足量FeCl3溶液,充分反应后,再加入M溶液作指示剂;
c.用0.2100mol·L-1的Na2S2O3标准溶液滴定至终点(化学方程式为2Na2S2O3+I2=Na2S4O6+2NaI),重复实验多次.测得平均消耗Na2S2O3标准溶液的体积为15.00mL。则M为__ (写名称);该产品中NI的质量分数为__ 。
⑤工业上也可用硫化钠或铁屑还原碘酸钠来制备碘化钠,但水合肼还原法制得的产品纯度更高,其原因__ 。
(1)水合肼的制备
①制取次氯酸钠和氢氧化钠的混合液。盛装氢氧化钠溶液的仪器名称是

②将尿素滴入次氯酸钠和氢氧化钠的混合液中,发生反应CO(NH2)2+NaClO+2NaOH=N2H4·H2O+NaCl+Na2CO3,反应中作氧化剂的是
(2)碘化钠的制备
I.向锥形瓶中加入40mL6mol·L-1NaOH溶液,搅拌、冷却,加入25.4g单质碘,打开恒温磁力搅拌器,保持60~70℃至反应完全;
II.继续加入稍过量的N2H4·H2O,还原生成的NaIO和NaIO3,得到NaI溶液,同时释放出一种空气中主要成分的气体;
III.将溶液蒸发浓缩、冷却结晶过滤、洗涤、干燥,得产品25.5g。
①步骤I反应完全的现象是
②步骤II中IO-参与反应的离子方程式为
③实验发现,水合肼实际用量比理论值偏高,可能的原因是
④测定产品中NaI含量的实验步骤如下:
a.称取10.00g产品并溶解,在500mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中,然后加入足量FeCl3溶液,充分反应后,再加入M溶液作指示剂;
c.用0.2100mol·L-1的Na2S2O3标准溶液滴定至终点(化学方程式为2Na2S2O3+I2=Na2S4O6+2NaI),重复实验多次.测得平均消耗Na2S2O3标准溶液的体积为15.00mL。则M为
⑤工业上也可用硫化钠或铁屑还原碘酸钠来制备碘化钠,但水合肼还原法制得的产品纯度更高,其原因
您最近一年使用:0次
【推荐3】Ⅰ.海带灰中富含以I−形式存在的碘元素。实验室提取I2的途径如下所示:
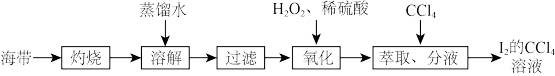
(1)灼烧海带至灰烬时所用的主要仪器名称是______ 。
(2)写出氧化环节的离子反应方程式:______ 。反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈______ 色。
(3)从I2的四氯化碳溶液中提取出碘单质的实验操作名称为______ 。
Ⅱ.某同学在实验室用铝土矿(含有Al2O3和SiO2,不考虑其他杂质)制取金属铝的流程如下:
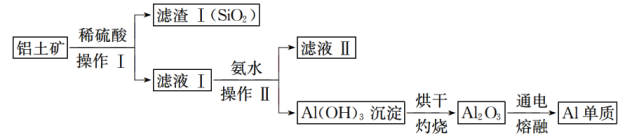
(1)写出操作Ⅱ中生成Al(OH)3沉淀的离子反应方程式为______ 。
(2)滤液Ⅱ中溶质的用途之一是______ 。
(3)电解熔融的Al2O3除得到金属铝之外,还可得到的气体产物是______ (填化学式)。

(1)灼烧海带至灰烬时所用的主要仪器名称是
(2)写出氧化环节的离子反应方程式:
(3)从I2的四氯化碳溶液中提取出碘单质的实验操作名称为
Ⅱ.某同学在实验室用铝土矿(含有Al2O3和SiO2,不考虑其他杂质)制取金属铝的流程如下:

(1)写出操作Ⅱ中生成Al(OH)3沉淀的离子反应方程式为
(2)滤液Ⅱ中溶质的用途之一是
(3)电解熔融的Al2O3除得到金属铝之外,还可得到的气体产物是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐1】⑴写出下图石油的蒸馏装置中所指仪器的名称:
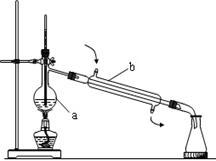
a.____________ , b._________ 。
⑵指出右图石油的蒸馏装置中的错误之处:
①缺铁圈和_______________ 。
②缺__________________ 防液体暴沸)。
③___________________________________ 。
④_________________________________ 。

a.
⑵指出右图石油的蒸馏装置中的错误之处:
①缺铁圈和
②缺
③
④
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐2】以下是实验室常用的部分仪器,请回答下列问题:
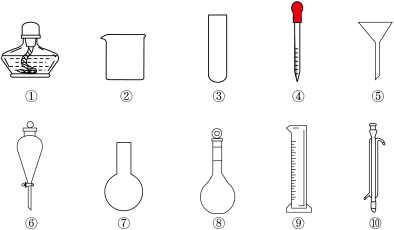
(1)序号为⑧和⑩的仪器的名称分别为______ 、_______ 。
(2)在分液操作中,必须用到上述仪器中的__________ (填序号)。
(3)能作反应容器且可直接加热的仪器是上述中的__________ (填名称)。
(4)配制一定物质的量浓度的溶液时要用到的仪器是____________ (填序号)。
(5)如图是温度计、量筒、滴定管的一部分,下述读数(虚线对应刻度)及说法正确的是_________ 。
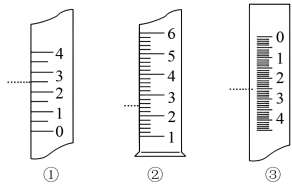
A.①是量筒,读数为 2.5 mL B.②是量筒,读数为 2.5 mL
C.③是滴定管,读数为 2.5 mL D.②是温度计,读数为 2.5 ℃
(6)除去氧化钙中的碳酸钙可用什么方法?______________ 。

(1)序号为⑧和⑩的仪器的名称分别为
(2)在分液操作中,必须用到上述仪器中的
(3)能作反应容器且可直接加热的仪器是上述中的
(4)配制一定物质的量浓度的溶液时要用到的仪器是
(5)如图是温度计、量筒、滴定管的一部分,下述读数(虚线对应刻度)及说法正确的是

A.①是量筒,读数为 2.5 mL B.②是量筒,读数为 2.5 mL
C.③是滴定管,读数为 2.5 mL D.②是温度计,读数为 2.5 ℃
(6)除去氧化钙中的碳酸钙可用什么方法?
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐3】如图所示的仪器和装置,请回答有关问题:
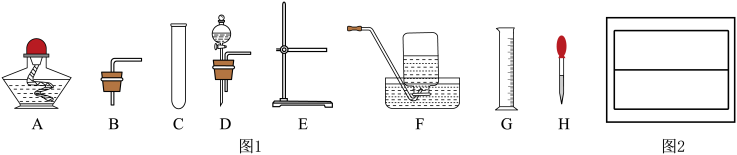
(1)若用高锰酸钾制取氧气,该反应的化学方程式是_____ ,其气体发生装置可选择上图中_____ (填标号)组合;
(2)实验室也可以用过氧化氢溶液来制取氧气,现要配制 溶质质量分数为
溶质质量分数为 的过氧化氢溶液,需要
的过氧化氢溶液,需要 的过氧化氢溶液
的过氧化氢溶液_____  ,若用
,若用 来量取
来量取 的过氧化氢溶液时,仰视读数,则配得的溶液中溶质质量分数
的过氧化氢溶液时,仰视读数,则配得的溶液中溶质质量分数_____ (填“偏大”或“偏小”);
(3)将配制好的溶液装入试剂瓶中,贴好标签。请在如图2所示的标签内填入试剂瓶所要贴的标签内容_____ 。

(1)若用高锰酸钾制取氧气,该反应的化学方程式是
(2)实验室也可以用过氧化氢溶液来制取氧气,现要配制
 溶质质量分数为
溶质质量分数为 的过氧化氢溶液,需要
的过氧化氢溶液,需要 的过氧化氢溶液
的过氧化氢溶液 ,若用
,若用 来量取
来量取 的过氧化氢溶液时,仰视读数,则配得的溶液中溶质质量分数
的过氧化氢溶液时,仰视读数,则配得的溶液中溶质质量分数(3)将配制好的溶液装入试剂瓶中,贴好标签。请在如图2所示的标签内填入试剂瓶所要贴的标签内容
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
解题方法
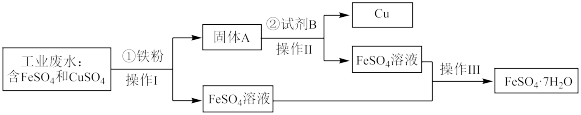
【推荐1】某工厂的工业废水中含有大量的FeSO4和CuSO4,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收FeSO4和金属Cu。请根据以下流程图,回答相关问题:_______ 。
(2)为了将CuSO4完全 转化,步骤①加入的铁粉应_______ (选填“过量”或“少量”),其对应的离子方程式为_______ 。
(3)固体A的成分是铁和_______ (填名称)。
(4)步骤②加入试剂B的稀溶液,B的化学式为_______ ,该物质在该反应中作_______ 剂(选填“氧化”或“还原”)。
(5)取1~2ml FeSO4溶液于试管中,滴加几滴NaOH溶液,生成的白色沉淀迅速变为灰绿色,最后变成_______ 色。
(6)另取1~2mLFeSO4溶液于试管中,滴加几滴氯水,该反应的离子方程式为_______ ,向反应后的溶液中再滴加几滴_______ 溶液,溶液变为血红色。
(2)为了将CuSO4
(3)固体A的成分是铁和
(4)步骤②加入试剂B的稀溶液,B的化学式为
(5)取1~2ml FeSO4溶液于试管中,滴加几滴NaOH溶液,生成的白色沉淀迅速变为灰绿色,最后变成
(6)另取1~2mLFeSO4溶液于试管中,滴加几滴氯水,该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
解题方法
【推荐2】肼(N2H4)是氮和氢形成的一种化合物,易溶于水。工业上利用尿素法生产肼,同时得到副产品十水合碳酸钠,其工艺流程如图:
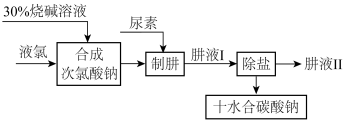
制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O
(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有______ (填标号)。
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2+H2O=HCl+HClO,请推测C12与NaOH溶液发生反应的化学方程式:____ 。从后续反应过程来看,若要使原料不浪费,合成次氯酸钠时投入的液氯与烧碱的质量之比为71:_________ 。
(3)实验室中,欲从母液中分离出十水合碳酸钠晶体。可采用的操作依次为________ 。(填标号)
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等。请写出肼除氧时发生反应的化学方程式:______________ 。

制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O
(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2+H2O=HCl+HClO,请推测C12与NaOH溶液发生反应的化学方程式:
(3)实验室中,欲从母液中分离出十水合碳酸钠晶体。可采用的操作依次为
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等。请写出肼除氧时发生反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
解题方法
【推荐3】某研究小组利用含硫酸亚铁和硫酸铜的工业废料制备铁红 氧化铁
氧化铁 和硫酸铵晶体。流程如图:
和硫酸铵晶体。流程如图:
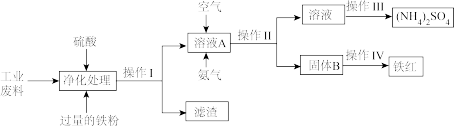
请回答下列问题:
(1)操作Ⅰ的名称是_____________ ,滤渣的成分为______________ 。
(2)简述下列实验操作:
①检验溶液A中金属阳离子的方法为__________________________ ;
②检验固体B是否被洗涤干净的方法是____________ 。
(3)测定废料中硫酸铜的质量分数:称取a g废料样品,将操作Ⅰ得到的滤渣用足量稀硫酸溶解、过滤、洗涤、干燥,称得固体质量为b g,则废料中硫酸铜的质量分数______________  写出含a、b的表达式
写出含a、b的表达式 。
。
 氧化铁
氧化铁 和硫酸铵晶体。流程如图:
和硫酸铵晶体。流程如图:
请回答下列问题:
(1)操作Ⅰ的名称是
(2)简述下列实验操作:
①检验溶液A中金属阳离子的方法为
②检验固体B是否被洗涤干净的方法是
(3)测定废料中硫酸铜的质量分数:称取a g废料样品,将操作Ⅰ得到的滤渣用足量稀硫酸溶解、过滤、洗涤、干燥,称得固体质量为b g,则废料中硫酸铜的质量分数
 写出含a、b的表达式
写出含a、b的表达式 。
。
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐1】实验室中用浓盐酸与MnO2制取Cl2,再用Cl2和Ca(OH)2反应制少量漂白粉。已知Cl2和Ca(OH)2制漂白粉是放热反应,温度稍高易发生副反应:
6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。现有三位同学分别设计的三套实验装置如下(U形管中放有玻璃纤维,气体能顺利通过):
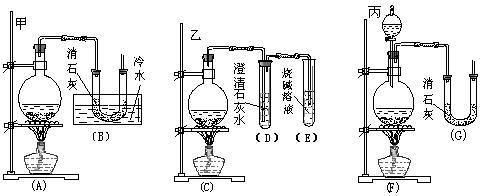
(1)请从以下六方面对上述甲、乙、丙三套装置的优缺点进行评价,将适当的选项序号填于下表内:
a.不易控制反应速率 b.容易控制反应速率 c.有副反应发生
d.可防止副反应发生 e.容易污染环境 f.可防止污染环境
(2)请从甲、乙、丙三套装置中,选取合理的组成部分(A、B、C、D、E、F、G),组装一套你认为更完善的实验装置,连接顺序(按气流从左到右的方向)为___________ ;在此装置及甲、乙、丙三装置中,你认为是否还缺少必要的装置,并说明原因_________________________________________________________________________________________________________________________________________ 。
(3)如果反应前加入了mg Ca(OH)2,反应结束并冷却后倒出固体物质称量为ng(设反应中产生的水仍留在固体物质中)。则该固体物质中Ca(ClO)2的质量分数的表达式为(不必化简):__________________________________________________ 。
6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。现有三位同学分别设计的三套实验装置如下(U形管中放有玻璃纤维,气体能顺利通过):

(1)请从以下六方面对上述甲、乙、丙三套装置的优缺点进行评价,将适当的选项序号填于下表内:
a.不易控制反应速率 b.容易控制反应速率 c.有副反应发生
d.可防止副反应发生 e.容易污染环境 f.可防止污染环境
| 优点 | 缺点 | |
| 甲装置 | ||
| 乙装置 | ||
| 丙装置 |
(3)如果反应前加入了mg Ca(OH)2,反应结束并冷却后倒出固体物质称量为ng(设反应中产生的水仍留在固体物质中)。则该固体物质中Ca(ClO)2的质量分数的表达式为(不必化简):
您最近一年使用:0次
解答题-无机推断题
|
容易
(0.94)
名校
解题方法
【推荐2】如表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是_____ ,C、D、E三种元素的简单离子半径从大到小的顺序是______ (填离子符号)。
(2)B的最高价氧化物对应的水化物和简单氢化物反应,实验现象为______ 。
(3)D单质在空气中燃烧可生成淡黄色粉末X,X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和如图所示实验装置证明X有提供氧气的作用,X盛放在装置C中。
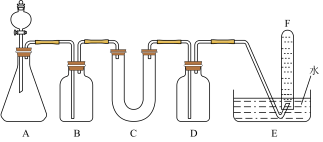
①装置A使用石灰石与盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是______ 。
②装置C中X与CO2反应的化学方程式是______ ,装置D盛放NaOH溶液的作用是除去CO2。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是
(2)B的最高价氧化物对应的水化物和简单氢化物反应,实验现象为
(3)D单质在空气中燃烧可生成淡黄色粉末X,X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和如图所示实验装置证明X有提供氧气的作用,X盛放在装置C中。

①装置A使用石灰石与盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是
②装置C中X与CO2反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐3】FeCl3为黑棕色固体,无水氯化铁在300℃以上升华,遇潮湿空气极易潮解。
(1)甲组同学拟用下列装置制取纯净干燥的氯气。
①装置B的作用是_________
②装置A中发生反应时消耗的氧化剂和还原剂的物质的量之比为__________
(2)乙组同学选用甲组实验中的装置ABC和下列装置制取FeCl3

①乙组同学的实验装置中,依次连接的合理顺序为:a→_____ →_____ →_____ →_____ →_____ →_____
②连好装置,检查装置的气密性,先打开装置A中___________ (填仪器的名称)的活塞,直到______ 再点燃装置F处的酒精灯,目的是_______
③装置D的作用有_______
(3)实验结束后,取少量F中的固体加水溶解,欲对所得产物FeCl3中是否含有FeCl2进行检测,所需试剂是_______
a.KSCN b.H2O2 c.K3[Fe(CN)6] d. .K4[Fe(CN)6]
经检测发现溶液中含有Fe2+,丙同学认为所得产物FeCl3中一定含有FeCl2,丁同学认为不一定,理由是_____
(1)甲组同学拟用下列装置制取纯净干燥的氯气。
①装置B的作用是
②装置A中发生反应时消耗的氧化剂和还原剂的物质的量之比为
(2)乙组同学选用甲组实验中的装置ABC和下列装置制取FeCl3

①乙组同学的实验装置中,依次连接的合理顺序为:a→
②连好装置,检查装置的气密性,先打开装置A中
③装置D的作用有
(3)实验结束后,取少量F中的固体加水溶解,欲对所得产物FeCl3中是否含有FeCl2进行检测,所需试剂是
a.KSCN b.H2O2 c.K3[Fe(CN)6] d. .K4[Fe(CN)6]
经检测发现溶液中含有Fe2+,丙同学认为所得产物FeCl3中一定含有FeCl2,丁同学认为不一定,理由是
您最近一年使用:0次



