将10℃的0.2molN2O4置于2L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) 2NO2(g)。下列结论能说明上述反应在该条件下已经达到平衡状态的是
2NO2(g)。下列结论能说明上述反应在该条件下已经达到平衡状态的是
①烧瓶内气体的平均相对分子质量不再变化
②NO2的物质的量浓度不再改变
③烧瓶内气体的压强不再变化
④烧瓶内气体的质量不再变化
⑤烧瓶内气体的颜色不再加深
⑥N2O4的消耗速率与NO2的生成速率之比为1:2
⑦NO2生成速率与NO2消耗速率相等
⑧烧瓶内气体的密度不再变化。
 2NO2(g)。下列结论能说明上述反应在该条件下已经达到平衡状态的是
2NO2(g)。下列结论能说明上述反应在该条件下已经达到平衡状态的是①烧瓶内气体的平均相对分子质量不再变化
②NO2的物质的量浓度不再改变
③烧瓶内气体的压强不再变化
④烧瓶内气体的质量不再变化
⑤烧瓶内气体的颜色不再加深
⑥N2O4的消耗速率与NO2的生成速率之比为1:2
⑦NO2生成速率与NO2消耗速率相等
⑧烧瓶内气体的密度不再变化。
| A.①②③⑤⑦ | B.①②③⑤⑥⑦ | C.①②③④ | D.②③⑦⑧ |
更新时间:2016/12/05 19:25:12
|
【知识点】 化学平衡
相似题推荐
单选题
|
适中
(0.65)
【推荐1】向体积为10L的恒容密闭容器中通入1.5mol 和1.5mol
和1.5mol 制备
制备 ,反应原理为
,反应原理为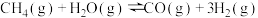 。在不同温度(
。在不同温度(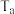 、
、 )下测得容器中
)下测得容器中 随时间的变化曲线如下图所示。
随时间的变化曲线如下图所示。
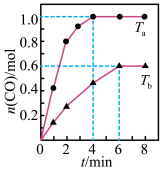
下列说法不正确 的是
 和1.5mol
和1.5mol 制备
制备 ,反应原理为
,反应原理为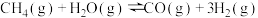 。在不同温度(
。在不同温度(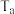 、
、 )下测得容器中
)下测得容器中 随时间的变化曲线如下图所示。
随时间的变化曲线如下图所示。
下列说法
A.该反应的正方向 |
B.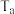 时, 时, 的平衡转化率 的平衡转化率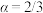 |
C. 时,若改为恒温恒压容器,平衡时 时,若改为恒温恒压容器,平衡时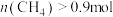 |
D.达平衡后再充入 ,不能提高 ,不能提高 的转化率 的转化率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将一定量的CO2与H2通入某密闭容器中合成甲醇,在催化剂作用下发生下述反应:
Ⅰ. CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1<0
CH3OH(g)+H2O(g) ΔH1<0
Ⅱ. CO2(g)+H2(g) H2O(g)+CO(g) ΔH2
H2O(g)+CO(g) ΔH2
催化反应相同时间,测得不同温度下CO2的转化率如图1所示(图中虚线表示相同条件下CO2的平衡转化率随温度的变化),CH3OH 的产率如图2所示。
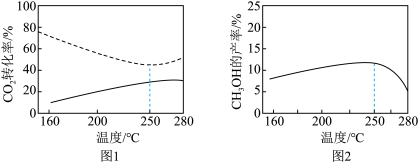
下列有关说法正确的是
Ⅰ. CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1<0
CH3OH(g)+H2O(g) ΔH1<0Ⅱ. CO2(g)+H2(g)
 H2O(g)+CO(g) ΔH2
H2O(g)+CO(g) ΔH2催化反应相同时间,测得不同温度下CO2的转化率如图1所示(图中虚线表示相同条件下CO2的平衡转化率随温度的变化),CH3OH 的产率如图2所示。

下列有关说法正确的是
| A.ΔH2 < 0 |
| B.250℃时,容器内反应达平衡 |
| C.250℃后, 随温度升高CH3OH 的产率减小,可能是因为催化剂对反应Ⅰ的活性降低 |
| D.250℃前,随温度升高CO2的平衡转化率减小,可能因为该温度范围内仅发生反应Ⅰ |
您最近半年使用:0次

 ,其转化率随温度变化如图所示。下列说法正确的是
,其转化率随温度变化如图所示。下列说法正确的是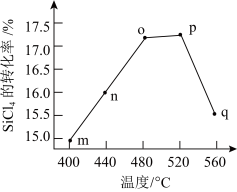
 的转化率
的转化率