已知热化学方程式:SO2(g)+ O2(g)
O2(g) SO3(g)
SO3(g)  H=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
H=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
 O2(g)
O2(g) SO3(g)
SO3(g)  H=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
H=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为| A.98.32kJ | B.196.64kJ/mol | C.<196.64kJ | D.>196.64kJ |
更新时间:2016/12/05 21:05:57
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】甲酸在一定条件下可分解生成CO和H2O,在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法正确的是
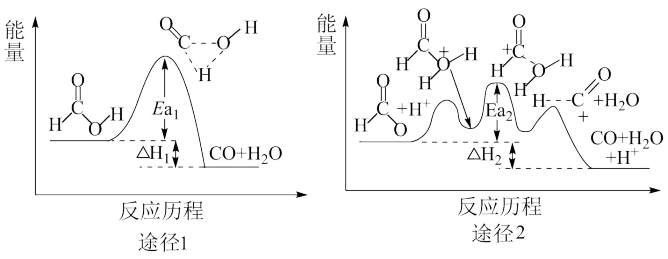

| A.途径1的活化能为Ea1,其大小与∆H1有关 |
| B.途径1使用了催化剂,途径2没有使用催化剂,但∆H1=∆H2 |
| C.途径2要经过三步才完成,而途径1只要一步就完成,所以途径1反应速率更快 |
| D.途径2中第二步反应的速率比第三步反应要慢 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】我国的“长三丙火箭”第三级推进器使用的燃料是液态氢。已知在25 C时,2 g H2在O2中完全燃烧生成液态水时放出热量285.8 kJ。下列有关说法中,正确的是
| A.H2的燃烧热为–285.8 kJ |
| B.2H2(g) + O2(g) = 2H2O(l) H = –571.6 kJ·mol–1 |
| C.25 C时,2H2(g) + O2(g) = 2H2O(g)的H –571.6 kJ·mol–1 |
| D.25 C时,11.2 L H2在O2中完全燃烧生成液态水时放出热量142.9 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】P4(白磷,s)⇌4P(红磷,s) ΔH=-17kJ·mol-1,根据以上热化学方程式,下列推论正确的是( )
| A.正反应是一个吸热反应 |
| B.白磷比红磷稳定 |
| C.当1mol白磷完全转变成红磷时放出17kJ热量 |
| D.当4g红磷转变成白磷时吸收17kJ热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于各图象的解释或得出的结论正确的是
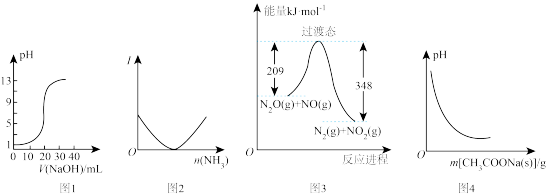

| A.图1表示0.10 mol·L-1的NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线 |
| B.图2表示向乙酸溶液中通入氨气至过量的过程中溶液导电性的变化 |
| C.根据图3所示可知:N2(g)+NO2(g)=N2O(g)+NO(g) ΔH=+139 kJ·mol-1 |
| D.图4表示向CH3COOH溶液中逐步加CH3COONa固体后,溶液pH的变化 |
您最近一年使用:0次



