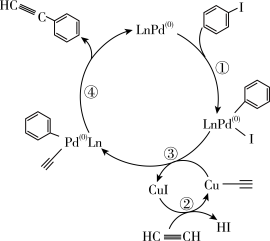
下列各组物质的熔点均与所含化学键的键能有关的是
| A.CaCl2、SiO2 | B.NaCl、HCl | C.CaO、CO2 | D.Cl2、I2 |
更新时间:2017-04-10 09:47:22
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列物质中,既含有离子键又含有共价键的是
| A.NH4NO3 | B.CH3COOH | C.K2O | D.H2SO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列各对原子序数的原子能以离子键结合成化合物的是
| A.1和17 | B.6和8 | C.13和17 | D.11和17 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中不正确的是
A. 键比 键比 键重叠程度大,形成的共价键通常更牢固 键重叠程度大,形成的共价键通常更牢固 |
B.两个原子之间形成共价键时,最多有一个 键 键 |
C.气体单质中,一定有 键,可能有 键,可能有 键 键 |
D. 分子中有一个 分子中有一个 键,2个 键,2个 键 键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】Ni可活化C2H6放出CH4,其反应历程如下图所示:
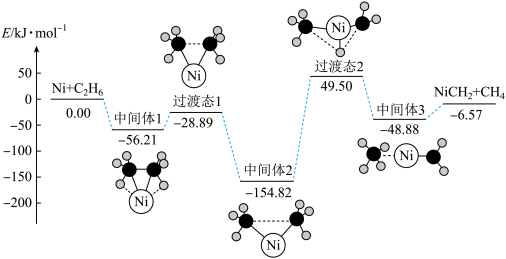
下列关于活化历程的说法正确的是

下列关于活化历程的说法正确的是
| A.决速步骤:中间体1→中间体2 | B.总反应为Ni+C2H6→NiCH2+CH4 |
| C.Ni−H键的形成对氢原子的迁移是不利的 | D.涉及非极性键的断裂和生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】有四个系列同族元素的物质,101.3 kPa 时测定的部分沸点(℃)数据如下表所示:
对应表中内容,下列叙述中正确的是
| ① | He -268.8 | Ne-249.5 | (a)-185.8 | Kr-151.7 |
| ② | F2 -187.0 | Cl2 -33.6 | (b)58.7 | I2 |
| ③ | (c) | HCl-84.0 | HBr -67.0 | HI |
| ④ | CH4 -161.0 | SiH4 -112.0 | GeH4 -90.0 | (d) -52.0 |
| A.系列①物质均为非金属单质,都含有共价键 |
| B.系列②物质的沸点逐渐升高是因为共价键越来越牢固 |
| C.系列③物质的还原性依次减弱 |
| D.沸点顺序:(c) >HI |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列关于化学键说法正确的是
A. 既有离子键又有共价键 既有离子键又有共价键 | B.破坏化学键的过程,一定发生了化学变化 |
| C.含离子键的化合物一定是离子化合物 | D.干冰升华过程中破坏了共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】类推的思维方法在化学学习与研究中可能会产生错误的结论,因此类推出的结论需经过实践的检验才能确定其正确与否。下列几种类推结论正确的是
| A.金刚石中C—C键的键长为154.45pm,C60中C—C键的键长为140~145pm,所以C60的熔点高于金刚石 |
| B.CO2晶体是分子晶体,SiO2晶体也是分子晶体 |
C.从CH4、NH 、SO 、SO 为正面体结构,可推测CC14、PH 为正面体结构,可推测CC14、PH 、PO 、PO 也为正四面体结构 也为正四面体结构 |
| D.C2H6是碳链为直线形的非极性分子,可推测C3H8也是碳链为直线形的非极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法中正确的有:
①含有离子的晶体一定是离子晶体
②离子键是阴、阳离子间的相互吸引作用
③金属晶体的导电性、导热性均与自由电子有关
④共价键的强弱决定分子晶体熔、沸点的高低
⑤共价晶体中一定含有共价键
⑥分子晶体的熔点一定比金属晶体低
⑦NaCl 晶体中,阴离子周围紧邻的阳离子数为6
⑧硬度由大到小:金刚石>碳化硅>晶体硅
①含有离子的晶体一定是离子晶体
②离子键是阴、阳离子间的相互吸引作用
③金属晶体的导电性、导热性均与自由电子有关
④共价键的强弱决定分子晶体熔、沸点的高低
⑤共价晶体中一定含有共价键
⑥分子晶体的熔点一定比金属晶体低
⑦NaCl 晶体中,阴离子周围紧邻的阳离子数为6
⑧硬度由大到小:金刚石>碳化硅>晶体硅
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次