A、B、C、D、E、F六种元素的原子序数依次递增。已知:
①已知F为第四周元素,除最外层只有一个电子外,其他各层上均填满电子,另外五种元素均为短周期主族元素;②A、C原子p轨道的电子数分别为2和4;③D原子最外层电子数为偶数;④E原子价电子(外围电子)排布为msnmpn-1。请回答下列问题:
(1)下列叙述正确的是_____ (填序号)。
A.金属键的强弱:D>E B.基态原子第一电离能:D>E
C.六种元素中,电负性最大的元素是E D.晶格能:NaCl<DCl2
(2)F基态原子的核外电子排布式为______ ;与F同一周期的元素中基态原子轨道上成单电子数最多的元素为______ (填元素符号)。
(3)A与C形成的非极性分子,该分子与过量强碱反应生成的酸根离子的空间构型为_____ 。
(4)已知原子数和价电子数相同的分子或离子为等电子体,互为等电子体的微粒结构相同,B3-中心原子的杂化轨道类型为____________ 。
①已知F为第四周元素,除最外层只有一个电子外,其他各层上均填满电子,另外五种元素均为短周期主族元素;②A、C原子p轨道的电子数分别为2和4;③D原子最外层电子数为偶数;④E原子价电子(外围电子)排布为msnmpn-1。请回答下列问题:
(1)下列叙述正确的是
A.金属键的强弱:D>E B.基态原子第一电离能:D>E
C.六种元素中,电负性最大的元素是E D.晶格能:NaCl<DCl2
(2)F基态原子的核外电子排布式为
(3)A与C形成的非极性分子,该分子与过量强碱反应生成的酸根离子的空间构型为
(4)已知原子数和价电子数相同的分子或离子为等电子体,互为等电子体的微粒结构相同,B3-中心原子的杂化轨道类型为
更新时间:2017-04-21 08:36:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)无机化合物甲、乙分别由三种元素组成。组成甲、乙化合物的元素原子的特征排布都可表示如下:asa、bsbbpb、csccp2c甲是一种溶解度较小的盐类化合物。由此可知甲、乙的化学式分别是___________ 、___________ 。
(2)根据周期表对角线规则,金属铍与铝的单质及其化合物性质相似,又已知氯化铝的熔、沸点较低,易升化。氢氧化铍与氢氧化镁可用___________ 鉴别,其离子方程式是___________ 。
(3)已知砷(As)元素原子的最外层电子排布是 4s24p3,砷酸钠在酸性条件下能把碘化钾氧化为单质碘,同时生成亚砷酸钠(Na3AsO3)和水,该反应的离子方程式为___________ 。
(1)无机化合物甲、乙分别由三种元素组成。组成甲、乙化合物的元素原子的特征排布都可表示如下:asa、bsbbpb、csccp2c甲是一种溶解度较小的盐类化合物。由此可知甲、乙的化学式分别是
(2)根据周期表对角线规则,金属铍与铝的单质及其化合物性质相似,又已知氯化铝的熔、沸点较低,易升化。氢氧化铍与氢氧化镁可用
(3)已知砷(As)元素原子的最外层电子排布是 4s24p3,砷酸钠在酸性条件下能把碘化钾氧化为单质碘,同时生成亚砷酸钠(Na3AsO3)和水,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)已知短周期元素A、B,A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为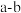 ,L层电子数为
,L层电子数为 ,则A为
,则A为___________ (填元素符号,下同),B为___________ 。
(2)已知X元素原子的L层比Y元素原子的L层少3个电子,Y元素原子的核外电子总数比X元素原子多5,则X、Y分别为___________ 、___________ 。
(1)已知短周期元素A、B,A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为
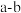 ,L层电子数为
,L层电子数为 ,则A为
,则A为(2)已知X元素原子的L层比Y元素原子的L层少3个电子,Y元素原子的核外电子总数比X元素原子多5,则X、Y分别为
您最近一年使用:0次

 ,B元素原子M层电子数为次外层与最内层电子数之差,C元素原子L层达稳定结构所需电子数为该层电子数的
,B元素原子M层电子数为次外层与最内层电子数之差,C元素原子L层达稳定结构所需电子数为该层电子数的 。由此推断三种元素名称分别是A
。由此推断三种元素名称分别是A

