A、B、C为电子层数小于或等于3的元素,A元素原子M层电子数为K层电子数的 ,B元素原子M层电子数为次外层与最内层电子数之差,C元素原子L层达稳定结构所需电子数为该层电子数的
,B元素原子M层电子数为次外层与最内层电子数之差,C元素原子L层达稳定结构所需电子数为该层电子数的 。由此推断三种元素名称分别是A
。由此推断三种元素名称分别是A________ 、B_______ 、C________ 。写出A的阳离子的结构示意图________ 。写出由A和B两种元素所形成的化合物的电离方程式________ 。
 ,B元素原子M层电子数为次外层与最内层电子数之差,C元素原子L层达稳定结构所需电子数为该层电子数的
,B元素原子M层电子数为次外层与最内层电子数之差,C元素原子L层达稳定结构所需电子数为该层电子数的 。由此推断三种元素名称分别是A
。由此推断三种元素名称分别是A
更新时间:2023-11-23 09:43:50
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】画出硒的原子结构示意图为___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业的关键原料之一,可由氨气和氟气反应得到:_______NH3+_______F2→_______NF3+_______NH4F。完成下列填空:
(1)配平上述反应方程式_______ 。
(2)F原子的结构示意图是_______ ,其能量最高的电子所占据的电子亚层符号为_______ 。从原子结构角度比较F和N元素的非金属性强弱_______ 。
(3)写出NH4F的电子式_______ ,溶液中NH 的检验方法是
的检验方法是_______ 。
(4)与NH 具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是
具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是_______ ,该产物的水溶液呈_______ 性,用适当的化学用语解释该溶液酸碱性的原因:_______ 。其稀溶液中存在关系式:c(OH-)-c(H+) =c(HCO ) +
) + _______
(1)配平上述反应方程式
(2)F原子的结构示意图是
(3)写出NH4F的电子式
 的检验方法是
的检验方法是(4)与NH
 具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是
具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是 ) +
) +
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】元素在周期表中的位置反映了元素的原子结构和性质。下图是元素周期表的一部分,请按要求回答下列问题:
(1)元素①位于元素周期表的第_______ 周期第_______ 族,它是形成化合物种类最多的元素。
(2)写出②的元素符号_______ 。
(3)画出元素④的原子结构示意图_______ 。
(4)元素③和⑤的最高价氧化物对应的水化物中碱性较强的是_______ (填化学式)。
(5)比较⑦和⑧的简单离子半径大小_______ >_______ (填离子符号)。
(6)写出元素⑧的单质与水反应的化学方程式:_______ 。
族 周期 | IA | 0 | |||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
(2)写出②的元素符号
(3)画出元素④的原子结构示意图
(4)元素③和⑤的最高价氧化物对应的水化物中碱性较强的是
(5)比较⑦和⑧的简单离子半径大小
(6)写出元素⑧的单质与水反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)某兴趣小组做电解质导电实验,如图所示。
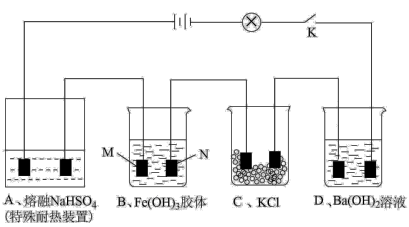
回答下列问题:
①闭合开关K,发现灯泡不亮,使灯泡变亮的方法___________ (写出一种方法即可)。
②装置A中电解质的电离方程式___________ ,在水溶液能与Fe反应生成氢气的离子方程式___________ 。
(2)向两份相同的Ba(OH)2溶液中,分别滴入浓度相等H2SO4和KHSO4,其导电能力随滴入溶液体积变化的曲线如下图所示。

①滴加H2SO4溶液的曲线是___________ (填①或②)。
②B点对应的溶液呈___________ (填“酸”、“碱”或“中”)性。
③起始点到D点之间发生反应的离子方程式为___________ 。
(1)某兴趣小组做电解质导电实验,如图所示。

回答下列问题:
①闭合开关K,发现灯泡不亮,使灯泡变亮的方法
②装置A中电解质的电离方程式
(2)向两份相同的Ba(OH)2溶液中,分别滴入浓度相等H2SO4和KHSO4,其导电能力随滴入溶液体积变化的曲线如下图所示。

①滴加H2SO4溶液的曲线是
②B点对应的溶液呈
③起始点到D点之间发生反应的离子方程式为
您最近一年使用:0次
【推荐2】回答下列问题:
(1)请写出以下物质溶于水的电离方程式:
H2SO4_______
(NH4)2SO4_______
(2)71 g某一价金属的硫酸盐中,含有0.5 mol SO ,则该硫酸盐的摩尔质量为
,则该硫酸盐的摩尔质量为___________ ,该金属的相对原子质量为___________ 。
(1)请写出以下物质溶于水的电离方程式:
H2SO4
(NH4)2SO4
(2)71 g某一价金属的硫酸盐中,含有0.5 mol SO
 ,则该硫酸盐的摩尔质量为
,则该硫酸盐的摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】溶液体系是化学反应的重要场所,也是高中化学重要的研究对象,物质在水溶液中有多种行为,请用化学用语解释下列行为
(1)25℃时,测得0.1mol/L NH3·H2O溶液的pH=11,由此确定NH3·H2O是弱电解质,NH3·H2O在水溶液中的电离方程式为:___________ 。
(2)25℃时,测得CH3COOH与CH3COONa的混合溶液pH=6,则溶液中存在的电荷关系为:c(CH3COO-)-c(Na+)=___________ (填计算式)。
(3)向沸水中逐滴滴加饱和FeCl3溶液,制备Fe(OH)3胶体,原理为:___________ 。
(4)磁化铝(Al2S3)等盐在水中不能存在,也不能通过水溶液中的离子反应来制取,原因是:___________ 。
(5)当向白色ZnS沉淀上滴加CuSO4溶液时,反应生成黑色的CuS沉淀,这种转化可表示为:___________ 。
(1)25℃时,测得0.1mol/L NH3·H2O溶液的pH=11,由此确定NH3·H2O是弱电解质,NH3·H2O在水溶液中的电离方程式为:
(2)25℃时,测得CH3COOH与CH3COONa的混合溶液pH=6,则溶液中存在的电荷关系为:c(CH3COO-)-c(Na+)=
(3)向沸水中逐滴滴加饱和FeCl3溶液,制备Fe(OH)3胶体,原理为:
(4)磁化铝(Al2S3)等盐在水中不能存在,也不能通过水溶液中的离子反应来制取,原因是:
(5)当向白色ZnS沉淀上滴加CuSO4溶液时,反应生成黑色的CuS沉淀,这种转化可表示为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某元素的基态原子最外层电子排布式为nsnnpn+2,则n=_______ ;基态原子中能量最高的是_______ 电子,核外电子的轨道表示式为_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)下列状态的镁中,电离最外层一个电子所需能量最大的是_____________ .
A.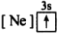 B.
B.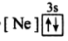 C.
C.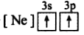 D.
D.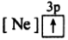
(2) 成为阳离子时首先失去
成为阳离子时首先失去____________ 轨道电子, 的价层电子排布式为
的价层电子排布式为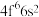 ,
,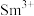 价层电子排布式为
价层电子排布式为____________ .比较离子半径:
____________ (填“大于”“小于”或“等于”) .
.
(3)在周期表中,与 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是___________ ,该元素基态原子核外 层电子的自旋
层电子的自旋___________ (填“相同”或“相反”). 中,电负性最高的元素是
中,电负性最高的元素是___________ .
(4) 基态核外电子排布式为
基态核外电子排布式为___________ .
A.
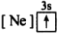 B.
B.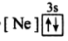 C.
C. D.
D.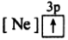
(2)
 成为阳离子时首先失去
成为阳离子时首先失去 的价层电子排布式为
的价层电子排布式为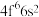 ,
,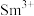 价层电子排布式为
价层电子排布式为
 .
.(3)在周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是 层电子的自旋
层电子的自旋 中,电负性最高的元素是
中,电负性最高的元素是(4)
 基态核外电子排布式为
基态核外电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A、B、C、D四种元素的核电荷数依次增大且质子数均小于18。已知A的原子核外最外层电子数是次外层电子数的2倍,B的最外层电子数是内层电子总数的1/2,C原子的核外次外层电子数为8,最外层电子数为6。D是四种元素中质子数最大的,则:
(1)A、B、C、D的元素符号分别是__________ 、_________ 、________ 、__________ 。
(2)B原子结构示意图是_________________ ,C离子结构示意图是_________________ 。
(1)A、B、C、D的元素符号分别是
(2)B原子结构示意图是
您最近一年使用:0次



