溶液体系是化学反应的重要场所,也是高中化学重要的研究对象,物质在水溶液中有多种行为,请用化学用语解释下列行为
(1)25℃时,测得0.1mol/L NH3·H2O溶液的pH=11,由此确定NH3·H2O是弱电解质,NH3·H2O在水溶液中的电离方程式为:___________ 。
(2)25℃时,测得CH3COOH与CH3COONa的混合溶液pH=6,则溶液中存在的电荷关系为:c(CH3COO-)-c(Na+)=___________ (填计算式)。
(3)向沸水中逐滴滴加饱和FeCl3溶液,制备Fe(OH)3胶体,原理为:___________ 。
(4)磁化铝(Al2S3)等盐在水中不能存在,也不能通过水溶液中的离子反应来制取,原因是:___________ 。
(5)当向白色ZnS沉淀上滴加CuSO4溶液时,反应生成黑色的CuS沉淀,这种转化可表示为:___________ 。
(1)25℃时,测得0.1mol/L NH3·H2O溶液的pH=11,由此确定NH3·H2O是弱电解质,NH3·H2O在水溶液中的电离方程式为:
(2)25℃时,测得CH3COOH与CH3COONa的混合溶液pH=6,则溶液中存在的电荷关系为:c(CH3COO-)-c(Na+)=
(3)向沸水中逐滴滴加饱和FeCl3溶液,制备Fe(OH)3胶体,原理为:
(4)磁化铝(Al2S3)等盐在水中不能存在,也不能通过水溶液中的离子反应来制取,原因是:
(5)当向白色ZnS沉淀上滴加CuSO4溶液时,反应生成黑色的CuS沉淀,这种转化可表示为:
更新时间:2024-01-03 15:42:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】分类是学习化学的重要方法,从物质的元素组成和化学性质视角对物质进行科学分类,可体现化学学科独有的魅力。回答下列问题:
(1)现有下列物质:①铜② ③熔融的
③熔融的 ④
④ ⑤酒精⑥氨水⑦稀硫酸⑧
⑤酒精⑥氨水⑦稀硫酸⑧ ⑨
⑨ 溶液⑩
溶液⑩ 胶体
胶体
①以上物质中,属于电解质且能导电的是___________ (填序号)
②写出⑨的电离方程式___________ 。
③写出实验室制备⑩的化学方程式___________ 。
④向 溶液中滴加
溶液中滴加 溶液至溶液呈中性,写出反应的离子反应方程式
溶液至溶液呈中性,写出反应的离子反应方程式___________ 。
(2)通过对物质进行分类,能够根据类别通性预测物质的性质。
①已知 属于酸性氧化物,则
属于酸性氧化物,则 与NaOH溶液反应的化学方程式为
与NaOH溶液反应的化学方程式为___________ 。
②亚磷酸( )是二元弱酸,它与足量NaOH溶液充分反应后生成的盐为
)是二元弱酸,它与足量NaOH溶液充分反应后生成的盐为___________ (填化学式)
③已知:硼酸( )是一元弱酸,与足量的NaOH溶液反应生成钠盐化学式为
)是一元弱酸,与足量的NaOH溶液反应生成钠盐化学式为 ,则硼酸在水中的电离方程式是
,则硼酸在水中的电离方程式是___________ 。
(1)现有下列物质:①铜②
 ③熔融的
③熔融的 ④
④ ⑤酒精⑥氨水⑦稀硫酸⑧
⑤酒精⑥氨水⑦稀硫酸⑧ ⑨
⑨ 溶液⑩
溶液⑩ 胶体
胶体①以上物质中,属于电解质且能导电的是
②写出⑨的电离方程式
③写出实验室制备⑩的化学方程式
④向
 溶液中滴加
溶液中滴加 溶液至溶液呈中性,写出反应的离子反应方程式
溶液至溶液呈中性,写出反应的离子反应方程式(2)通过对物质进行分类,能够根据类别通性预测物质的性质。
①已知
 属于酸性氧化物,则
属于酸性氧化物,则 与NaOH溶液反应的化学方程式为
与NaOH溶液反应的化学方程式为②亚磷酸(
 )是二元弱酸,它与足量NaOH溶液充分反应后生成的盐为
)是二元弱酸,它与足量NaOH溶液充分反应后生成的盐为③已知:硼酸(
 )是一元弱酸,与足量的NaOH溶液反应生成钠盐化学式为
)是一元弱酸,与足量的NaOH溶液反应生成钠盐化学式为 ,则硼酸在水中的电离方程式是
,则硼酸在水中的电离方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某小组在实验室探究Ba(OH)2溶液与稀硫酸反应的实质。向 Ba(OH)2溶液中滴加稀硫酸,测定导电率的变化如图所示,回答下列问题:

(1)从分类角度分析,Ba(OH)2在水中以离子形式存在的依据是___________ ;Ba(OH)2的电离方程式为__________________________ 。
(2)A-B段发生反应的离子方程式为_______________________________ 。
(3)B点之后,导电率曲线上升的原因是____________________ 。
(4)书写下列两种情况的离子方程式。
①向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至 恰好完全沉淀:
恰好完全沉淀:_____________________________
②向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性:___________________________________

(1)从分类角度分析,Ba(OH)2在水中以离子形式存在的依据是
(2)A-B段发生反应的离子方程式为
(3)B点之后,导电率曲线上升的原因是
(4)书写下列两种情况的离子方程式。
①向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至
 恰好完全沉淀:
恰好完全沉淀:②向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I. 今有12种物质:①A1 ②稀硝酸 ③H2SO4 ④液氨 ⑤CO2 ⑥空气 ⑦NaCl CaCO3 NaHCO3 酒精 Al2O3
Al2O3  石墨。以上物质中属于电解质但熔融状态下并不导电的是
石墨。以上物质中属于电解质但熔融状态下并不导电的是____________ (填序号,下同),属于非电解质的是___________ 。
II.按要求填写化学用语:
(1)Na2SO4的电离方程式:_______________________ ;
(2)Ba(OH)2与CuSO4两稀溶液混合的离子方程式:______________________ ;
(3)写一个能用Fe3++30H-═Fe(OH)3表示的化学方程式:______________________ 。
 Al2O3
Al2O3  石墨。以上物质中属于电解质但熔融状态下并不导电的是
石墨。以上物质中属于电解质但熔融状态下并不导电的是II.按要求填写化学用语:
(1)Na2SO4的电离方程式:
(2)Ba(OH)2与CuSO4两稀溶液混合的离子方程式:
(3)写一个能用Fe3++30H-═Fe(OH)3表示的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ、掌握电解质和非电解质的概念,能熟练判断一种物质是否是电解质,是认识电解质的性质的前提:以下有①~⑩种物质:①石墨②液氯③氨水④ ⑤
⑤ ⑥
⑥ ⑦红褐色的氢氧化铁胶体⑧稀硫酸⑨熔融
⑦红褐色的氢氧化铁胶体⑧稀硫酸⑨熔融 ⑩蔗糖
⑩蔗糖
(1)上述物质属于电解质的是___________ ;(填序号,多写不给分,下同)属于非电解质的是___________ 。
(2)下列制备⑦的操作方法正确的是___________。(填字母)
(3)向盛有⑦的烧杯中还滴加入盐酸至过量,会出现一系列变化,现象为:___________ 。
(4)写出⑥溶液中加入⑨溶液至 完全沉淀的离子反应方程式
完全沉淀的离子反应方程式___________ 。
Ⅱ、高铁酸钠 是一种新型的净水剂,可以通过下述反应制取(未配平):
是一种新型的净水剂,可以通过下述反应制取(未配平):
(5)配平下面方程式并用单线桥标出电子转移情况:___________ 。
 。
。
 ⑤
⑤ ⑥
⑥ ⑦红褐色的氢氧化铁胶体⑧稀硫酸⑨熔融
⑦红褐色的氢氧化铁胶体⑧稀硫酸⑨熔融 ⑩蔗糖
⑩蔗糖(1)上述物质属于电解质的是
(2)下列制备⑦的操作方法正确的是___________。(填字母)
| A.向饱和氯化铁溶液中滴加适量的氢氧化钠稀溶液 |
| B.加热煮沸氯化铁饱和溶液 |
| C.在氨水中滴加氯化铁浓溶液 |
| D.在沸水中滴加饱和氯化铁溶液,煮沸至出现红褐色液体 |
(4)写出⑥溶液中加入⑨溶液至
 完全沉淀的离子反应方程式
完全沉淀的离子反应方程式Ⅱ、高铁酸钠
 是一种新型的净水剂,可以通过下述反应制取(未配平):
是一种新型的净水剂,可以通过下述反应制取(未配平):(5)配平下面方程式并用单线桥标出电子转移情况:
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有如下物质:①Na;②NaOH溶液;③ 固体;④
固体;④ ;⑤酒精(
;⑤酒精( );⑥蒸馏水;⑦
);⑥蒸馏水;⑦ 溶液;⑧
溶液;⑧ 晶体。
晶体。
(1)以上物质中,属于电解质的是_______ (填序号,右同),属于非电解质的是_______ 。
(2)将②与⑦进行混合,该过程中发生反应的离子方程式是_______ 。
(3)向氢氧化钡溶液中加入物质③的溶液至 恰好沉淀完全,其离子方程式为
恰好沉淀完全,其离子方程式为_______ 。
(4)向100mL②溶液中通入一定量的④,然后向该溶液中逐滴加入2 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示:
的体积(标准状况)关系如图所示:
①0A段发生反应的离子方程式为_______ 。
②m=_______ mL。
③原②溶液的物质的量浓度为_______ 。
(5)将0.1mol⑤在足量氧气中充分燃烧,再将全部产物缓慢通过足量的 固体,
固体, 固体质量增加
固体质量增加______ g。
 固体;④
固体;④ ;⑤酒精(
;⑤酒精( );⑥蒸馏水;⑦
);⑥蒸馏水;⑦ 溶液;⑧
溶液;⑧ 晶体。
晶体。(1)以上物质中,属于电解质的是
(2)将②与⑦进行混合,该过程中发生反应的离子方程式是
(3)向氢氧化钡溶液中加入物质③的溶液至
 恰好沉淀完全,其离子方程式为
恰好沉淀完全,其离子方程式为(4)向100mL②溶液中通入一定量的④,然后向该溶液中逐滴加入2
 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示:
的体积(标准状况)关系如图所示:
①0A段发生反应的离子方程式为
②m=
③原②溶液的物质的量浓度为
(5)将0.1mol⑤在足量氧气中充分燃烧,再将全部产物缓慢通过足量的
 固体,
固体, 固体质量增加
固体质量增加
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,无二次污染。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
回答下列问题:
(1)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①该反应中还原剂是___ 。每生成1molO2,该反应转移___ mol电子。
②K2FeO4在水处理过程中所起的作用是___ 。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:___ 。
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),其原因是___ 。
回答下列问题:
(1)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①该反应中还原剂是
②K2FeO4在水处理过程中所起的作用是
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】研究电解质在水溶液中的离子反应与平衡有重要的意义。
(1)常温下,用 溶液滴定
溶液滴定 溶液的滴定曲线如下图所示。
溶液的滴定曲线如下图所示。
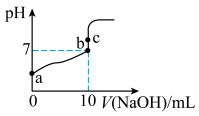
①a点溶液的 pH___________ 1(填“>”、“<”或“=”),请用化学用语解释其原因___________ 。
② b 点溶液中的溶质为___________ (填化学式)。
③c点溶液中,
___________ 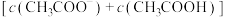 。c点
。c点
___________  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
④a、b、c三点中,水的电离程度最大的点为___________ 。
(2)用电位滴定法模拟测定某醋酸溶液样品中醋酸的含量,操作如下:
已知:该条件下,醋酸和 以物质的量1:1反应时得到的溶液
以物质的量1:1反应时得到的溶液 为8.7。
为8.7。
i.准确量取 醋酸溶液样品,加入蒸馏水至总体积为
醋酸溶液样品,加入蒸馏水至总体积为 ,取其中
,取其中 进行滴定实验,用酸度计检测
进行滴定实验,用酸度计检测 变化;
变化;
ii.逐滴滴入 的
的 溶液,酸度计显示
溶液,酸度计显示 停止滴定,记录消耗的
停止滴定,记录消耗的 溶液的体积V(NaOH);
溶液的体积V(NaOH);
iii.平行测定多次(数据见表1);
iv.分析处理数据。
表1实验数据记录表格
①在滴定过程中,在滴定过程中,若出现下列情况,测定结果偏低的是___________ 。
A.滴定前用待滴定的醋酸溶液润洗锥形瓶
B.在振荡锥形瓶时不慎将瓶内溶液浅出
C.若在滴定过程中不慎将数滴碱液滴锥形瓶外
D.用蒸馏水洗涤碱式滴定管后即使用,没有用碱液润洗
②根据表1中的有效数据,计算消耗的 溶液的平均体积V(NaOH)=
溶液的平均体积V(NaOH)=___________  。该醋酸溶液样品中醋酸的含量是
。该醋酸溶液样品中醋酸的含量是___________  。
。
(3)已知:25℃时 、
、 和
和 的电离平衡常数:
的电离平衡常数:
① 的电离平衡常数表达式
的电离平衡常数表达式
___________ 。
②25℃时,浓度均为 的
的 溶液、
溶液、 溶液、
溶液、 溶液的碱性由大到小的排序是
溶液的碱性由大到小的排序是___________ 。
③25℃时,若初始时次氯酸溶液中 的物质的量浓度为
的物质的量浓度为 ,达到电离平衡时溶液中
,达到电离平衡时溶液中
___________  。
。
④下列化学反应可能发生的是___________ 。
A.
B.
C.
D.
(1)常温下,用
 溶液滴定
溶液滴定 溶液的滴定曲线如下图所示。
溶液的滴定曲线如下图所示。
①a点溶液的 pH
② b 点溶液中的溶质为
③c点溶液中,

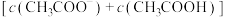 。c点
。c点
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)④a、b、c三点中,水的电离程度最大的点为
(2)用电位滴定法模拟测定某醋酸溶液样品中醋酸的含量,操作如下:
已知:该条件下,醋酸和
 以物质的量1:1反应时得到的溶液
以物质的量1:1反应时得到的溶液 为8.7。
为8.7。i.准确量取
 醋酸溶液样品,加入蒸馏水至总体积为
醋酸溶液样品,加入蒸馏水至总体积为 ,取其中
,取其中 进行滴定实验,用酸度计检测
进行滴定实验,用酸度计检测 变化;
变化;ii.逐滴滴入
 的
的 溶液,酸度计显示
溶液,酸度计显示 停止滴定,记录消耗的
停止滴定,记录消耗的 溶液的体积V(NaOH);
溶液的体积V(NaOH);iii.平行测定多次(数据见表1);
iv.分析处理数据。
表1实验数据记录表格
| 编号 | 1 | 2 | 3 |
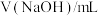 | 23.99 | 24.01 | 24.00 |
A.滴定前用待滴定的醋酸溶液润洗锥形瓶
B.在振荡锥形瓶时不慎将瓶内溶液浅出
C.若在滴定过程中不慎将数滴碱液滴锥形瓶外
D.用蒸馏水洗涤碱式滴定管后即使用,没有用碱液润洗
②根据表1中的有效数据,计算消耗的
 溶液的平均体积V(NaOH)=
溶液的平均体积V(NaOH)= 。该醋酸溶液样品中醋酸的含量是
。该醋酸溶液样品中醋酸的含量是 。
。
(3)已知:25℃时
 、
、 和
和 的电离平衡常数:
的电离平衡常数:| 化学式 |  |  |  |
电离平衡常数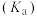 |  |   |  |
 的电离平衡常数表达式
的电离平衡常数表达式
②25℃时,浓度均为
 的
的 溶液、
溶液、 溶液、
溶液、 溶液的碱性由大到小的排序是
溶液的碱性由大到小的排序是③25℃时,若初始时次氯酸溶液中
 的物质的量浓度为
的物质的量浓度为 ,达到电离平衡时溶液中
,达到电离平衡时溶液中
 。
。④下列化学反应可能发生的是
A.

B.

C.

D.

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.利用下列五种有机物回答问题:
① ②
② ③聚丙烯 ④
③聚丙烯 ④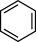 ⑤
⑤
(1)能使溴的四氯化碳溶液褪色的是_______ (序号);
(2)既能发生取代反应又能发生加成反应的是_______ (序号);
(3)⑤的名称为_______ (系统命名法);
(4)②的一种同分异构体,核磁共振氢谱表明其只有一种化学环境的氢,则该化合物的结构简式为:_______ 。
Ⅱ.运用电离及盐类水解知识回答下列问题:
(5)由 晶体得到纯的无水
晶体得到纯的无水 的合理方法是
的合理方法是_______ 。
(6)常温下, 的盐酸中
的盐酸中 和
和 氯化铵中
氯化铵中 的比值为
的比值为_______ 。
①
 ②
② ③聚丙烯 ④
③聚丙烯 ④ ⑤
⑤
(1)能使溴的四氯化碳溶液褪色的是
(2)既能发生取代反应又能发生加成反应的是
(3)⑤的名称为
(4)②的一种同分异构体,核磁共振氢谱表明其只有一种化学环境的氢,则该化合物的结构简式为:
Ⅱ.运用电离及盐类水解知识回答下列问题:
(5)由
 晶体得到纯的无水
晶体得到纯的无水 的合理方法是
的合理方法是(6)常温下,
 的盐酸中
的盐酸中 和
和 氯化铵中
氯化铵中 的比值为
的比值为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)常温下,有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、盐酸和NaNO3溶液中的一种。已知A、B溶液中水的电离程度相同,A、C溶液的pH相同。则B是_____________ ,C是_____________ 。
(2)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种:
a. c(Cl-)>c(NH4+)>c(H+)>c(OH-) b. c(Cl-)>c(NH4+)>c(OH-)>c(H+)
c. c(NH4+)>c(Cl-)>c(OH-)>c(H+) d. c(Cl-)>c(H+)>c(NH4+)>c(OH-)
则:
①上述关系一定不正确的是____________ 填序号)。
②溶液中只有一种溶质,则该溶液中离子浓度的大小关系为____________ 填序号)。
③若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显______________________ (填“酸性”“碱性”或“中性”)。
(2)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种:
a. c(Cl-)>c(NH4+)>c(H+)>c(OH-) b. c(Cl-)>c(NH4+)>c(OH-)>c(H+)
c. c(NH4+)>c(Cl-)>c(OH-)>c(H+) d. c(Cl-)>c(H+)>c(NH4+)>c(OH-)
则:
①上述关系一定不正确的是
②溶液中只有一种溶质,则该溶液中离子浓度的大小关系为
③若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A=H++HA-,HA- H++A2-。据此回答下列问题。
H++A2-。据此回答下列问题。
(1)Na2A溶液显______ (选填“酸性”、“碱性”、“中性”或“无法确定”)。
(2)在0.1mol/L的Na2A溶液中,下列粒子浓度关系式正确的是______ 。
(3)室温下,pH=10的氨水与pH=4的NH4C1溶液中,由水电离出的c(H+)之比为______ 。
(4)①NH4Al(SO4)2可作净水剂,其理由是______ 。(用必要的化学用语和相关文字说明)。
②相同条件下,0.1mol·L-1NH4Al(SO4)2溶液中c(NH )
)______ (填“等于”“大于”或“小于”)0.1mol·L-1NH4HSO4溶液中c(NH )。
)。
(5)已知Ksp(BaCO3)=2.6×l0-9,Ksp(BaSO4)=1.1×10-10。
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为____ mol/L。
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中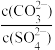 =
=______ (保留三位有效数字)。
 H++A2-。据此回答下列问题。
H++A2-。据此回答下列问题。(1)Na2A溶液显
(2)在0.1mol/L的Na2A溶液中,下列粒子浓度关系式正确的是
| A.0.1mol/L=c(HA-)+c(A2-)+c(H2A) |
| B.c(Na+)+c(OH-)=c(HA-)+c(H+) |
| C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) |
| D.c(Na+)=2c(HA-)+2c(A2-) |
(4)①NH4Al(SO4)2可作净水剂,其理由是
②相同条件下,0.1mol·L-1NH4Al(SO4)2溶液中c(NH
 )
) )。
)。(5)已知Ksp(BaCO3)=2.6×l0-9,Ksp(BaSO4)=1.1×10-10。
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中
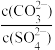 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)在25℃条件下将pH=12的氨水稀释过程中,下列说法正确的是___ 。
A.能使溶液中c(NH4+)·c(OH-)增大
B.溶液中c(H+)·c(OH-)不变
C.能使溶液中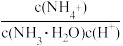 比值增大
比值增大
D.此过程中Kw增大
(2)25℃时,向0.1mol·L-1的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是____ (填序号)。
①氨水与氯化铵发生化学反应
②氯化铵溶液水解显酸性,增加了c(H+)
③氯化铵溶于水,电离出大量铵离子,抑制了一水合氨的电离,使c(OH-)减小
(3)室温下,如果将0.2molNH4Cl和0.1molNaOH全部溶于水,形成混合溶液(假设无损失)。
①___ 和___ 两种粒子的物质的量之和等于0.2mol。
②____ 和___ 两种粒子的物质的量之和比OH-多0.1mol。
A.能使溶液中c(NH4+)·c(OH-)增大
B.溶液中c(H+)·c(OH-)不变
C.能使溶液中
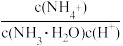 比值增大
比值增大D.此过程中Kw增大
(2)25℃时,向0.1mol·L-1的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是
①氨水与氯化铵发生化学反应
②氯化铵溶液水解显酸性,增加了c(H+)
③氯化铵溶于水,电离出大量铵离子,抑制了一水合氨的电离,使c(OH-)减小
(3)室温下,如果将0.2molNH4Cl和0.1molNaOH全部溶于水,形成混合溶液(假设无损失)。
①
②
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】硫及其化合物在生产、生活中具有广泛的用途,根据所学知识,回答下列问题。
已知:常温下K(NH3·H2O)=1.6×10-5,lg2=0.3。
(1)(NH4)2SO4溶液可用来除铁锈,其原因是_______ (用离子方程式表示)。
(2)常温下,0.1mol·L-1的(NH4)2SO4溶液的pH=_______ ,由水电离出的c(H+)=_______ mol·L-1。
(3)常温下,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1的NaOH溶液,得到溶液的pH与NaOH溶液的体积的关系如图所示(忽略溶液混合时体积的变化)。
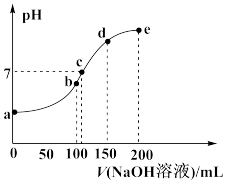
①a点时,溶液中各离子的浓度由大到小的顺序为_______ (用离子符号表示)。
②c点时,c(NH )+c(Na+)
)+c(Na+)_______ (填“>”“<”或“=”)c(SO )。
)。
③d点时, =
=_______ 。
已知:常温下K(NH3·H2O)=1.6×10-5,lg2=0.3。
(1)(NH4)2SO4溶液可用来除铁锈,其原因是
(2)常温下,0.1mol·L-1的(NH4)2SO4溶液的pH=
(3)常温下,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1的NaOH溶液,得到溶液的pH与NaOH溶液的体积的关系如图所示(忽略溶液混合时体积的变化)。

①a点时,溶液中各离子的浓度由大到小的顺序为
②c点时,c(NH
 )+c(Na+)
)+c(Na+) )。
)。③d点时,
 =
=
您最近一年使用:0次



