三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业的关键原料之一,可由氨气和氟气反应得到:_______NH3+_______F2→_______NF3+_______NH4F。完成下列填空:
(1)配平上述反应方程式_______ 。
(2)F原子的结构示意图是_______ ,其能量最高的电子所占据的电子亚层符号为_______ 。从原子结构角度比较F和N元素的非金属性强弱_______ 。
(3)写出NH4F的电子式_______ ,溶液中NH 的检验方法是
的检验方法是_______ 。
(4)与NH 具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是
具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是_______ ,该产物的水溶液呈_______ 性,用适当的化学用语解释该溶液酸碱性的原因:_______ 。其稀溶液中存在关系式:c(OH-)-c(H+) =c(HCO ) +
) + _______
(1)配平上述反应方程式
(2)F原子的结构示意图是
(3)写出NH4F的电子式
 的检验方法是
的检验方法是(4)与NH
 具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是
具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是 ) +
) +
2022·上海奉贤·一模 查看更多[1]
更新时间:2021-12-24 16:46:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】元素周期表中第VIIA族元素的单质及其化合物的用途广泛。
(1)第VIIA族原子半径最小的元素的原子结构示意图为_______ 。
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是_______ (填序号)。
a.Cl2、Br2、I2的沸点 b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的稳定性 d.HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体
①完成I中反应的总化学方程式:_______ ;
②II中转化的基本反应类型是_______ ,该反应过程能析出KClO3晶体而无其它晶体析出的主要原因是_______ 。
(4)一定条件,在水溶液中1molCl-、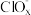 (x=1,2,3,4)的能量(kJ·mol-1)相对大小如图所示。
(x=1,2,3,4)的能量(kJ·mol-1)相对大小如图所示。
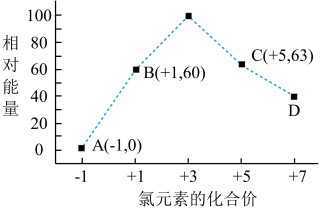
①上图中最不稳定的离子对应的酸是_______ (填写名称)。
②B→A+C反应的能量变化为_______ kJ·mol-1。
(1)第VIIA族原子半径最小的元素的原子结构示意图为
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是
a.Cl2、Br2、I2的沸点 b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的稳定性 d.HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液
 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体①完成I中反应的总化学方程式:
②II中转化的基本反应类型是
(4)一定条件,在水溶液中1molCl-、
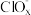 (x=1,2,3,4)的能量(kJ·mol-1)相对大小如图所示。
(x=1,2,3,4)的能量(kJ·mol-1)相对大小如图所示。
①上图中最不稳定的离子对应的酸是
②B→A+C反应的能量变化为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】表格为门捷列夫元素周期表的一部分,其中的编号代表对应的元素。用元素符号回答下列问题:
(1)基态F原子有___________ 种运动状态的电子。
(2)元素③⑪电负性较大的是___________ ﹔Se的原子结构示意图为___________ 。
(3)元素铬的基态原子的价电子排布式为:___________ 。
(4)Cu基态原子中,能量最高的电子占据的原子轨道的形状为___________ 。
(5)该表格中电负性最大的元素与第一电离能最小的元素形成的化合物的电子式为___________ 。
(6)②③的简单气态氢化物中较稳定的是___________ (填化学式),元素⑥⑦的最高价氧化物的水化物相互反应的离子方程式为___________ 。

(1)基态F原子有
(2)元素③⑪电负性较大的是
(3)元素铬的基态原子的价电子排布式为:
(4)Cu基态原子中,能量最高的电子占据的原子轨道的形状为
(5)该表格中电负性最大的元素与第一电离能最小的元素形成的化合物的电子式为
(6)②③的简单气态氢化物中较稳定的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图是________ 。
(2)已知某粒子的结构示意图为
试回答:
①当x-y=10时,该粒子为________ (填“原子”、“阳离子”或“阴离子”)。
②当y=8时,粒子可能为(填名称)________ 、________ 、________ 、________ 、________ 。
③写出y=3与y=7的元素最高价氧化物对应水化物发生反应的离子方程式__________________________ 。
(2)已知某粒子的结构示意图为

试回答:
①当x-y=10时,该粒子为
②当y=8时,粒子可能为(填名称)
③写出y=3与y=7的元素最高价氧化物对应水化物发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据以下反应:
KMnO4+ Na2SO3+ H2SO4= MnSO4+ Na2SO4+ K2SO4+ H2O
回答下列问题:
I.请配平该反应方程式___ ,该反应还原剂是___ ,还原产物是___ 。
II.当反应转移1mol电子时,被氧化的物质的质量为___ g。
Ⅲ.用单线桥法标出反应中电子转移的方向和数目___ 。
KMnO4+ Na2SO3+ H2SO4= MnSO4+ Na2SO4+ K2SO4+ H2O
回答下列问题:
I.请配平该反应方程式
II.当反应转移1mol电子时,被氧化的物质的质量为
Ⅲ.用单线桥法标出反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】双氧水是常见的氧化剂、消毒剂,一种制取双氧水的流程如下:
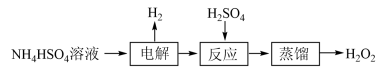
(1)“电解”后生成(NH4)2S2O8,该反应的化学方程式为______ 。
(2)“反应”中部分物质的浓度变化如图所示,该反应的离子方程式为______ 。

(3)双氧水中H2O2的含量可以用酸性KMnO4溶液来测定,测定时MnO 被还原成Mn2+,测定反应的离子方程式为
被还原成Mn2+,测定反应的离子方程式为______ 。
(4)pH=6时,(NH4)2S2O8溶液与足量MnSO4反应有MnO2沉淀生成,过滤后所得滤液中含硫微粒均为SO42-,该反应的离子方程式为______ 。

(1)“电解”后生成(NH4)2S2O8,该反应的化学方程式为
(2)“反应”中部分物质的浓度变化如图所示,该反应的离子方程式为

(3)双氧水中H2O2的含量可以用酸性KMnO4溶液来测定,测定时MnO
 被还原成Mn2+,测定反应的离子方程式为
被还原成Mn2+,测定反应的离子方程式为(4)pH=6时,(NH4)2S2O8溶液与足量MnSO4反应有MnO2沉淀生成,过滤后所得滤液中含硫微粒均为SO42-,该反应的离子方程式为
您最近一年使用:0次
【推荐3】I.某一在水溶液中进行的反应体系中,有反应物和生成物共六种物质,这六种物质是: HCl(浓)、KMnO4、MnCl2、H2O、Cl2、 KCl,已知Cl2、KCl 为生成物。
(1)该反应中的氧化剂是_______ (写化学式),氧化产物为____ (写化学式),该反应中,氧化产物与还原产物的物质的量之比为__________
(2) 写出该反应的离子方程式:________________
(3) 用单线桥表示该反应电子转移的方向和数目。______________
(4)HCl 在上述反应中体现出米的性质是___________
(5)用该反应制得了标况下560mLCl2,则被氧化的物质为_____ mol,转移电子数为______ NA(NA表示阿伏伽德罗常数的值)。
Ⅱ.高锰酸钾标准溶液经常用来滴定测量物质的含量。用高锰酸钾法闻接测定石灰石中CaCO3的含量的方法为: 称取试样0.1250g,用稀盐酸溶解后加入(NH4)2C2O4得CaC2O4沉淀。沉淀经过滤洗涤后溶于稀硫酸中。滴定生成的H2C2O4 用去浓度为0.0 16mo/LKMnO4 溶液25.00mL。
(1)写出CaC2O4沉淀溶解的离子方程式:___________________
(2)配平并完成下列高锰酸钾滴定草酸反应的离子方程式:_____________
口MnO4-+ 口H2C2O4+H+=口Mn2++口CO2↑+口
(3)①石灰石中CaCO3的百分含量:_______
②滴定反应中产生的标准状况下的CO2气体为_____ mL (保留两位小数)。
(1)该反应中的氧化剂是
(2) 写出该反应的离子方程式:
(3) 用单线桥表示该反应电子转移的方向和数目。
(4)HCl 在上述反应中体现出米的性质是
(5)用该反应制得了标况下560mLCl2,则被氧化的物质为
Ⅱ.高锰酸钾标准溶液经常用来滴定测量物质的含量。用高锰酸钾法闻接测定石灰石中CaCO3的含量的方法为: 称取试样0.1250g,用稀盐酸溶解后加入(NH4)2C2O4得CaC2O4沉淀。沉淀经过滤洗涤后溶于稀硫酸中。滴定生成的H2C2O4 用去浓度为0.0 16mo/LKMnO4 溶液25.00mL。
(1)写出CaC2O4沉淀溶解的离子方程式:
(2)配平并完成下列高锰酸钾滴定草酸反应的离子方程式:
口MnO4-+ 口H2C2O4+H+=口Mn2++口CO2↑+口
(3)①石灰石中CaCO3的百分含量:
②滴定反应中产生的标准状况下的CO2气体为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:
H2A H++HA- HA-
H++HA- HA- H++A2-
H++A2-
已知相同浓度时的电离程度α(H2A)> α(HA-),设有下列四种溶液:
(A)0.01mol.L-1的H2A溶液
(B)0.01mol.L-1的NaHA溶液
(C)0.01mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
(D)0.02mol.L-1的NaOH与0.02 mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号)
(1) c(H+)最大的是_________
(2)在0.01mol.L-1的NaHA溶液中2C(A2- )+(C(HA-)+C C(OH-)-C(H+)=_________
(3) 0.02mol.L-1的NaOH与0.02 mol.L-1的NaHA溶液等体积混合显______________ 性原因
(用离子方程式表示)_____________________________________________________
H2A
 H++HA- HA-
H++HA- HA- H++A2-
H++A2-已知相同浓度时的电离程度α(H2A)> α(HA-),设有下列四种溶液:
(A)0.01mol.L-1的H2A溶液
(B)0.01mol.L-1的NaHA溶液
(C)0.01mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
(D)0.02mol.L-1的NaOH与0.02 mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号)
(1) c(H+)最大的是
(2)在0.01mol.L-1的NaHA溶液中2C(A2- )+(C(HA-)+C C(OH-)-C(H+)=
(3) 0.02mol.L-1的NaOH与0.02 mol.L-1的NaHA溶液等体积混合显
(用离子方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,用0.10mol·L-1的氨水滴定 10.00mL0.05 mol·L-1的二元酸 H2Y的溶液,滴定过程中加入氨水的体积(V)与溶液中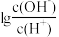 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
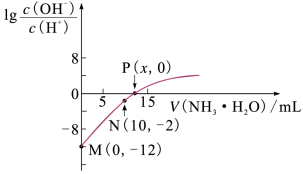
(1)写出H2Y的电离方程式_______
(2)滴定过程中,M、N、P三点对应水电离出的H+浓度由大到小的顺序为_______
(3)用x表示的NH3·H2O电离平衡常数值Kb=_______
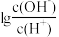 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
(1)写出H2Y的电离方程式
(2)滴定过程中,M、N、P三点对应水电离出的H+浓度由大到小的顺序为
(3)用x表示的NH3·H2O电离平衡常数值Kb=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.请回答下列问题:
(1)向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如图所示:

a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是____ 。
(2)已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
①物质的量浓度均为0.1mol/L的四种溶液:pH由小到大排列的顺序是____ (用编号填写)。
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
②写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:____ 。
(3)已知常温时,amol/L醋酸在水中与0.1mol/LNaOH等体积混合,溶液为中性,则醋酸钠的水解平衡常数Kh=_____ (用含a的代数式表示)。
Ⅱ.结合表格回答下列问题(均为常温下的数据):
(4)0.1mol/L的KHC2O4溶液呈酸性,该溶液中各离子浓度由大到小的顺序为____ 。
(5)pH相同的NaClO和CH3COOK溶液中,[c(Na+)-c(C1O-)]____ [c(K+)-c(CH3COO-)](填“>”、“<”或“=”)。
(6)向0.1mol/LCH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液pH=____ 。(CH3COOH的电离平衡常数Ka=1.8×10-5)
(1)向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如图所示:

a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是
(2)已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
②写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(3)已知常温时,amol/L醋酸在水中与0.1mol/LNaOH等体积混合,溶液为中性,则醋酸钠的水解平衡常数Kh=
Ⅱ.结合表格回答下列问题(均为常温下的数据):
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 | H2C2O4 | K1=5.4×10-2 | H2S | K1=1.3×10-7 |
| HClO | 3×10-8 | K2=4.7×10-11 | K2=5.4×10-5 | K2=7.1×10-15 |
(5)pH相同的NaClO和CH3COOK溶液中,[c(Na+)-c(C1O-)]
(6)向0.1mol/LCH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如图是s能级和p能级的原子轨道图,试回答下列问题:
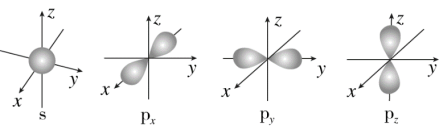
(1)s电子的原子轨道呈_______ 形,每个s能级有_______ 个原子轨道;p电子的原子轨道呈_______ 形,每个p能级有_______ 个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是_______ 电子,其电子云在空间有_______ 方向。
(3)下列原子或离子的电子排布式或轨道表示式正确的是_______ (填序号)
①K+:
②F: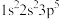
③P: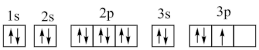
④Cu: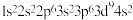
⑤Fe2+: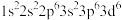
⑥Mg:
⑦O: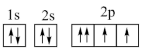

(1)s电子的原子轨道呈
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是
(3)下列原子或离子的电子排布式或轨道表示式正确的是
①K+:

②F:
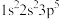
③P:
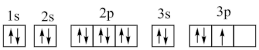
④Cu:
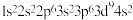
⑤Fe2+:
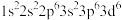
⑥Mg:

⑦O:
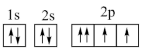
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】我国的四大发明之一黑火药,爆炸时发生反应的化学方程式为:S + 2KNO3 + 3C → K2S + 3CO2↑+ N2↑。请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,数据“39.10”表示的是________ ;钾元素在周期表中的位置为___________________ 。

(2)上述元素中,简单离子电子层结构与氩原子相同,且离子半径最大的元素,其原子核外有_____ 种不同能级的电子;已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是__________________________________ 。
(3)上述反应生成物中,属于非电解质的是_________________ (写结构式);其中熔点最高的物质的电子式是______________ 。
(4)上述化学方程式的元素中,属于同周期元素的非金属性由强到弱的顺序为_______________ ,能证明其递变规律的事实是_______________ (填字母)。
A、最高价氧化物对应水化物的酸性 B、气态氢化物的沸点
C、单质与氢气反应的难易程度 D、其两两组合形成的化合物中元素的化合价
(5)上述反应中,如1.5mol还原剂________ (填“得到”或“失去”)________ mol电子,则生成_________ g还原产物。
(1)如图所示为元素周期表中钾元素框图,数据“39.10”表示的是

(2)上述元素中,简单离子电子层结构与氩原子相同,且离子半径最大的元素,其原子核外有
(3)上述反应生成物中,属于非电解质的是
(4)上述化学方程式的元素中,属于同周期元素的非金属性由强到弱的顺序为
A、最高价氧化物对应水化物的酸性 B、气态氢化物的沸点
C、单质与氢气反应的难易程度 D、其两两组合形成的化合物中元素的化合价
(5)上述反应中,如1.5mol还原剂
您最近一年使用:0次



