如图是s能级和p能级的原子轨道图,试回答下列问题:
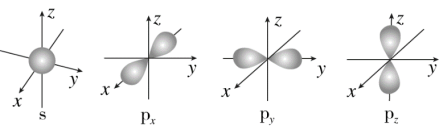
(1)s电子的原子轨道呈_______ 形,每个s能级有_______ 个原子轨道;p电子的原子轨道呈_______ 形,每个p能级有_______ 个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是_______ 电子,其电子云在空间有_______ 方向。
(3)下列原子或离子的电子排布式或轨道表示式正确的是_______ (填序号)
①K+:
②F: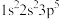
③P: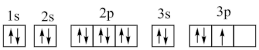
④Cu: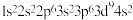
⑤Fe2+: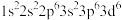
⑥Mg:
⑦O: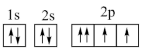

(1)s电子的原子轨道呈
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是
(3)下列原子或离子的电子排布式或轨道表示式正确的是
①K+:

②F:
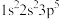
③P:
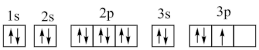
④Cu:
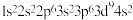
⑤Fe2+:
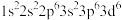
⑥Mg:

⑦O:
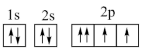
更新时间:2022-10-04 20:01:01
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)玻尔原子结构模型成功地解释了___________ 的实验事实,电子所处的轨道的能量是___________ 的。最大不足之处是___________ 。
(2)p能级上有___________ 个原子轨道,在空间沿___________ 轴对称,记为___________ ,___________ ,___________ ,其能量关系为___________ 。
(2)p能级上有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】依据原子结构知识回答下列问题。
(1)下列有关说法错误的是___________。
(2)基态V原子中具有___________ 种不同能量的电子,具有___________ 种不同空间运动状态的电子,具有___________ 种不同运动状态的电子。
(3)基态Cu原子的简化电子排布式为___________ ,基态Se原子的价电子轨道表示式为___________ ,基态Mn2+的价电子排布式为___________ 。
(1)下列有关说法错误的是___________。
| A.简单离子的还原性:P3->O2->F- |
| B.在元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有两种 |
| C.焰色试验与电子跃迁有关 |
| D.基态铝原子占据的最高能级的电子云轮廓图的形状为球形 |
(3)基态Cu原子的简化电子排布式为
您最近一年使用:0次
【推荐3】依据原子结构知识回答下列问题。
(1)下列有关说法错误的是_______。
(2)基态氟原子的第一电离能_______ 基态氮原子的第一电离能(填大于、小于或等于)的原因是_______ 。
(3)基态Mn2+的价电子排布式为_______ 。
(4)Li2O是离子晶体,其形成过程中的能量变化如图(a)所示。
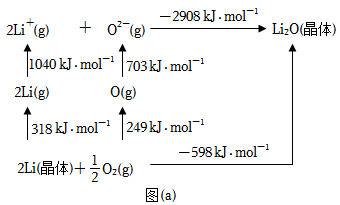
可知,Li原子的第一电离能为_______ kJ·mol-1,O=O键键能为_______ kJ·mol-1。
(1)下列有关说法错误的是_______。
| A.简单离子的还原性: P3->O2->F- |
| B.在元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有两种 |
| C.焰色试验与电子跃迁有关 |
| D.基态铝原子占据的最高能级的电子云轮廓图的形状为球形 |
(3)基态Mn2+的价电子排布式为
(4)Li2O是离子晶体,其形成过程中的能量变化如图(a)所示。
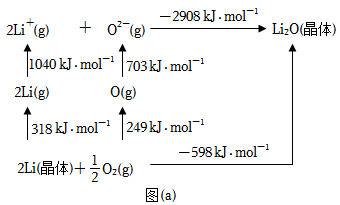
可知,Li原子的第一电离能为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】基态与激发态

(1)基态原子:处于___________ 状态的原子,
(2)基态原子___________ ,电子跃迁到___________ ,变为激发态原子;
(3)电子从较高能量的激发态跃迁到较低能量的激发态乃至基态时,将___________ ;
(4)___________ 是电子跃迁释放能量的重要形式之一。

(1)基态原子:处于
(2)基态原子
(3)电子从较高能量的激发态跃迁到较低能量的激发态乃至基态时,将
(4)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子在不同状态下的电子排布式有以下几种,其中处于激发态且能量较高的是___________ 。(填标号)
a. b.
b. c.
c. d.
d.
(2)①一氯乙烯(C2H3Cl)分子中,C的一个___________ 杂化轨道与Cl的3px轨道形成C-Cl___________ 键,并且Cl的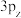 轨道与C的
轨道与C的 轨道形成3中心4电子的大π键
轨道形成3中心4电子的大π键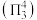 。
。
②一氯乙烷(C2H5Cl)、一氯乙烯(C2H3Cl)、一氯乙炔(C2HCl)分子中,C-Cl键长的顺序是___________ ,理由:(ⅰ)C的杂化轨道中s成分越多,形成的C-Cl键越强;(ⅱ)___________ 。
(1)氟原子在不同状态下的电子排布式有以下几种,其中处于激发态且能量较高的是
a.
 b.
b. c.
c. d.
d.
(2)①一氯乙烯(C2H3Cl)分子中,C的一个
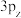 轨道与C的
轨道与C的 轨道形成3中心4电子的大π键
轨道形成3中心4电子的大π键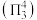 。
。②一氯乙烷(C2H5Cl)、一氯乙烯(C2H3Cl)、一氯乙炔(C2HCl)分子中,C-Cl键长的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种_______ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是_______ (填序号)。
a.1s22s22p43s13p 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p
c.1s22s22p63s13p d.1s22s22p63s2
d.1s22s22p63s2
(3)Ti原子位于元素周期表中的_______ 区,其价电子排布式为_______ 。
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+_______ Fe2+(填“大于”或“小于”)。
(5)下列各组多电子原子的能级能量比较不正确的是_______。
①2p=3p②4s>2s③4p>4f④4d>3d
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.1s22s22p43s13p
 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p
c.1s22s22p63s13p
 d.1s22s22p63s2
d.1s22s22p63s2(3)Ti原子位于元素周期表中的
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+
(5)下列各组多电子原子的能级能量比较不正确的是_______。
①2p=3p②4s>2s③4p>4f④4d>3d
| A.①④ | B.①③ | C.③④ | D.②③ |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I以下是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利不相容原理,哪些违反了洪特规则。
①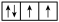 ②
② ③
③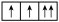 ④
④ ⑤
⑤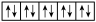
(1)违反泡利不相容原理的有___________
(2)违反洪特规则的有___________ 。
II含氧酸可表示为:(HO)mROn,酸的强度与酸中的非羟基氧原子数n有关,n越大,酸性越强。一般n=0弱酸,n=1中强酸,n=2强酸,n=3超强酸。据实验事实可知:硼酸(H3BO3)是弱酸,亚磷酸是中强酸(H3PO3)。
(3)写出两种酸的结构式:___________ 、___________ 。
(4)写出亚磷酸与过量的NaOH反应的方程式___________ 。
①
 ②
② ③
③ ④
④ ⑤
⑤
(1)违反泡利不相容原理的有
(2)违反洪特规则的有
II含氧酸可表示为:(HO)mROn,酸的强度与酸中的非羟基氧原子数n有关,n越大,酸性越强。一般n=0弱酸,n=1中强酸,n=2强酸,n=3超强酸。据实验事实可知:硼酸(H3BO3)是弱酸,亚磷酸是中强酸(H3PO3)。
(3)写出两种酸的结构式:
(4)写出亚磷酸与过量的NaOH反应的方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】据《科技日报》报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂,在室温条件下以 为氧化剂直接将
为氧化剂直接将 氧化成C的含氧化合物。请回答下列问题:
氧化成C的含氧化合物。请回答下列问题:
(1)在Mn、Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”,该基态原子的价电子排布式为___________ 。
(2)在第4周期过渡金属元素中,基态原子未成对电子数最多的元素是___________ (填元素符号)。
(3)石墨烯限域单原子铁能活化分子 中的C-H键,导致C与H之间的作用力
中的C-H键,导致C与H之间的作用力___________ (填“减弱”或“不变”)。
(4)常温下,在催化剂作用下, 氧化
氧化 生成
生成 、HCHO、HCOOH等。
、HCHO、HCOOH等。
①它们的沸点由高到低的顺序为HCOOH> >HCHO,其主要原因是
>HCHO,其主要原因是___________ 。
② 和HCHO比较,键角较大的是
和HCHO比较,键角较大的是___________ ,主要原因是___________ 。
 为氧化剂直接将
为氧化剂直接将 氧化成C的含氧化合物。请回答下列问题:
氧化成C的含氧化合物。请回答下列问题:(1)在Mn、Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”,该基态原子的价电子排布式为
(2)在第4周期过渡金属元素中,基态原子未成对电子数最多的元素是
(3)石墨烯限域单原子铁能活化分子
 中的C-H键,导致C与H之间的作用力
中的C-H键,导致C与H之间的作用力(4)常温下,在催化剂作用下,
 氧化
氧化 生成
生成 、HCHO、HCOOH等。
、HCHO、HCOOH等。①它们的沸点由高到低的顺序为HCOOH>
 >HCHO,其主要原因是
>HCHO,其主要原因是②
 和HCHO比较,键角较大的是
和HCHO比较,键角较大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在原子结构理论中,有四个原理,分别是①构造原理,②泡利原理,③洪特规则,④能量最低原理。在以下的现象中主要决定的因素是(填序号,各只填一项)。
(1)各能级最多容纳的电子数是该能级原子轨道数的2倍_______ 。
(2)碳原子的核外电子排布基态时是1s22s22p2而不是1s22s12p3_______ 。
(3)最外层电子数不会超过8个,次外层电子数不会超过18个_______ 。
(4)铬(24Cr)的电子排布式是1s22s22p63s23p63d54s1而不是1s22s22p63s23p63d44s2_______ 。
(5)在磷原子的基态原子结构中,有3个未成对的单电子_______ 。
(6)第四周期元素中,4p轨道半充满的是_______ ,3d轨道半充满的是_______ ,4s轨道半充满的是_______ 。(填元素符号)
(1)各能级最多容纳的电子数是该能级原子轨道数的2倍
(2)碳原子的核外电子排布基态时是1s22s22p2而不是1s22s12p3
(3)最外层电子数不会超过8个,次外层电子数不会超过18个
(4)铬(24Cr)的电子排布式是1s22s22p63s23p63d54s1而不是1s22s22p63s23p63d44s2
(5)在磷原子的基态原子结构中,有3个未成对的单电子
(6)第四周期元素中,4p轨道半充满的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】据《科技日报》报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂,在室温条件下以 为氧化剂直接将
为氧化剂直接将 氧化成C的含氧化合物。请回答下列问题:
氧化成C的含氧化合物。请回答下列问题:
(1)在Mn、Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”,该基态原子的价电子排布式为___________ 。
(2)在第4周期过渡金属元素中,基态原子未成对电子数最多的元素是___________ (填元素符号)。
(3)石墨烯限域单原子铁能活化分子 中的C-H键,导致C与H之间的作用力
中的C-H键,导致C与H之间的作用力___________ (填“减弱”或“不变”)。
(4)常温下,在催化剂作用下, 氧化
氧化 生成
生成 、HCHO、HCOOH等。
、HCHO、HCOOH等。
①它们的沸点由高到低的顺序为HCOOH> >HCHO,其主要原因是
>HCHO,其主要原因是___________ 。
② 和HCHO比较,键角较大的是
和HCHO比较,键角较大的是___________ ,主要原因是___________ 。
 为氧化剂直接将
为氧化剂直接将 氧化成C的含氧化合物。请回答下列问题:
氧化成C的含氧化合物。请回答下列问题:(1)在Mn、Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”,该基态原子的价电子排布式为
(2)在第4周期过渡金属元素中,基态原子未成对电子数最多的元素是
(3)石墨烯限域单原子铁能活化分子
 中的C-H键,导致C与H之间的作用力
中的C-H键,导致C与H之间的作用力(4)常温下,在催化剂作用下,
 氧化
氧化 生成
生成 、HCHO、HCOOH等。
、HCHO、HCOOH等。①它们的沸点由高到低的顺序为HCOOH>
 >HCHO,其主要原因是
>HCHO,其主要原因是②
 和HCHO比较,键角较大的是
和HCHO比较,键角较大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】原子结构与元素周期表存在着内在联系。根据已学知识,请回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:第________ 周期第________ 族。
(2)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:____________ 。
(3)写出3p轨道上只有2个未成对电子的元素的符号:____________ 、____________ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:第
(2)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:
(3)写出3p轨道上只有2个未成对电子的元素的符号:
您最近一年使用:0次



