卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子在不同状态下的电子排布式有以下几种,其中处于激发态且能量较高的是___________ 。(填标号)
a. b.
b. c.
c. d.
d.
(2)①一氯乙烯(C2H3Cl)分子中,C的一个___________ 杂化轨道与Cl的3px轨道形成C-Cl___________ 键,并且Cl的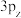 轨道与C的
轨道与C的 轨道形成3中心4电子的大π键
轨道形成3中心4电子的大π键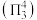 。
。
②一氯乙烷(C2H5Cl)、一氯乙烯(C2H3Cl)、一氯乙炔(C2HCl)分子中,C-Cl键长的顺序是___________ ,理由:(ⅰ)C的杂化轨道中s成分越多,形成的C-Cl键越强;(ⅱ)___________ 。
(1)氟原子在不同状态下的电子排布式有以下几种,其中处于激发态且能量较高的是
a.
 b.
b. c.
c. d.
d.
(2)①一氯乙烯(C2H3Cl)分子中,C的一个
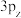 轨道与C的
轨道与C的 轨道形成3中心4电子的大π键
轨道形成3中心4电子的大π键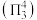 。
。②一氯乙烷(C2H5Cl)、一氯乙烯(C2H3Cl)、一氯乙炔(C2HCl)分子中,C-Cl键长的顺序是
更新时间:2024-05-05 17:11:52
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】新工艺采用金属氧化物 催化尿素与甲醇合成碳酸二甲酯
催化尿素与甲醇合成碳酸二甲酯 ,副产物氨气回收重新生成尿素,有关的方程式如下:
,副产物氨气回收重新生成尿素,有关的方程式如下:
反应①: +2CH3OH(g)
+2CH3OH(g)
 +2NH3(g)
+2NH3(g)
反应②:2NH3(g)+CO2(g)
 +H2O(l)
+H2O(l)
完成下列填空:
(1)C原子核外能量最高的电子有______ 个,比较 、N、O简单离子的半径大小
、N、O简单离子的半径大小__________ 。
(2)下列事实能说明氮的非金属性比碳强的是______ (选填编号)。
a.酸性: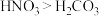 b.最高正价:氮>碳
b.最高正价:氮>碳
c.沸点: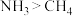 d.吸引电子能力强弱:氮>碳
d.吸引电子能力强弱:氮>碳
(3)达到平衡时,反应①碳酸二甲酯的产率 随温度T的变化关系如图所示,则反应是
随温度T的变化关系如图所示,则反应是__________ 反应(选填“放热”或“吸热”),
______  (选填“>”或“<”)。
(选填“>”或“<”)。

(4)某一恒温恒容 装置内,
装置内, 与
与 发生反应②,
发生反应②,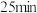 后,气体的密度减少
后,气体的密度减少 ,则
,则 内氨气的平均反应速率为
内氨气的平均反应速率为__________ 。
(5)传统合成DMC的方法是以光气( ,有剧毒)和甲醇为原料,请写出相应的化学方程式
,有剧毒)和甲醇为原料,请写出相应的化学方程式__________ 。
(6)新工艺合成DMC的方法和传统方法相比,优点有__________ (任写两点)。
 催化尿素与甲醇合成碳酸二甲酯
催化尿素与甲醇合成碳酸二甲酯 ,副产物氨气回收重新生成尿素,有关的方程式如下:
,副产物氨气回收重新生成尿素,有关的方程式如下:反应①:
 +2CH3OH(g)
+2CH3OH(g)
 +2NH3(g)
+2NH3(g)反应②:2NH3(g)+CO2(g)

 +H2O(l)
+H2O(l)完成下列填空:
(1)C原子核外能量最高的电子有
 、N、O简单离子的半径大小
、N、O简单离子的半径大小(2)下列事实能说明氮的非金属性比碳强的是
a.酸性:
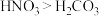 b.最高正价:氮>碳
b.最高正价:氮>碳c.沸点:
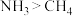 d.吸引电子能力强弱:氮>碳
d.吸引电子能力强弱:氮>碳(3)达到平衡时,反应①碳酸二甲酯的产率
 随温度T的变化关系如图所示,则反应是
随温度T的变化关系如图所示,则反应是
 (选填“>”或“<”)。
(选填“>”或“<”)。
(4)某一恒温恒容
 装置内,
装置内, 与
与 发生反应②,
发生反应②,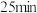 后,气体的密度减少
后,气体的密度减少 ,则
,则 内氨气的平均反应速率为
内氨气的平均反应速率为(5)传统合成DMC的方法是以光气(
 ,有剧毒)和甲醇为原料,请写出相应的化学方程式
,有剧毒)和甲醇为原料,请写出相应的化学方程式(6)新工艺合成DMC的方法和传统方法相比,优点有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】基态与激发态

(1)基态原子:处于___________ 状态的原子,
(2)基态原子___________ ,电子跃迁到___________ ,变为激发态原子;
(3)电子从较高能量的激发态跃迁到较低能量的激发态乃至基态时,将___________ ;
(4)___________ 是电子跃迁释放能量的重要形式之一。

(1)基态原子:处于
(2)基态原子
(3)电子从较高能量的激发态跃迁到较低能量的激发态乃至基态时,将
(4)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图是s能级和p能级的原子轨道图,试回答下列问题:
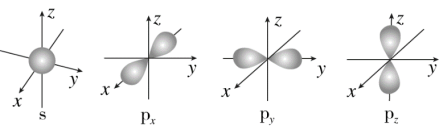
(1)s电子的原子轨道呈_______ 形,每个s能级有_______ 个原子轨道;p电子的原子轨道呈_______ 形,每个p能级有_______ 个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是_______ 电子,其电子云在空间有_______ 方向。
(3)下列原子或离子的电子排布式或轨道表示式正确的是_______ (填序号)
①K+:
②F: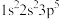
③P: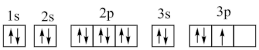
④Cu: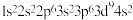
⑤Fe2+: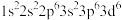
⑥Mg:
⑦O: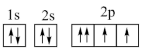

(1)s电子的原子轨道呈
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是
(3)下列原子或离子的电子排布式或轨道表示式正确的是
①K+:

②F:
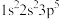
③P:
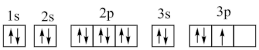
④Cu:
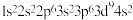
⑤Fe2+:
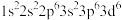
⑥Mg:

⑦O:
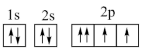
您最近一年使用:0次
【推荐1】光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可作太阳能电池材料的有单晶硅、多晶硅、非晶硅、 、
、 、
、 、
、 、
、 、
、 等。
等。
(1)指出31号元素镓 在元素周期表中的位置:第
在元素周期表中的位置:第___________ 周期第___________ 族。
(2) 、
、 、
、 电负性从大到小的顺序为
电负性从大到小的顺序为___________ 。
(3) 元素的第一电离能
元素的第一电离能___________ (填“大于”“小于”或“等于”) 元素的第一电离能,原因是
元素的第一电离能,原因是___________ 。
(4)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:___________ 。
(5)写出 轨道上只有2个未成对电子的元素的符号:
轨道上只有2个未成对电子的元素的符号:___________ 、___________ ;二者电负性:___________ >___________ 。
(6)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:___________ 。
 、
、 、
、 、
、 、
、 、
、 等。
等。(1)指出31号元素镓
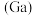 在元素周期表中的位置:第
在元素周期表中的位置:第(2)
 、
、 、
、 电负性从大到小的顺序为
电负性从大到小的顺序为(3)
 元素的第一电离能
元素的第一电离能 元素的第一电离能,原因是
元素的第一电离能,原因是(4)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:
(5)写出
 轨道上只有2个未成对电子的元素的符号:
轨道上只有2个未成对电子的元素的符号:(6)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)以下列出的是一些原子的2p能级和3d能级上电子排布的情况。违反了泡利原理的是______ (填序号,下同),违反了洪特规则的是______ 。
①
②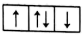
③
④
⑤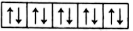
⑥
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为______ ;其最高价氧化物对应水化物的化学式是______ 。
(3)将下列多电子原子的能级按能级能量由低到高的顺序排列:______ (填序号)。
①1s ②3d ③4s ④3s ⑤4p ⑥3p
①

②

③

④

⑤

⑥

(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为
(3)将下列多电子原子的能级按能级能量由低到高的顺序排列:
①1s ②3d ③4s ④3s ⑤4p ⑥3p
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.铝合金和钢铁是国家重要的金属材料。回答下列问题:
(1)下列是气态铝原子或离子的电子排布式,其中处于激发态的有___________ (填序号)。A变为D所需的能量为E1,D变为E所需的能量为E2,则E1___________ E2(填“>”“<”或“=”),理由是___________ 。
A.1s22s22p63s23p1 B.1s22s22p63s13px13py1 C.1s22s22p63s13px13pz1
D.1s22s22p63s2 E.1s22s22p63s1 F.1s22s22p63s13p1
(2)利用电解法可在铝制品表面形成致密的氧化物保护膜,不仅可以增加美观,而且可以延长铝制品使用时间。制取氧化物保护膜的装置如下图所示,阳极的电极反应方程式为___________ 。
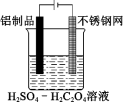
Ⅱ.钢铁在潮湿空气中容易生锈,某兴趣小组查阅资料可知,钢铁腐蚀的快慢与温度、电解质溶液的pH值、氧气浓度以及钢铁中的含碳量有关,为此设计了下列实验。

通过上述实验分析回答:
(3)上述实验①、②探究___________ 对铁的腐蚀快慢的影响,写出实验②碳电极上的电极反应式___________ ;
(4)上述四个实验中___________ (用编号表示)发生吸氧腐蚀,上述四个实验铁腐蚀由快到慢的顺序为___________ (用编号表示)。
(1)下列是气态铝原子或离子的电子排布式,其中处于激发态的有
A.1s22s22p63s23p1 B.1s22s22p63s13px13py1 C.1s22s22p63s13px13pz1
D.1s22s22p63s2 E.1s22s22p63s1 F.1s22s22p63s13p1
(2)利用电解法可在铝制品表面形成致密的氧化物保护膜,不仅可以增加美观,而且可以延长铝制品使用时间。制取氧化物保护膜的装置如下图所示,阳极的电极反应方程式为

Ⅱ.钢铁在潮湿空气中容易生锈,某兴趣小组查阅资料可知,钢铁腐蚀的快慢与温度、电解质溶液的pH值、氧气浓度以及钢铁中的含碳量有关,为此设计了下列实验。

| 编号 | ① | ② | ③ | ④ |
| A | 100 mL饱和NaCl溶液 | 100 mL饱和NaCl溶液 | 100 mLpH = 2 CH3COOH | 100 mLpH = 5 H2SO4 |
| B | m g铁粉 | m g铁粉和n g碳粉混合物 | m g铁粉和n g碳粉混合物 | m g铁粉和n g碳粉混合物 |
| 锥形瓶中压强随时间变化 | 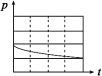 | 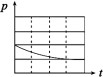 | 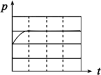 |  |
通过上述实验分析回答:
(3)上述实验①、②探究
(4)上述四个实验中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮、氟及其化合物在生产及生活中有着广泛的用途。请回答下列问题:
(1)氟磷灰石可用于制取磷肥,基态P原子有___________ 个未成对电子, 的中心P原子的杂化方式为
的中心P原子的杂化方式为___________ 。
(2)氟气可以用于制取惰性强于 的保护气
的保护气 ,也可以用于制取聚合反应的催化剂
,也可以用于制取聚合反应的催化剂 ,
, 可以作为工业制取硅单质的中间物质(
可以作为工业制取硅单质的中间物质( )的原料。
)的原料。
① 分子的空间结构为
分子的空间结构为___________ 。
②S、P、Si的第一电离能由大到小的顺序为___________ 。
(3)Na与N形成的 可用于汽车的安全气囊中,其中阴离子的空间结构为
可用于汽车的安全气囊中,其中阴离子的空间结构为___________ 。
(4)键角比较:
___________  (填“>”或“<”),其原因为
(填“>”或“<”),其原因为___________ 。
(1)氟磷灰石可用于制取磷肥,基态P原子有
 的中心P原子的杂化方式为
的中心P原子的杂化方式为(2)氟气可以用于制取惰性强于
 的保护气
的保护气 ,也可以用于制取聚合反应的催化剂
,也可以用于制取聚合反应的催化剂 ,
, 可以作为工业制取硅单质的中间物质(
可以作为工业制取硅单质的中间物质( )的原料。
)的原料。①
 分子的空间结构为
分子的空间结构为②S、P、Si的第一电离能由大到小的顺序为
(3)Na与N形成的
 可用于汽车的安全气囊中,其中阴离子的空间结构为
可用于汽车的安全气囊中,其中阴离子的空间结构为(4)键角比较:

 (填“>”或“<”),其原因为
(填“>”或“<”),其原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】比较下列分子或离子中的键角大小(填“>”“<”或“=”):
①PH3___________  ,原因是
,原因是___________ 。
②
___________  。
。
①PH3
 ,原因是
,原因是②

 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】价电子对互斥(简称VSEPR)理论可用于预测简单分子的空间结构。请回答下列问题:
(1)利用价电子对互斥理论推断下列分子或离子的空间结构:
①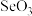
_____ ;②
_____ ;③
_____ ;④
_____ ;⑤
_____
(2)利用价电子对互斥理论推断键角的大小:(填“>”“<”或“=”,下同)
①甲醛分子中 的键角
的键角_____ 120°;
②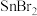 分子中
分子中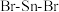 的键角
的键角_____ 120°;
③ 分子中
分子中 的键角
的键角_____ 109°28′。
(3)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据图所示的这两种微粒的球棍模型,写出相应的化学式:

A:_____ ;B:_____ 。
(4)按要求写出第2周期非金属元素组成的中性分子的化学式:平面形分子_____ ,三角锥形分子_____ ,四面体形分子_____ 。
(5)气态氢化物热稳定性 大于
大于 的主要原因是
的主要原因是_____ 。
(6)常温下,在水中的溶解度乙醇大于氯乙烷,原因是_____ 。
(1)利用价电子对互斥理论推断下列分子或离子的空间结构:
①
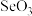




(2)利用价电子对互斥理论推断键角的大小:(填“>”“<”或“=”,下同)
①甲醛分子中
 的键角
的键角②
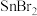 分子中
分子中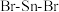 的键角
的键角③
 分子中
分子中 的键角
的键角(3)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据图所示的这两种微粒的球棍模型,写出相应的化学式:

A:
(4)按要求写出第2周期非金属元素组成的中性分子的化学式:平面形分子
(5)气态氢化物热稳定性
 大于
大于 的主要原因是
的主要原因是(6)常温下,在水中的溶解度乙醇大于氯乙烷,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐1】[化学——选修3:物质结构与性质]碳及其化合物广泛存在于自然界中,回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________ 形象化描述。在基态原子中,核外存在______ 对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是_____________ 。
(3)CS2分子中,共价键的类型有_____________ ,C原子的杂化轨道类型是_______ ,写出两个与CS2具有相同空间构型和键合形式的分子或离子_______________ 。
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于_____ 晶体。
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接_____ 个六元环,每个六元环占有___ 个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接________ 个六元环,六元环中最多有________ 个C原子在同一平面。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)碳在形成化合物时,其键型以共价键为主,原因是
(3)CS2分子中,共价键的类型有
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】碳及其化合物广泛存在于自然界中.回答下列问题:
(1)碳在形成化合物时,其键型以共价键为主,原因是_______ 。
(2) 分子中含有
分子中含有_______ (填“ 键”“
键”“ 键”或“
键”或“ 键和
键和 键”),C原子的杂化轨道类型是
键”),C原子的杂化轨道类型是_______ 。
(3)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:


①在石墨烯晶体中,每个C原子连接_______ 个六元环,每个六元环占有_______ 个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接_______ 个六元环。
(1)碳在形成化合物时,其键型以共价键为主,原因是
(2)
 分子中含有
分子中含有 键”“
键”“ 键”或“
键”或“ 键和
键和 键”),C原子的杂化轨道类型是
键”),C原子的杂化轨道类型是(3)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:


①在石墨烯晶体中,每个C原子连接
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】绿芦笋中含有天门冬氨酸(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。回答下列问题:___________ ,其中N原子的杂化轨道类型为___________ ,图中O—C—C的键角___________ C—C—N的键角(填“大于”或“小于”)。
(2) 和
和 热稳定性较好的是
热稳定性较好的是___________ ,从分子结构角度解释其原因:___________ 。
(3)分子结构修饰在药物设计与合成中有广泛的应用。若将天门冬氨酸中的 ,换成
,换成 ,得到的新物质的酸性会增强,原因是
,得到的新物质的酸性会增强,原因是___________ 。
(4)四个主族元素部分简单氢化物沸点随周期序数的变化如图所示。其中表示第VIIA族元素简单氢化物沸点变化的是曲线___________ (填字母),O—H…O的键能小于F—H…F,但水的沸点高于HF的原因可能是___________ 。

(2)
 和
和 热稳定性较好的是
热稳定性较好的是(3)分子结构修饰在药物设计与合成中有广泛的应用。若将天门冬氨酸中的
 ,换成
,换成 ,得到的新物质的酸性会增强,原因是
,得到的新物质的酸性会增强,原因是(4)四个主族元素部分简单氢化物沸点随周期序数的变化如图所示。其中表示第VIIA族元素简单氢化物沸点变化的是曲线

您最近一年使用:0次



