氮、氟及其化合物在生产及生活中有着广泛的用途。请回答下列问题:
(1)氟磷灰石可用于制取磷肥,基态P原子有___________ 个未成对电子, 的中心P原子的杂化方式为
的中心P原子的杂化方式为___________ 。
(2)氟气可以用于制取惰性强于 的保护气
的保护气 ,也可以用于制取聚合反应的催化剂
,也可以用于制取聚合反应的催化剂 ,
, 可以作为工业制取硅单质的中间物质(
可以作为工业制取硅单质的中间物质( )的原料。
)的原料。
① 分子的空间结构为
分子的空间结构为___________ 。
②S、P、Si的第一电离能由大到小的顺序为___________ 。
(3)Na与N形成的 可用于汽车的安全气囊中,其中阴离子的空间结构为
可用于汽车的安全气囊中,其中阴离子的空间结构为___________ 。
(4)键角比较:
___________  (填“>”或“<”),其原因为
(填“>”或“<”),其原因为___________ 。
(1)氟磷灰石可用于制取磷肥,基态P原子有
 的中心P原子的杂化方式为
的中心P原子的杂化方式为(2)氟气可以用于制取惰性强于
 的保护气
的保护气 ,也可以用于制取聚合反应的催化剂
,也可以用于制取聚合反应的催化剂 ,
, 可以作为工业制取硅单质的中间物质(
可以作为工业制取硅单质的中间物质( )的原料。
)的原料。①
 分子的空间结构为
分子的空间结构为②S、P、Si的第一电离能由大到小的顺序为
(3)Na与N形成的
 可用于汽车的安全气囊中,其中阴离子的空间结构为
可用于汽车的安全气囊中,其中阴离子的空间结构为(4)键角比较:

 (填“>”或“<”),其原因为
(填“>”或“<”),其原因为
更新时间:2024-01-25 14:45:06
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是两者的键能(单位: )数据:
)数据:
结合数据说明 比
比 活泼的原因:
活泼的原因:_______ 。
 )数据:
)数据: |  |  | |
 | 351 | 745 | 1071.9 |
 | 139 | 418 | 946 |
结合数据说明
 比
比 活泼的原因:
活泼的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)固态氟化氢中存在(HF)n形式,画出(HF)3的链状结构_______ 。
(2)CF2=CF2和ETFE分子中C的杂化轨道类型分别为_______ 和_______ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
(1)固态氟化氢中存在(HF)n形式,画出(HF)3的链状结构
(2)CF2=CF2和ETFE分子中C的杂化轨道类型分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)Ag的核外电子排布式是[Kr]4d105s1,则Ag在元素周期表中的位置是_______ 。下列属于基态Ag+的电子排布式的是_______ 。(填标号)
A.[Kr]4d95s2 B.[Kr]4d10 C.[Kr]4d95s1
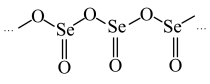
(2)硒所在的主族中,简单气态氢化物沸点最低的是________ (填化学式);硒的某种氧化物为链状聚合结构(如图所示),该氧化物的化学式为_______ 。
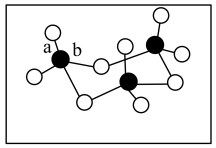
(3)固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为_______ ,该结构中S-O键长有两类,一类键长约140pm,另一类键长约160pm,较短的键为_______ (填图中字母)。
(4)FeSO4•H2O结构如图所示。
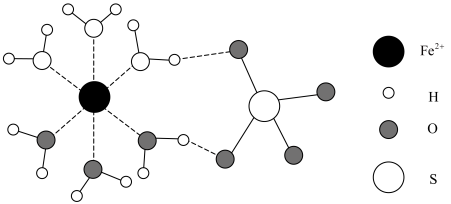
Fe2+价层电子排布式为________ 。比较SO 和H2O分子中的键角大小并给出相应解释:
和H2O分子中的键角大小并给出相应解释:_______ 。
(1)Ag的核外电子排布式是[Kr]4d105s1,则Ag在元素周期表中的位置是
A.[Kr]4d95s2 B.[Kr]4d10 C.[Kr]4d95s1
(2)硒所在的主族中,简单气态氢化物沸点最低的是

(3)固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为

(4)FeSO4•H2O结构如图所示。

Fe2+价层电子排布式为
 和H2O分子中的键角大小并给出相应解释:
和H2O分子中的键角大小并给出相应解释:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表为长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区的元素是___________ (填编号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为_________ 。
(3)④ ⑤ ⑥ ⑦四种元素的第一电离能由大到小的顺序是___________ (用元素符号表示)。
(4)按原子轨道的重叠方式,③与⑥形成的化合物中σ键有______ 个,π键有______ 个。
(5)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为_______ ;该元素与元素①形成的分子X的空间构形为___________ 。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:__________________ 。

请回答下列问题:
(1)表中属于d区的元素是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
(3)④ ⑤ ⑥ ⑦四种元素的第一电离能由大到小的顺序是
(4)按原子轨道的重叠方式,③与⑥形成的化合物中σ键有
(5)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为
(6)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】H、C、N、O、S是重要的非金属元素,请按要求回答下列问题:
(1)C元素的一种氢化物(分子中含有6个原子)是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是_______ 。(填序号)。
a.该氢化物分子中C原子采用 杂化 b.6个原子不在同一平面上
杂化 b.6个原子不在同一平面上
c.只含有4个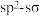 键和1个
键和1个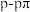 键 d.分子既含有极性键又含有非极性键
键 d.分子既含有极性键又含有非极性键
(2)相同条件下 与
与 分子在水中的溶解度较大的是
分子在水中的溶解度较大的是_______ (写分子式),理由是_______ 。 中的O—C—O键角
中的O—C—O键角_______ (填“>”“<”或“=”) 中的O—S—O键角。
中的O—S—O键角。
(3)已知(CN)2是直线形分子,且有对称性,则(CN)2分子的结构式为_______ ;其中 键与
键与 键的个数比为
键的个数比为_______ 。
(1)C元素的一种氢化物(分子中含有6个原子)是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是
a.该氢化物分子中C原子采用
 杂化 b.6个原子不在同一平面上
杂化 b.6个原子不在同一平面上c.只含有4个
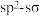 键和1个
键和1个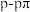 键 d.分子既含有极性键又含有非极性键
键 d.分子既含有极性键又含有非极性键(2)相同条件下
 与
与 分子在水中的溶解度较大的是
分子在水中的溶解度较大的是 中的O—C—O键角
中的O—C—O键角 中的O—S—O键角。
中的O—S—O键角。(3)已知(CN)2是直线形分子,且有对称性,则(CN)2分子的结构式为
 键与
键与 键的个数比为
键的个数比为
您最近一年使用:0次



