比较下列分子或离子中的键角大小(填“>”“<”或“=”):
①PH3___________  ,原因是
,原因是___________ 。
②
___________  。
。
①PH3
 ,原因是
,原因是②

 。
。
2023高三·全国·专题练习 查看更多[1]
(已下线)第4讲 空间构型
更新时间:2023-09-29 14:34:47
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)H2O的沸点高于H2S是因为________________ ;H2O分子比H2S分子稳定是因为__________________ 。
(2)Al和铁红发生铝热反应的化学方程式_________________ ,该反应的用途是_________________ (任写一条)。
(2)Al和铁红发生铝热反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列填空:
(1)有下列分子或离子:①CS2,②PCl3,③H2S,④CH2O,⑤H3O+,⑥NH4+,⑦BF3,⑧SO2。粒子的立体构型为直线形的有________ (填序号,下同);粒子的立体构型为V形的有________ ;粒子的立体构型为平面三角形的有________ ;粒子的立体构型为三角锥形的有____ ;粒子的立体构型为正四面体形的有____ 。
(2)俗称光气的氯代甲酰氯分子(COCl2)为平面三角形,但C—Cl键与C=O键之间的夹角为124.3°;C—Cl键与C—Cl键之间的夹角为111.4°,解释其原因:____ 。
(1)有下列分子或离子:①CS2,②PCl3,③H2S,④CH2O,⑤H3O+,⑥NH4+,⑦BF3,⑧SO2。粒子的立体构型为直线形的有
(2)俗称光气的氯代甲酰氯分子(COCl2)为平面三角形,但C—Cl键与C=O键之间的夹角为124.3°;C—Cl键与C—Cl键之间的夹角为111.4°,解释其原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
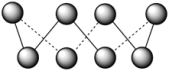
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是_______ 。
(2)比较酸性:H2SeO4_______ H2SeO3(填“>”、“<”或“=”)。
(3)气态SeO3分子的立体构型为_______ ,  离子的VSEPR模型为
离子的VSEPR模型为_______ 。
(4)H2Se、H2S、H2O的沸点由高到低的顺序是_______ ,原因是_______ 。
(5)H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角大,原因是_______ 。
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

(2)比较酸性:H2SeO4
(3)气态SeO3分子的立体构型为
 离子的VSEPR模型为
离子的VSEPR模型为(4)H2Se、H2S、H2O的沸点由高到低的顺序是
(5)H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角大,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】2022年春晚节目《只此青绿》取材于宋代名画《千里江山图》,该画描绘了山清水秀的美丽景色,历经千年色彩依然,其中青色来自蓝铜矿颜料[主要成分为Cu3(CO3)2(OH)2]。请回答下列问题:
(1)从原子结构角度分析,第二电离能I2(Fe)与I2(Cu)的关系是I2(Fe)___________ I2(Cu)(填“>”“<”或“=”)
(2) 的空间构型为
的空间构型为___________ 。
(3)我国科学家制取了一种铜的配合物如图所示,该配合物中四种非金属元素电负性由大到小的顺序是___________ (填元素符号),该配合物中采用sp2杂化的碳原子与sp3杂化的碳原子个数比为___________ 。

(1)从原子结构角度分析,第二电离能I2(Fe)与I2(Cu)的关系是I2(Fe)
(2)
 的空间构型为
的空间构型为(3)我国科学家制取了一种铜的配合物如图所示,该配合物中四种非金属元素电负性由大到小的顺序是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题。
(1)CCl4、H2S、BF3、CO2键角由大到小的顺序是___________ 。
(2)As4O6的分子结构如图所示: ,其中As原子的杂化方式为
,其中As原子的杂化方式为___________ ,O原子的杂化方式为___________ 。
(3)[Co(NO2)(NH3)5]Cl2中Co3+的配位数为___________ ,粒子中的大π键可用符号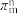 表示,中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大
表示,中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则配体中NO
),则配体中NO 的大π键可表示为
的大π键可表示为___________ ,空间构型为___________ 。
(4)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)回答下列问题:
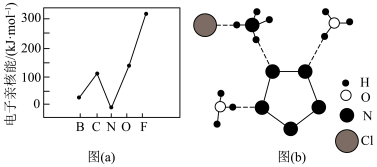
①元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1(纵坐标)变化趋势如图(a)。其中除氮元素外,其他元素的E1自左而右依次增大的原因___________ ,氮元素的E1呈现异常的原因是___________ 。
②用X射线衍射实验方法测得化合物R的晶体结构,其局部结构如图(b)所示:从结构分析,R中两种阳离子的相同之处为___________ (填标号),不同之处为___________ (填标号)。
A.中心原子的杂化类型
B.中心原子的价层电子对数
C.立体结构
(1)CCl4、H2S、BF3、CO2键角由大到小的顺序是
(2)As4O6的分子结构如图所示:
 ,其中As原子的杂化方式为
,其中As原子的杂化方式为(3)[Co(NO2)(NH3)5]Cl2中Co3+的配位数为
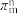 表示,中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大
表示,中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则配体中NO
),则配体中NO 的大π键可表示为
的大π键可表示为(4)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)回答下列问题:

①元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1(纵坐标)变化趋势如图(a)。其中除氮元素外,其他元素的E1自左而右依次增大的原因
②用X射线衍射实验方法测得化合物R的晶体结构,其局部结构如图(b)所示:从结构分析,R中两种阳离子的相同之处为
A.中心原子的杂化类型
B.中心原子的价层电子对数
C.立体结构
您最近一年使用:0次

 分子中,键角∠HCO
分子中,键角∠HCO

