下列有关实验操作的叙述不正确的是
| A.可用酸式滴定管移取高锰酸钾溶液 |
| B.实验剩余的药品都要放回原试剂瓶中,不能随意丢弃 |
| C.使用经蒸馏水润湿的pH试纸测溶液的pH,结果可能偏小 |
| D.配制一定物质的量浓度的NaCl溶液,定容时俯视会使溶液浓度偏高 |
更新时间:2017-05-03 09:03:15
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】读所给药品标签,有关分析不正确的是
| 选项 | A | B | C | D |
| 药品标签 | 饱和氯水1.01×105Pa,20℃ | 药品:××× | 碳酸氢钠:NaHCO3 俗名:小苏打(84g  mol-1) mol-1) | 浓硫酸(H2SO4) 密度:1.84g  mL-1 mL-1浓度:98.0% |
| 分析 | 试剂应装在橡胶塞的细口瓶中 | 该药品不能与皮肤直接接触 | 该物质受热易分解 | 该药品物质的量浓度为18.4mol L-1 L-1 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】玻璃棒是化学实验中的常用仪器。下列有关玻璃棒的使用不合理的是
A. | B. |
C.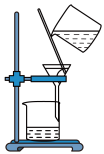 | D.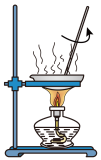 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验操作或叙述正确的是
①不宜用瓷坩埚灼烧氢氧化钠或碳酸钠固体;
②为了提高纯锌与稀硫酸反应的速率,可向稀硫酸中滴入几滴CuSO4溶液;
③用蒸馏水润湿的pH试纸测定溶液的pH一定有误差;
④向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,可以制得Fe(OH)3胶体;
⑤配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸;
⑥向饱和NaCl溶液中滴加浓硫酸制备HCl;
⑦亚硫酸钠与浓硫酸反应制备SO2;
⑧欲配制90ml 0.2 mol·L-1CuSO4溶液,需要称量CuSO4·5H2O的质量为4.5g 。
①不宜用瓷坩埚灼烧氢氧化钠或碳酸钠固体;
②为了提高纯锌与稀硫酸反应的速率,可向稀硫酸中滴入几滴CuSO4溶液;
③用蒸馏水润湿的pH试纸测定溶液的pH一定有误差;
④向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,可以制得Fe(OH)3胶体;
⑤配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸;
⑥向饱和NaCl溶液中滴加浓硫酸制备HCl;
⑦亚硫酸钠与浓硫酸反应制备SO2;
⑧欲配制90ml 0.2 mol·L-1CuSO4溶液,需要称量CuSO4·5H2O的质量为4.5g 。
| A.①②⑧ | B.①②⑦ | C.③④⑥ | D.⑤⑦⑧ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列方案能达到实验目的是
| A.用排水集气法收集Cl2 | B.用水萃取溴的CCl4中的溴单质 |
| C.用焰色反应鉴别NaCl和KOH | D.利用Fe与稀盐酸制取FeCl3 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列操作或提供的仪器(夹持仪器任选)不能实现相应实验目的是
| 选项 | 目的 | 仪器或操作 |
| A | 分离CCl4萃取碘水后的溶液 | 分液漏斗、烧杯 |
| B | 从食盐水中获得NaCl晶体 | 蒸发皿、玻璃棒、酒精灯、泥三角 |
| C | 将酸性溶液中的MnO4﹣完全转化Mn2+ | 向溶液中滴加H2O2溶液至紫色消失 |
| D | 配制100 mL 1.0 mol/L CuSO4溶液 | 将25 g CuSO4•5H2O溶于100 mL蒸馏水中 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



