由U形管、铁棒、石墨棒、1 L 0.lmol/L CuCl2溶液等组成如图装置,下列说法不正确的是
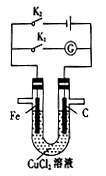
| A.同时打开K1、K2,铁棒上有紫红色物质析出 |
| B.只闭合K1,石墨棒上有紫红色物质析出 |
| C.只闭合K2,当电路中通过0.3mol电子时,两极共产生4.48L(标准状况)气体 |
| D.只闭合K2,一段时间后,将电解质溶液搅拌均匀,溶液的pH变大(不考虑Cl2的溶解) |
更新时间:2017-05-04 17:11:20
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
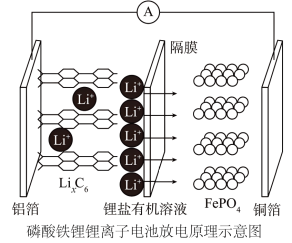
【推荐1】2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家,磷酸铁锂锂离子电池充电时阳极反应式为, ,电池放电时,锂离子从石墨晶体中脱嵌出来,通过隔膜迁移到磷酸铁锂晶体表面,然后重新嵌入到磷酸铁锂的晶格内,放电工作示意图如图。下列叙述不正确的是
,电池放电时,锂离子从石墨晶体中脱嵌出来,通过隔膜迁移到磷酸铁锂晶体表面,然后重新嵌入到磷酸铁锂的晶格内,放电工作示意图如图。下列叙述不正确的是
 ,电池放电时,锂离子从石墨晶体中脱嵌出来,通过隔膜迁移到磷酸铁锂晶体表面,然后重新嵌入到磷酸铁锂的晶格内,放电工作示意图如图。下列叙述不正确的是
,电池放电时,锂离子从石墨晶体中脱嵌出来,通过隔膜迁移到磷酸铁锂晶体表面,然后重新嵌入到磷酸铁锂的晶格内,放电工作示意图如图。下列叙述不正确的是
| A.放电时,Li+通过隔膜移向正极 |
| B.放电时,电子由铝箔沿导线流向铜箔 |
C.放电时正极反应为: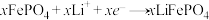 |
| D.磷酸铁锂锂离子电池充放电过程通过Li+迁移实现,C、Fe、P元素化合价均不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】科学家发明了一种Al-PbO2电池,电解质为K2SO4、H2SO4、KOH,通过x和y两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域(a>b),结构示意图如图所示。下列说法不正确的是
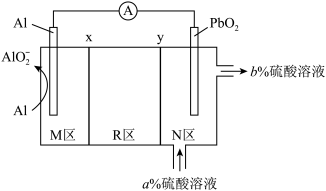

| A.K+通过x膜移向R区域 |
| B.R区域的电解质浓度逐渐减小 |
C.放电时,Al电极反应为:Al-3e-+4OH-=AlO +2H2O +2H2O |
| D.消耗1.8gAl时,N区域电解质溶液减少16.0g |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】利用电解法将 转化为
转化为 的原理如图所示。下列说法错误的是
的原理如图所示。下列说法错误的是

 转化为
转化为 的原理如图所示。下列说法错误的是
的原理如图所示。下列说法错误的是
A.电解过程中, 由b极区向a极区迁移 由b极区向a极区迁移 |
B.电极b上反应为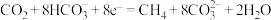 |
| C.电解过程中电能能转化为化学能 |
D.电解时 溶液浓度增大 溶液浓度增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】锌—空气电池可用作电动车的动力电源。该电池的电解质溶液为KOH溶液,总反应为: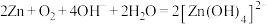 。下列说法错误的是
。下列说法错误的是
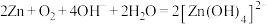 。下列说法错误的是
。下列说法错误的是A.Zn做负极, 在正极发生还原反应 在正极发生还原反应 |
| B.当电路中通过2mol电子时,消耗氧气22.4L(标准状况) |
C.电解质溶液中 向正极移动 向正极移动 |
D.负极反应式为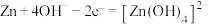 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】近期科技工作者开发了一套以乙醇为原料制备DDE(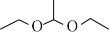 )的电解装置如下图所示。下列说法正确的是
)的电解装置如下图所示。下列说法正确的是
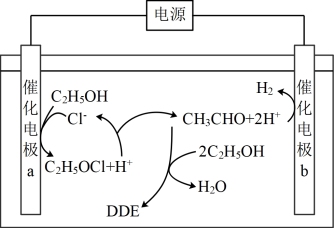
 )的电解装置如下图所示。下列说法正确的是
)的电解装置如下图所示。下列说法正确的是
| A.催化电极的电极电势:b>a |
| B.每产生1molH2需要消耗3mol乙醇 |
| C.电解后溶液的pH会减小(忽略溶液体积变化) |
D.阴极电极反应式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列化学用语或离子方程式书写错误的是
A.用电子式表示 形成过程: 形成过程: |
B.用惰性电极电解 溶液: 溶液: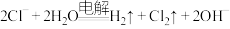 |
C.向含 的溶液中通入amolCl2 的溶液中通入amolCl2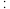  |
D. 溶液中加入 溶液中加入 产生沉淀: 产生沉淀: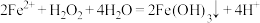 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】我国科学家研发了一种水系可逆Zn-CO2电池,电池工作时,复合膜(由a、b膜复合而成)层间的H2O解离成H+ 和OH-,在外加电场中可透过相应的离子膜定向移动。当闭合K1时,Zn-CO2电池工作原理如图所示。下列说法不正确的是
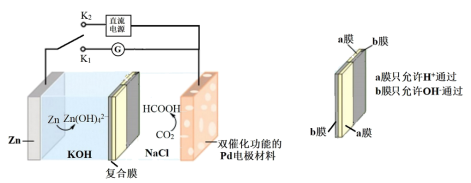

| A.闭合K2时,Zn电极与直流电源正极相连 |
| B.闭合K2时,Pd电极是阳极,发生氧化反应 |
| C.闭合K1时,H+通过a膜向Pd电极方向移动 |
D.闭合K1时,Zn表面的电极反应式为Zn + 4OH- - 2e- = Zn(OH) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】如图所示,a、b、c、d均为石墨电极,通电进行电解,下列说法正确的是( )


| A.电路中电子流向:负极→d→c→b→a→正极 |
| B.a、c两极产生气体的物质的量相等 |
| C.SO42-向b电极运动,Cl-向c电极运动 |
| D.通电后乙烧杯滴入酚酞溶液d极会变红 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】如图所示,将两烧杯中的电极用电线相连,四个电极分别为Mg、Al、Pt、C。当闭合开关S后,以下表示正确的是( )
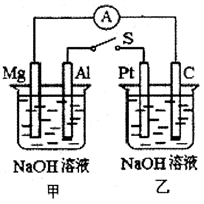

| A.Mg、C两极生成的气体在一定条件下可以恰好完全反应 |
| B.Al、Pt两极有H2产生 |
| C.两池能量转换方式相同 |
| D.甲池pH减小,乙池pH不变 |
您最近一年使用:0次

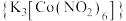 是一种黄色难溶物。检验
是一种黄色难溶物。检验 的反应原理如下:
的反应原理如下: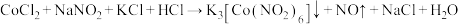 (未配平)。下列说法错误的是
(未配平)。下列说法错误的是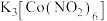 中配位原子是氧原子
中配位原子是氧原子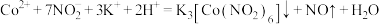
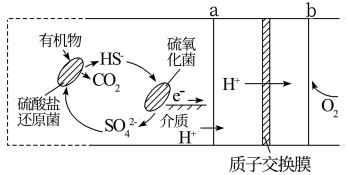
 溶液时,在阳极和阴极析出产物的物质的量之比为2:1
溶液时,在阳极和阴极析出产物的物质的量之比为2:1 溶液时,溶液浓度将增大,pH不变
溶液时,溶液浓度将增大,pH不变

