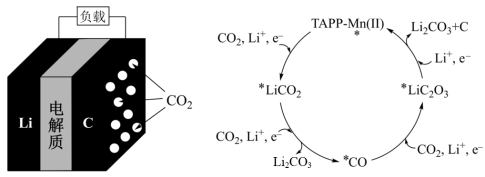
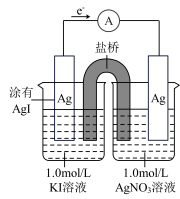
Li-FeS2热激活电池以固体KCl、LiCl为电解质,放电总反应为:FeS2+4Li=Fe +2Li2S,下列说法不正确的是
| A.负极反应式为:Li-e-=Li+ | B.正极反应式为:FeS2+4e-=Fe+2S2- |
| C.电池放电时K+向正极移动 | D.可用KCl、LiCl的水溶液做电解质溶液 |
更新时间:2017-05-07 19:44:37
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示,下列说法正确的是
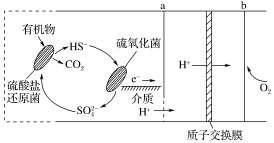

A.HS-转化为 的反应为HS-+4H2O-8e-= 的反应为HS-+4H2O-8e-= +9H+ +9H+ |
| B.电极b是该电池的正极,发生氧化反应 |
| C.电子从电极b流出,经外电路流向电极a |
| D.若外电路中有0.4mol电子发生转移,则有0.5molH+通过质子交换膜 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】将图1所示装置中的盐桥(琼脂-饱和 溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是
溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是

 溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是
溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是
A.图1中,铁棒质量减少5.6g,则甲池 溶液的质量增加5.6g 溶液的质量增加5.6g |
B.图1中的石墨电极与图2中乙池石墨 电极的电极反应式相同 电极的电极反应式相同 |
| C.两图所示装置的能量变化均是将化学能转化为电能 |
D.图2中电子流向为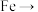 电流计→石墨a→石墨b→铜丝→石墨c→ 电流计→石墨a→石墨b→铜丝→石墨c→ |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】光催化微生物燃料电池的工作原理如图所示:

已知:电极a在光激发条件下会产生电子( )-空穴(
)-空穴( )。下列说法错误的是
)。下列说法错误的是

已知:电极a在光激发条件下会产生电子(
 )-空穴(
)-空穴( )。下列说法错误的是
)。下列说法错误的是| A.电极电势:电极a>电极b |
B.光激发时,光生电子会与 结合,光生空穴会与电极b产生的电子结合 结合,光生空穴会与电极b产生的电子结合 |
C.电极b发生的电极反应式为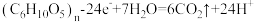 |
D.电池工作一段时间后,右侧溶液pH保持不变(不考虑 的溶解) 的溶解) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
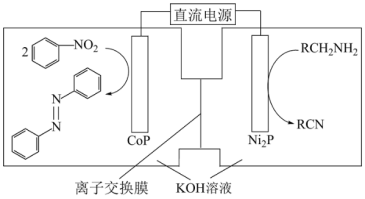
【推荐2】天津大学研究团队以KOH溶液为电解质,CoP和Ni2P纳米片为催化电极材料,电催化合成偶氮化合物(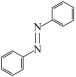 )的装置如图所示(R代表烃基)。下列说法正确的是
)的装置如图所示(R代表烃基)。下列说法正确的是
 )的装置如图所示(R代表烃基)。下列说法正确的是
)的装置如图所示(R代表烃基)。下列说法正确的是
| A.若用铅蓄电池作为电源,CoP极连接铅蓄电池的正极 |
| B.Ni2P电极反应式为RCH2NH2-4e-+4OH-=RCN+4H2O |
| C.合成1mol偶氮化合物,需转移4mol电子 |
| D.离子交换膜是阳离子交换膜 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
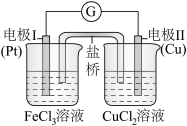
【推荐1】如图是某同学设计的原电池装置,下列叙述中正确的是( )

| A.氧化剂和还原剂必须直接接触才能发生反应 |
| B.电极Ⅱ上发生还原反应,作原电池的正极 |
| C.该原电池的总反应式为:2Fe3++Cu===Cu2++2Fe2+ |
| D.盐桥中装有含氯化钾的琼脂,K+移向负极区 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】以N2和H2为反应物,盐酸酸化的NH4Cl溶液为电解质的原电池,工作原理如下图所示,下列说法不正确的是
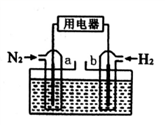

| A.b电极为负极 |
| B.反应过程中,溶液中的Cl-向a电极移动 |
| C.a电极的电极反应式为:N2+6e-+8H+=2NH4+ |
| D.电池反应为N2+3H2+2HCl=2NH4Cl |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知反应Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s)为自发进行的氧化还原反应,将其设计成如右图所示的原电池,下列说法中正确的是
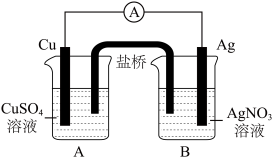

| A.铜电极是正极,其电极反应为Cu-2e-=Cu2+ |
| B.当铜电极质量减少0.64g时,电解质溶液中有0.02mol电子通过 |
| C.装置盐桥中可装有含琼脂的KCl饱和溶液 |
| D.银电极上发生还原反应,电极质量增加 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,下列说法正确的是
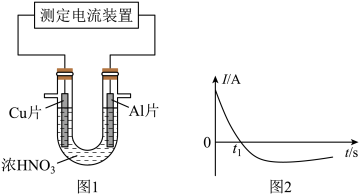
| A.0-t1时,原电池的负极是铜片 |
| B.0-t1时,正极的电极反应式是2H++2e-=H2↑ |
| C.t1时刻,电流方向发生变化的原因是Al 在浓硝酸中发生钝化,氧化膜阻止了Al进一步反应 |
| D.tl时刻后,电子从铝经过导线流向铜 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列几个与电化学相关的装置示意图中,有关叙述正确的是


| A.装置①是电解Na2SO4溶液联合生产硫酸和烧碱示意图,若气体甲,乙的体积比约为1∶2,则离子交换膜c、d均为阴离子交换膜,产物丙为硫酸溶液 |
| B.装置②是以肼(N2H4)为燃料的电池装置,a极的反应式:N2H4+4OH--4e-=N2↑+4H2O |
| C.装置③是在待镀铁制品上镀铜的实验装置,电镀过程中电极Ⅱ上Cu2+放电而使溶液中Cu2+浓度逐渐变小 |
| D.装置④是金属牺牲阳极的阴极保护法实验装置,加入K3[Fe(CN)6]溶液后,Fe电极附近会产生蓝色沉淀 |
您最近一年使用:0次