浅绿色的硫酸亚铁铵晶体[又名莫尔盐,(NH4)2SO4·FeSO4·6H2O]比绿矾(FeSO4·7H2O)更稳定,常用于定量分析。莫尔盐的一种实验室制法如下:
废铁屑
 溶液A
溶液A
 莫尔盐
莫尔盐
(1)向废铁屑中加入稀硫酸后,并不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是________________________________________________________________ ;
证明溶液A不含Fe3+的最佳试剂是______ (填字母)。
a.酚酞溶液 b.KSCN溶液
c.烧碱溶液 d.KMnO4溶液
操作Ⅰ的步骤是加热蒸发、_____________ 、过滤。
(2)浓度均为0.1 mol·L-1莫尔盐溶液和(NH4)2SO4溶液,c(NH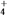 )前者大于后者,原因是
)前者大于后者,原因是____________________________________________________________ 。
(3)用托盘天平称量(NH4)2SO4晶体,晶体要放在天平________ (填“左”或“右”)盘。
(4)从下列装置中选取必要的装置制取(NH4)2SO4溶液,连接的顺序(用接口字母表示)是a接_________ ;________ 接________ 。


(5)将装置C中两种液体分离开的操作名称是_____________ 。
装置D的作用是____________________________________________ 。
废铁屑

 溶液A
溶液A
 莫尔盐
莫尔盐(1)向废铁屑中加入稀硫酸后,并不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是
证明溶液A不含Fe3+的最佳试剂是
a.酚酞溶液 b.KSCN溶液
c.烧碱溶液 d.KMnO4溶液
操作Ⅰ的步骤是加热蒸发、
(2)浓度均为0.1 mol·L-1莫尔盐溶液和(NH4)2SO4溶液,c(NH
 )前者大于后者,原因是
)前者大于后者,原因是(3)用托盘天平称量(NH4)2SO4晶体,晶体要放在天平
(4)从下列装置中选取必要的装置制取(NH4)2SO4溶液,连接的顺序(用接口字母表示)是a接


(5)将装置C中两种液体分离开的操作名称是
装置D的作用是
更新时间:2017-06-30 03:34:10
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】过氧化钠、过氧化镁、过氧化氢都是重要的过氧化物。回答下列问题:
(1)取少量含Fe2+、H+溶液于试管中,滴加几滴硫氰酸钾溶液,无明显现象:再滴加H2O2,发现溶液变红色,其中包括的反应_____________________ ,_____________________ 。(写离子方程式);继续加H2O2,红色逐渐褪去且有气泡产生,反应原理为:H2O2+SCN-—SO42-+CO2↑+N2↑+H2O+_______ (将方程式补充完成并配平)
(2)过氧化镁不溶于水,但易溶于稀酸。广泛用作胃药,治疗胃酸过多。试写出过氧化镁与胃酸反应的离子方程式__________________________________ 。
(3)高温下,过氧化钠在隔绝空气环境中可以将铁单质氧化成含FeO42-高铁酸盐,该反应的化学方程式为_________________________________ 。
(1)取少量含Fe2+、H+溶液于试管中,滴加几滴硫氰酸钾溶液,无明显现象:再滴加H2O2,发现溶液变红色,其中包括的反应
(2)过氧化镁不溶于水,但易溶于稀酸。广泛用作胃药,治疗胃酸过多。试写出过氧化镁与胃酸反应的离子方程式
(3)高温下,过氧化钠在隔绝空气环境中可以将铁单质氧化成含FeO42-高铁酸盐,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】比较下列两组反应,回答有关问题。
一组:①Na2O2+CO2 ②Na2O2+SO2
二组:③Na2O2+FeCl3(溶液) ④Na2O2+FeCl2(溶液)
问题:
(1)写出①、②两反应的化学方程式_______ 、______ 。
(2)判断③、④反应中可能发生的现象,为什么?______
(3)Na2O2在什么情况下表现强氧化性?________
一组:①Na2O2+CO2 ②Na2O2+SO2
二组:③Na2O2+FeCl3(溶液) ④Na2O2+FeCl2(溶液)
问题:
(1)写出①、②两反应的化学方程式
(2)判断③、④反应中可能发生的现象,为什么?
(3)Na2O2在什么情况下表现强氧化性?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某化学兴趣小组利用铁粉、锌粉、0.1mol•L-1FeCl3溶液、0.1mol•L-1FeCl2溶液、KSCN溶液和新制氯水来探究Fe2+、Fe3+的氧化性、还原性。
(1)用上述所给物质写出体现Fe2+具有还原性的化学方程式:_______ 。
(2)设计实验方案,完成下列表格。
①处的现象为_______ ;①处加入铁粉后反应的离子方程式为__ ;②处的现象为_______ ;
(3)取一定量氯化亚铁固体,配制成0.1mol•L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是_______ 。
(4)该兴趣小组为探究“Fe2+具有氧化性”,提出了向FeCl2溶液中加入锌粉,该反应的离子方程式为___ 。
(1)用上述所给物质写出体现Fe2+具有还原性的化学方程式:
(2)设计实验方案,完成下列表格。
| 探究内容 | 实验方案 | 实验现象 |
| 探究Fe3+具有氧化性 | 取少量0.1mol/LFeCl3溶液中加入足量铁粉,再加入少量KSCN溶液 | 加入铁粉后,溶液颜色变为①___;加入KSCN溶液后,溶液②____ |
①处的现象为
(3)取一定量氯化亚铁固体,配制成0.1mol•L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是
(4)该兴趣小组为探究“Fe2+具有氧化性”,提出了向FeCl2溶液中加入锌粉,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铁及其化合物在人类的生产生活中扮演着重要的角色。
(1)铁是人体中一种重要的金属元素,在血红蛋白中存在着的铁能结合氧分子进行输氧。据此分析血红蛋白中铁存在的价态为_______ 。(已知:铁常见的化合价有+2、+3价)
(2)铁和水不能反应,但可以与高温水蒸气作用。写出该反应的化学方程式,用单线桥法标出电子转移的方向和数目_______ 。
(3)把铁丝投入氯化铁溶液中充分反应,溶液的颜色从_______ 变为_______ ,写出该反应的化学方程式_______ 。检验氯化铁溶液是否反应完全的操作是_______ 。
(1)铁是人体中一种重要的金属元素,在血红蛋白中存在着的铁能结合氧分子进行输氧。据此分析血红蛋白中铁存在的价态为
(2)铁和水不能反应,但可以与高温水蒸气作用。写出该反应的化学方程式,用单线桥法标出电子转移的方向和数目
(3)把铁丝投入氯化铁溶液中充分反应,溶液的颜色从
您最近一年使用:0次
【推荐2】当人体缺铁时,往往需要服用补铁剂,人体能吸收的是+2价铁元素。查看一些补铁剂的主要成分,了解其中铁元素的价态。
(1)你认为可以采用什么方法检验补铁剂中铁元素的价态_________ ?
(2)天然食品中含有的大多是+3价铁元素,为了使+3价铁元素转化为+2价铁元素并被人体更好地吸收,你认为应该采取哪些措施?请查阅资料寻找办法__________ 。
(1)你认为可以采用什么方法检验补铁剂中铁元素的价态
(2)天然食品中含有的大多是+3价铁元素,为了使+3价铁元素转化为+2价铁元素并被人体更好地吸收,你认为应该采取哪些措施?请查阅资料寻找办法
您最近一年使用:0次

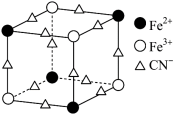
 结构如图所示(K+未画出),则一个晶胞中的K+个数为
结构如图所示(K+未画出),则一个晶胞中的K+个数为