一定温度下,将一定量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是
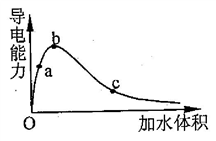

| A.a,b,c三点溶液的pH:a>b>c |
| B.若用湿润的pH试纸测试c处溶液的pH,比实际的pH偏小 |
| C.a,b,c三点溶液用1mol·L-1的NaOH溶液中和,消耗NaOH溶液的体积a>b>c |
| D.a,b,c点醋酸的电离程度:c>b>a |
更新时间:2017-07-05 15:33:24
|
【知识点】 弱电解质电离平衡的影响因素
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】常温下,关于1 mol ·L-1的H2C2O4溶液的理解正确的是
| A.加水稀释过程中,溶液的pH减小 |
B.c(H2C2O4 )+c( )+c( )+c( )=1mol·L-1 )=1mol·L-1 |
| C.溶液中,l mol·L-1<c(H+)<2 mol·L-1 |
D.溶液中,H2C2O4 电离出的c(H+):c( ) =2:1 ) =2:1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列说法正确的是
| A.向浓度均为0.1mol/L的NaCl和Na2SiO3溶液中分别滴加酚酞,NaCl溶液不变色,Na2SiO3溶液变成红色,说明非金属性:Si |
| B.为处理锅炉水垢中的CaSO4,可用饱和碳酸钠溶液浸泡 |
| C.稀释0.1mol/LCH3COOH溶液,溶液中各离子的浓度均减小 |
| D.已知Ksp(BaSO4)sp(BaCO3),则在硫酸钡悬浊液中加入碳酸钠粉末搅拌,一定没有碳酸钡生成 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下,下列关于电解质溶液中的比值问题说法正确的是
A.pH=11的NaOH和pH=3CH3COOH等体积混合: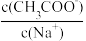 <1 <1 |
B.向Ba(OH)2和氨水的混合液中加入盐酸: 增大 增大 |
C.向CaCO3和CaSO4的悬浊液中加入少量Na2CO3固体: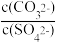 增大 增大 |
D.向CH3COONa溶液中加水稀释: 减小 减小 |
您最近一年使用:0次



