已知相同条件下,物质具有的能量越低,物质越稳定。常温常压时,红磷比白磷稳定,在下列反应中:
①4P(白磷,s)+5O2(g) = 2P2O5(s) △H= -a kJ/mol
②4P(红磷,s)+5O2(g) = 2P2O5(s) △H= -bkJ/mol
若a、b均大于零,则a和b的关系为(△H小于零,代表反应放热)
①4P(白磷,s)+5O2(g) = 2P2O5(s) △H= -a kJ/mol
②4P(红磷,s)+5O2(g) = 2P2O5(s) △H= -bkJ/mol
若a、b均大于零,则a和b的关系为(△H小于零,代表反应放热)
| A.a<b | B.a=b | C.a>b | D.无法确定 |
更新时间:2017-08-21 22:22:43
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知:①H2 (g) + Se (g)  H2Se (g) +87.48kJ ②Se (g) → Se (s) +102.17kJ; 下列选项正确的是
H2Se (g) +87.48kJ ②Se (g) → Se (s) +102.17kJ; 下列选项正确的是

 H2Se (g) +87.48kJ ②Se (g) → Se (s) +102.17kJ; 下列选项正确的是
H2Se (g) +87.48kJ ②Se (g) → Se (s) +102.17kJ; 下列选项正确的是
| A.H2 (g) + Se (s)的总能量对应图中线段 b |
| B.相同物质的量的 Se,Se(s)的能量高于 Se(g) |
| C.1mol Se (g)中通入 1mol H2(g),反应放热 87.48kJ |
D.H2 (g) + S (g)  H2S (g) +QkJ ,Q< 87.48kJ H2S (g) +QkJ ,Q< 87.48kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:2H2(g)+O2(g)=2H2O(g)  H=-483.6kJ·mol-1
H=-483.6kJ·mol-1
 H=-483.6kJ·mol-1
H=-483.6kJ·mol-1
| A.H2的燃烧热是241.8kJ/mol |
| B.破坏1molH-O键需要的能量是463.4kJ |
C.2H2(g)+O2(g)=2H2O(l)  H<-483.6·mob H<-483.6·mob |
| D.H2(g)中的H-H键比H2O(g)中的H-O键弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关叙述正确的是
| A.CuSO4(aq)+Fe(s)=FeSO4(aq)+Cu(s) △H其他条件不变,增大反应物的量,△H也发生相应的变化 |
| B.相同条件下,若1 mol O、1 mol O2所具有的能量分别为E1、E2,则2E1<E2 |
| C.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同 |
| D.H+(aq)+OH-(aq)=H2O(l) △H=-57.3 kJ•mol-1,则1 mol NaOH固体与足量稀盐酸充分混合放出57.3 kJ热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上合成尿素的反应为 ,其能量变化如图所示。已知:
,其能量变化如图所示。已知: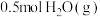 变为
变为 时放出的热量是20.4kJ。
时放出的热量是20.4kJ。

下列热化学方程式错误的是
 ,其能量变化如图所示。已知:
,其能量变化如图所示。已知: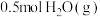 变为
变为 时放出的热量是20.4kJ。
时放出的热量是20.4kJ。
下列热化学方程式错误的是
A.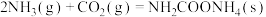 ∆H=-159.47kJ∙mol-1 ∆H=-159.47kJ∙mol-1 |
B. ∆H=+72.49kJ∙mol-1 ∆H=+72.49kJ∙mol-1 |
C. ∆H=-86.98kJ∙mol-1 ∆H=-86.98kJ∙mol-1 |
D.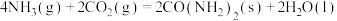 ∆H=-173.96kJ∙mol-1 ∆H=-173.96kJ∙mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】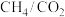 催化重整的反应为
催化重整的反应为
①

其中,积炭是导致催化剂失活的主要原因。产生积炭的反应有:
②
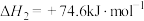
③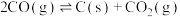
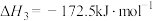
科研人员研究压强对催化剂活性的影响:在1073K时,将恒定组成的 、
、 混合气体,以恒定流速通过反应器,测得数据如下。
混合气体,以恒定流速通过反应器,测得数据如下。不正确 的是
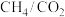 催化重整的反应为
催化重整的反应为①


其中,积炭是导致催化剂失活的主要原因。产生积炭的反应有:
②

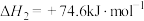
③
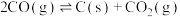
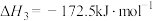
科研人员研究压强对催化剂活性的影响:在1073K时,将恒定组成的
 、
、 混合气体,以恒定流速通过反应器,测得数据如下。
混合气体,以恒定流速通过反应器,测得数据如下。
A.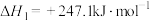 |
| B.压强越大,Ra降低越快,其主要原因是反应①平衡逆向移动 |
C.保持其他条件不变,适当增大投料时 ,可减缓Ra的衰减 ,可减缓Ra的衰减 |
D.研究表明“通入适量 有利于重整反应”,因为 有利于重整反应”,因为 能与C反应并放出热量 能与C反应并放出热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】二氧化碳加氢制甲烷过程中的主要反应为
CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H=-164.7kJ•mol-1
CO2(g)+H2(g)=CO(g)+H2O(g) △H=41.2kJ•mol-1
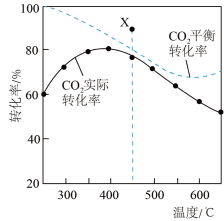
在密闭容器中,1.01×105Pa、n起始(CO2):n起始(H2)=1:4时,CO2平衡转化率、在催化剂作用下反应相同时间所测得的CO2实际转化率随温度的变化如题图所示。CH4的选择性可表示为 ×100%。下列说法正确的是
×100%。下列说法正确的是
CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H=-164.7kJ•mol-1
CO2(g)+H2(g)=CO(g)+H2O(g) △H=41.2kJ•mol-1
在密闭容器中,1.01×105Pa、n起始(CO2):n起始(H2)=1:4时,CO2平衡转化率、在催化剂作用下反应相同时间所测得的CO2实际转化率随温度的变化如题图所示。CH4的选择性可表示为
 ×100%。下列说法正确的是
×100%。下列说法正确的是
| A.反应2CO(g)+2H2(g)=CO2(g)+CH4(g)的焓变△H=-205.9kJ•mol-1 |
| B.CH4的平衡选择性随着温度的升高而增加 |
| C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃ |
D.450℃时,提高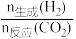 的值或增大压强,均能使CO2平衡转化率达到X点的值 的值或增大压强,均能使CO2平衡转化率达到X点的值 |
您最近一年使用:0次



