有一包粉末可能含有K+、Fe3+、Al3+、Cl-、 、
、 中的若干种,现进行以下实验:
中的若干种,现进行以下实验:
(1)取少量固体,加入稀硝酸搅拌,固体全部溶解,没有气体放出;
(2)向(1)溶液中加入一定量Ba(OH)2溶液,生成有色沉淀,过滤后在滤液中加入稀硝酸酸化,然后滴入AgNO3溶液,有白色沉淀生成;
(3)取(2)中的有色沉淀加入足量的稀盐酸后,沉淀全部溶解;
(4)重新取少量固体加入适量蒸馏水搅拌后,固体全部溶解,得到澄清溶液;
(5)向(4)的溶液中加入氨水使溶液呈碱性,有沉淀生成,过滤,往得到的沉淀中加入过量的NaOH溶液,沉淀减少。
根据上述实验,这包粉末中一定不含有的离子是________________ ,肯定含有的离子是___________ ,不能确定是否含有的离子是______________ ,可通过______________ 来进一步确定该离子。
 、
、 中的若干种,现进行以下实验:
中的若干种,现进行以下实验:(1)取少量固体,加入稀硝酸搅拌,固体全部溶解,没有气体放出;
(2)向(1)溶液中加入一定量Ba(OH)2溶液,生成有色沉淀,过滤后在滤液中加入稀硝酸酸化,然后滴入AgNO3溶液,有白色沉淀生成;
(3)取(2)中的有色沉淀加入足量的稀盐酸后,沉淀全部溶解;
(4)重新取少量固体加入适量蒸馏水搅拌后,固体全部溶解,得到澄清溶液;
(5)向(4)的溶液中加入氨水使溶液呈碱性,有沉淀生成,过滤,往得到的沉淀中加入过量的NaOH溶液,沉淀减少。
根据上述实验,这包粉末中一定不含有的离子是
更新时间:2017-08-24 14:56:40
|
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】有三种物质A、B、C,其中一种是碱,其余两种是盐。它们均可溶于水,电离只产生下表中的离子:
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以与C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请回答下列问题:
(1)X的名称是___________ ,X___________ (填“是”或“不是”)电解质。
(2)C在水中的电离方程式为___________ 。鉴别C溶液中阴离子的实验操作方法___________ 。
(3)写出以下水溶液中反应的离子方程式。
①A溶液与B溶液反应生成无色气体X:___________ 。
②B溶液与C溶液反应至溶液呈中性:___________ 。
| 阳离子 | Na+、H+、Ba2+ |
| 阴离子 | OH–、CO 、SO 、SO |
①A溶液与B溶液反应生成无色气体X,气体X可以与C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请回答下列问题:
(1)X的名称是
(2)C在水中的电离方程式为
(3)写出以下水溶液中反应的离子方程式。
①A溶液与B溶液反应生成无色气体X:
②B溶液与C溶液反应至溶液呈中性:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】某小组探究CuCl2溶液和Na2SO3溶液反应的主要产物,开展如下活动。
[实验准备]
(1)用亚硫酸钠固体配制100mL0.2mol·L-1Na2SO3溶液,下列仪器中无需使用的有___________ (填名称)。
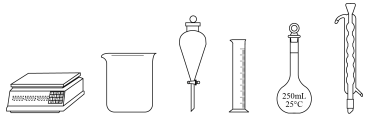
(2)检验亚硫酸钠溶液在空气中是否变质所需的试剂为___________ 。
[理论预测]
(3)预测3中反应的离子方程式为___________ 。
[实验探究]
实验1
取1mL0.2mol·L-1Na2SO3溶液和2mL0.2mol·L-1CuCl2溶液混合,立即生成橙黄色沉淀,3min后沉淀颜色变浅并伴有少量白色沉淀产生振荡1min沉淀全部变为白色。
为证明实验1产生的白色沉淀为CuCl,需鉴定沉淀中含Cl-、Cu+,其中鉴定含Cu+的实验设计如下:
实验2
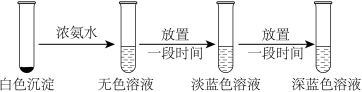
(4)已知[Cu(NH3)2]+、[Cu(NH3)4]2+在水中分别呈无色和深蓝色,实验2总反应的离子方程式为_____ 。
[进一步探究]
查阅资料获知橙黄色沉淀可能为xCuSO3·yCu2SO3·zH2O,在实验1获得橙黄色沉淀后,立即离心分离并洗涤。为探究其组成进行如下实验:
实验3

(5)离心分离的目的是加快过滤速度,防止___________ 。
(6)已知2Cu2++4I-=2CuI↓+I2,实验3___________ (选填“能”或“不能”)证明橙黄色沉淀中含有Cu2+和 。
。
为验证橙黄色沉淀转化为CuCl的原因可能是Cl-提高了Cu2+的氧化性,进行如下实验(已知装置中物质氧化性与还原性强弱差异越大,电压越大)。
实验4
(7)①表中X为___________ 。
②能证实实验结论的实验现象为___________ 。
[解释和结论]
综上所述,Cu2+与 发生复分解反应速率较快,发生氧化还原反应趋势更大。
发生复分解反应速率较快,发生氧化还原反应趋势更大。
[实验准备]
(1)用亚硫酸钠固体配制100mL0.2mol·L-1Na2SO3溶液,下列仪器中无需使用的有

(2)检验亚硫酸钠溶液在空气中是否变质所需的试剂为
[理论预测]
| 预测 | 主要产物 | 主要实验现象 |
| 1 | CuSO3 | 生成绿色沉淀 |
| 2 | Cu(OH)2、SO2 | 溶液中出现蓝色沉淀,伴有刺激性气味气体产生 |
| 3 | Cu2SO3 | 生成红色沉淀 |
| 4 | CuCl | 生成白色沉淀 |
[实验探究]
实验1
取1mL0.2mol·L-1Na2SO3溶液和2mL0.2mol·L-1CuCl2溶液混合,立即生成橙黄色沉淀,3min后沉淀颜色变浅并伴有少量白色沉淀产生振荡1min沉淀全部变为白色。
为证明实验1产生的白色沉淀为CuCl,需鉴定沉淀中含Cl-、Cu+,其中鉴定含Cu+的实验设计如下:
实验2

(4)已知[Cu(NH3)2]+、[Cu(NH3)4]2+在水中分别呈无色和深蓝色,实验2总反应的离子方程式为
[进一步探究]
查阅资料获知橙黄色沉淀可能为xCuSO3·yCu2SO3·zH2O,在实验1获得橙黄色沉淀后,立即离心分离并洗涤。为探究其组成进行如下实验:
实验3

(5)离心分离的目的是加快过滤速度,防止
(6)已知2Cu2++4I-=2CuI↓+I2,实验3
 。
。为验证橙黄色沉淀转化为CuCl的原因可能是Cl-提高了Cu2+的氧化性,进行如下实验(已知装置中物质氧化性与还原性强弱差异越大,电压越大)。
实验4
| 装置 | 试剂a | 试剂b | 电压表读数 |
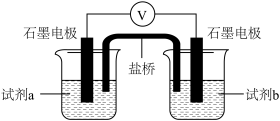 | 0.2mol·L-1Na2SO3溶液 | 0.2mol·L-1CuCl2 溶液 | V1 |
| 0.2mol·L-1Na2SO3溶液 | X | V2 |
②能证实实验结论的实验现象为
[解释和结论]
综上所述,Cu2+与
 发生复分解反应速率较快,发生氧化还原反应趋势更大。
发生复分解反应速率较快,发生氧化还原反应趋势更大。
您最近一年使用:0次
【推荐3】某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1 mol/L。
某同学欲探究废水的组成,进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
②取少量溶液,加入KSCN溶液无明显变化。
③另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
④向③中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由①、②、③判断,溶液中一定不含有的阴离子是_______ ,一定不含有的阳离子是_______ (写离子符号)。
(2)③中加入少量盐酸生成无色气体的离子方程式是_______ ,④中生成白色沉淀的离子方程式是_______ 。
(3)该同学最终确定原溶液中所含阴离子是_______ ,阳离子是_______ (写离子符号)。
(4)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为_______ g。
| 阳离子 | K+、Mg2+、Fe3+、Al3+、Fe2+ |
| 阴离子 | Cl-、 、 、 、 、 、 、 |
①用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
②取少量溶液,加入KSCN溶液无明显变化。
③另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
④向③中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由①、②、③判断,溶液中一定不含有的阴离子是
(2)③中加入少量盐酸生成无色气体的离子方程式是
(3)该同学最终确定原溶液中所含阴离子是
(4)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为
您最近一年使用:0次



