1.钒的化合物常用于制作催化剂和新型电池。回答下列问题:
27.金属钒可由铝热反应制得。已知25℃、101 kPa时,
4A1(s)+3O
2(g)=2Al
2O
3(s)
△H
1=a kJ·mol
-14V(s) +5O
2(g)=2V
2O
5(s)
△H
2=b kJ·mol
-1则用铝热反应冶炼金属V(s)的热化学方程式为
_____________________。
28.V
2O
5为橙黄至砖红色固体,无味、有毒,微溶于水,是许多有机和无机反应的催化剂。下图表示的是25℃时,部分含钒微粒的存在形式、浓度和存在的pH范围(其余可溶性微粒均未标出),图中“[V]”表示含钒微粒的浓度,虚线表示[V]或pH的范围尚未准确确定。
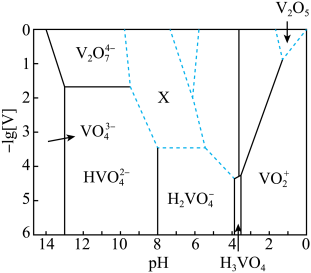
①V
2O
5溶于足量2mol • L
-1NaOH溶液中,发生反应的离子方程式为
_________________,向反应后的溶液中,滴加硫酸溶液至过量(pH<1)的过程中,开始溶液保持澄清,滴加一段时间后,观察到有橙黄色沉淀产生,继续滴加硫酸溶液,沉淀又消失。则沉淀消失过程中发生反应的化学方程式为
_______________。
②上述滴加硫酸溶液的过程中,先后发生如下反应:
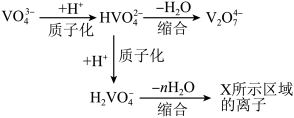
则“X所示区域溶液中的离子”不可能是
___________(填序号);
a.V
3O

b.V
4O
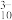
c. V
4O
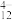
29.V
2O
5是反应2SO
2+O
2
2SO
3的催化剂。其他条件不变,加入V
2O
5后,该反应的速率加快的原因是
_______________;恒温恒压下,加入V
2O
5,该反应的平衡常数
________________(填“增大”、 “减小”或“不变”);
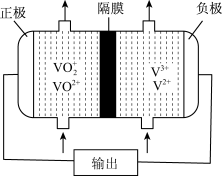
30.下图所示为可充电的全钒液流电池构造示意图,该电池中的隔膜只允许H
+通过。电池放电时,负极区溶液的pH将
_____________(填“增大”、“减小”或“不变”),电池充电时,阳极的电极反应式为
_____________________。