22. 某同学欲配制80mL1.00mol•L
-1NaOH溶液,配制过程如下:
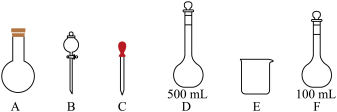
(1)选择适当仪器。在下列给出的玻璃仪器中,不需要用到的是
___。
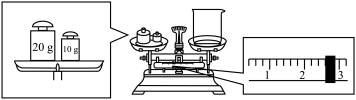
(2)先用托盘天平称量烧杯的质量,天平平衡后的状态如图,则烧杯的实际质量为
___g。要完成本实验,该同学应称取
___g(烧杯质量不计算在内)NaOH固体,再在烧杯中用适量蒸馏水溶解、冷却。
(3)将烧杯中的溶液转移至
___ (填仪器名称,下同)中,并用少量蒸馏水洗涤烧杯内壁及玻璃棒2
〜3次,洗涤液也注入该仪器中。
(4)继续加蒸馏水至离刻度线1
〜2cm处,改用
___滴加蒸馏水至凹液面最低处与刻度线相切。
(5)盖上瓶塞,上下颠倒
___ (填操作名称),将所配溶液转移至指定试剂瓶中,贴上标签。
(6)下列操作使所配物质的量浓度偏大的有
___(填写字母)。
A.称量时用了生锈的砝码;
B.将NaOH放在托盘天平的右盘上称量(使用游码);
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中;
D.往容量瓶转移时,有少量液体溅出;
E.定容时俯视刻度线;
F.容量瓶未干燥即用来配制溶液;
G.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。