18. 某同学查阅教材上的溶解性表时发现,CuCO
3对应的为“—”,表示不存在或遇水就分解。已知铜离子的常见沉淀为Cu(OH)
2(蓝色)、Cu
2(OH)
2SO
4(蓝色)、Cu
2(OH)
2CO
3(绿色)等,它们均不含结晶水。为了探究CuSO
4和Na
2CO
3反应产物的成分,该同学按以下实验方法制备了两种沉淀,并设计了探究沉淀成分的实验。
取2个小烧杯和2个锥形瓶,在每个烧杯里加入50mL0.5mol/L的CuSO
4溶液,在锥形瓶里分别加入40mL 和50mL0.5mol/LNa
2CO
3溶液,置于70℃水中水浴加热,然后将CuSO
4溶液加入到Na
2CO
3溶液中,继续水浴,均有气泡产生,几分钟后分别得到蓝绿色和绿色沉淀。过滤、洗涤、干燥,得到两份固体。
I.对蓝绿色沉淀成分的探究。
通过右边实验证实,沉淀中含有Cu
2(OH)
2CO
3和Cu
2(OH)
2SO
4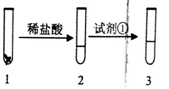
(1)证明有Cu
2(OH)
2CO
3存在的现象为
____________;
(2)试剂①为
__________,证明有Cu
2(OH)
2SO
4存在的现象为
______________。
II.对绿色沉淀成分的探究
重复I实验,发现没有SO
42-存在,有Cu
2(OH)
2CO
3存在;
通过下列实验证实,沉淀中只有Cu
2(OH)
2CO
3
(3)该同学想通过测量固体分解所得气体的质量来确定沉淀的成分,按上述思路组装好装置,加入相应的药品,并指出所加药品的目的
___________。
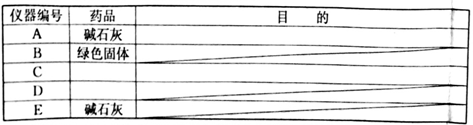
(4)按照该同学的设计思路,只需测定某两个装置的质量变化,即△m
_____:△m
______=
_______时(括号中填写装置的序号)就可确定固体是Cu
2(OH)
2CO
3。
(5)结论:n(Cu
2+):n(CO
32-)>1时,所得固体产物有Cu
2(OH)
2CO
3和Cu
2(OH)
2SO
4;n(Cu
2+):n(CO
32-)≤1时,所得固体产物全部是Cu
2(OH)
2CO
3,生成该沉淀发生反应的离子方程式为:
____________。