描述下列反应的现象并写出反应的离子方程式。
(1)向FeCl3溶液中滴加NaOH溶液,现象:__________________ ,离子方程式:____________________
(2)向NaHCO3溶液中滴加稀H2SO4,现象:__________________ ,离子方程式:__________________
(3)稀HNO3和Ba(OH)2溶液混合,现象:__________________ ,离子方程式:____________________
(4)比较:上述三个离子反应发生的条件的不同点是______________________ ;相同点是________________
(1)向FeCl3溶液中滴加NaOH溶液,现象:
(2)向NaHCO3溶液中滴加稀H2SO4,现象:
(3)稀HNO3和Ba(OH)2溶液混合,现象:
(4)比较:上述三个离子反应发生的条件的不同点是
2017高一·全国·课时练习 查看更多[2]
更新时间:2017-11-27 08:01:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
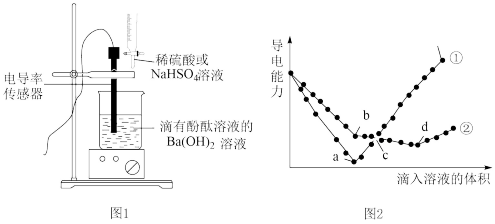
【推荐1】已知:溶液中自由移动的离子浓度越大,导电能力就越强。图1是向20mL 0.01mol/L 溶液(含酚酞)中滴加浓度均为0.02mol/L稀
溶液(含酚酞)中滴加浓度均为0.02mol/L稀 和
和 溶液的装置示意图。图2表示溶液导电能力随滴入
溶液的装置示意图。图2表示溶液导电能力随滴入 溶液(①)和
溶液(①)和 (②)溶液体积V(mL)的关系曲线。完成下列填空:
(②)溶液体积V(mL)的关系曲线。完成下列填空:
(1)本实验的反应本质是离子反应,以下也属于离子反应是_______ 。(选填编号)
A. 还原CuO B.Zn与稀硫酸制备
还原CuO B.Zn与稀硫酸制备
C. 高温分解 D.
高温分解 D. 溶于NaOH溶液生成
溶于NaOH溶液生成
E.甲烷( )的燃烧 F.
)的燃烧 F. 除去粗盐中的某些可溶性杂质
除去粗盐中的某些可溶性杂质
(2)写出曲线①的离子方程式:_______ 。
(3)曲线①测定过程中烧杯中的现象是_______ 。a点对应溶液的体积为_______ mL。
(4)曲线②中,____ 点对应的溶液呈中性,_____ 点对应的溶液中 恰好完全沉淀。
恰好完全沉淀。
(5)曲线②的c点溶液所含离子有_______ ,其中离子浓度最大的是_______ 。
 溶液(含酚酞)中滴加浓度均为0.02mol/L稀
溶液(含酚酞)中滴加浓度均为0.02mol/L稀 和
和 溶液的装置示意图。图2表示溶液导电能力随滴入
溶液的装置示意图。图2表示溶液导电能力随滴入 溶液(①)和
溶液(①)和 (②)溶液体积V(mL)的关系曲线。完成下列填空:
(②)溶液体积V(mL)的关系曲线。完成下列填空:
(1)本实验的反应本质是离子反应,以下也属于离子反应是
A.
 还原CuO B.Zn与稀硫酸制备
还原CuO B.Zn与稀硫酸制备
C.
 高温分解 D.
高温分解 D. 溶于NaOH溶液生成
溶于NaOH溶液生成
E.甲烷(
 )的燃烧 F.
)的燃烧 F. 除去粗盐中的某些可溶性杂质
除去粗盐中的某些可溶性杂质(2)写出曲线①的离子方程式:
(3)曲线①测定过程中烧杯中的现象是
(4)曲线②中,
 恰好完全沉淀。
恰好完全沉淀。(5)曲线②的c点溶液所含离子有
您最近一年使用:0次
【推荐2】按下列要求填空
①向碳酸氢钙溶液中加入少量氢氧化钠溶液的离子方程式:________________________ 。
氯化铝溶液与NaHCO3溶液混合的离子方程式:______________________ 。
②在KClO3+ 6HCl =" KCl" + 3Cl2↑ + 3H2O的反应中,被氧化的氯原子与被还原的氯原子的物质的量之比是_______________ 。
③强酸性的未知无色溶液中可能含有大量的Cl-、S2-、NO3-、CO32-、NH4+、Cu2+、Fe3+、Ag+等,现已检出有Ag+,你认为其中____________ 离子还需要鉴定是否存在,请写出检验该离子的离子方程式_____________________ 。
④某化合物的相对分子质量为m,在t℃时AmL该化合物的饱和溶液为Bg,将其蒸干后得到固体Cg。该化合物在t℃时的溶解度为_______________ g,该饱和溶液中溶质的物质的量浓度为__________________ mol/L。
①向碳酸氢钙溶液中加入少量氢氧化钠溶液的离子方程式:
氯化铝溶液与NaHCO3溶液混合的离子方程式:
②在KClO3+ 6HCl =" KCl" + 3Cl2↑ + 3H2O的反应中,被氧化的氯原子与被还原的氯原子的物质的量之比是
③强酸性的未知无色溶液中可能含有大量的Cl-、S2-、NO3-、CO32-、NH4+、Cu2+、Fe3+、Ag+等,现已检出有Ag+,你认为其中
④某化合物的相对分子质量为m,在t℃时AmL该化合物的饱和溶液为Bg,将其蒸干后得到固体Cg。该化合物在t℃时的溶解度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列物质:① 晶体,②铜丝,③
晶体,②铜丝,③ ,④二氧化硫,⑤
,④二氧化硫,⑤ 固体,⑥
固体,⑥ 固体,⑦水,⑧稀硝酸,⑨蔗糖。
固体,⑦水,⑧稀硝酸,⑨蔗糖。
(1)按物质的分类方法,填写表格的空白处(填序号):
(2)某学习小组为证实 溶液和
溶液和 溶液的反应是离子反应,设计了如下实验。请把该实验报告补充完整。
溶液的反应是离子反应,设计了如下实验。请把该实验报告补充完整。
【实验原理】溶液的导电性由溶液中离子的浓度及离子电荷数决定,观察_______ ,据此判断溶液中自由移动的离子浓度的变化,从而证明反应是离子反应。
【实验装置】如图所示。
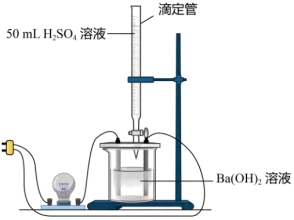
【实验过程与记录】
(3)书写下列两种情况的离子方程式。
①向 溶液中,逐滴加入
溶液中,逐滴加入 溶液至恰好完全沉淀:
溶液至恰好完全沉淀:_______ 。
②向 溶液中,逐滴加入
溶液中,逐滴加入 溶液至溶液显中性:
溶液至溶液显中性:_______ 。
 晶体,②铜丝,③
晶体,②铜丝,③ ,④二氧化硫,⑤
,④二氧化硫,⑤ 固体,⑥
固体,⑥ 固体,⑦水,⑧稀硝酸,⑨蔗糖。
固体,⑦水,⑧稀硝酸,⑨蔗糖。(1)按物质的分类方法,填写表格的空白处(填序号):
| 分类标准 | 能导电的物质 | 电解质 | 弱电解质 | 非电解质 | 既不是电解质也不是非电解质 |
| 属于该类的物质 |
(2)某学习小组为证实
 溶液和
溶液和 溶液的反应是离子反应,设计了如下实验。请把该实验报告补充完整。
溶液的反应是离子反应,设计了如下实验。请把该实验报告补充完整。【实验原理】溶液的导电性由溶液中离子的浓度及离子电荷数决定,观察
【实验装置】如图所示。

【实验过程与记录】
| 实验步骤 | 实验现象 | 实验结论 |
连接好装置,向烧杯中加入25mL一定浓度的 溶液和2滴酚酞溶液,逐滴滴加一定浓度的 溶液和2滴酚酞溶液,逐滴滴加一定浓度的 溶液直至过量,边滴边振荡 溶液直至过量,边滴边振荡 |  溶液和 溶液和 溶液的反应是离子反应 溶液的反应是离子反应 |
(3)书写下列两种情况的离子方程式。
①向
 溶液中,逐滴加入
溶液中,逐滴加入 溶液至恰好完全沉淀:
溶液至恰好完全沉淀:②向
 溶液中,逐滴加入
溶液中,逐滴加入 溶液至溶液显中性:
溶液至溶液显中性:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列十种物质:①HCl②CH3COOH③SO2④Na2CO3⑤CCl4⑥Ca(OH)2⑦Fe⑧NH3•H2O⑨空气⑩K2SO4
(1)上述物质中属于弱电解质的是_______ (填序号,下同),属于非电解质的是_______ 。
(2)②在水溶液中的电离方程式为_______ 。
(3)分离⑤和水的混合物所用的方法是_______ 。
(4)写出①和⑦反应的离子方程式_______ 。
(5)检验⑩中阳离子所用的方法是_______ ,现象是_______ 。
(6)已知SO2是酸性氧化物,将其通入⑥中,写出对应的化学方程式_______ 。
(7)④与二氧化硅(SiO2)在高温下发生化学反应,生成一种新的盐和二氧化碳。写出该反应的化学方程式_______ 。
(1)上述物质中属于弱电解质的是
(2)②在水溶液中的电离方程式为
(3)分离⑤和水的混合物所用的方法是
(4)写出①和⑦反应的离子方程式
(5)检验⑩中阳离子所用的方法是
(6)已知SO2是酸性氧化物,将其通入⑥中,写出对应的化学方程式
(7)④与二氧化硅(SiO2)在高温下发生化学反应,生成一种新的盐和二氧化碳。写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据下列反应现象,回答问题:
(1)向氯化铜溶液中滴加氢氧化钠溶液,其现象是________________________________ ,离子反应方程式是________________________________ 。
(2)向碳酸氢钠溶液中滴加稀硫酸,其现象是________________________________________ ,离子反应方程式是____________________________________ 。
(3)稀硝酸与氢氧化钾溶液混合,其现象是_________________________________________ ,离子反应方程式是______________________________________ 。
(4)上述三个反应均属于______________ 反应(填基本反应类型),反应发生的条件的不同点是第一个生成________________ ,第二个生成______________ ,第三个生成______________ ;相同点是_____________________ 。
(1)向氯化铜溶液中滴加氢氧化钠溶液,其现象是
(2)向碳酸氢钠溶液中滴加稀硫酸,其现象是
(3)稀硝酸与氢氧化钾溶液混合,其现象是
(4)上述三个反应均属于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据所学知识,回答下列问题:
(1)高铁酸钠(Na2FeO4)可作为高效、多功能水处理剂,其摩尔质量是__________ 。高铁酸钠可与水反应生成Fe(OH)3胶体、氢氧化钠和氧气,写出相应的离子方程式:_____________ 。
(2)戴维通过电解法首先制得了金属钠,随后几十年内,工业上采用铁粉和氢氧化钠高温熔融的方法制得钠蒸气,同时获得Fe3O4和氢气。写出该反应的化学方程式_____________ ,该反应中属于电解质但不属于氧化物的物质是________________ (填化学式),若制得22.4L(折算为标准状况下)钠蒸气,转移电子的数目为________________ 。
(3)漂白粉常用于饮水、污水、排泄物及被污染的环境消毒,其主要成分是氯化钙和次氯酸钙[Ca(ClO)2],有效成分为次氯酸钙。为测得某漂白粉的有效成分含量,称取A g漂白粉样品溶解,往所得溶液中通入CO2至不再产生沉淀为止,反应的化学方程式为Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,若反应生成次氯酸(HClO)的物质的量为Kmol,则该漂白粉中有效成分的质量分数为___________ %(用含A、K的式子表示)。
(1)高铁酸钠(Na2FeO4)可作为高效、多功能水处理剂,其摩尔质量是
(2)戴维通过电解法首先制得了金属钠,随后几十年内,工业上采用铁粉和氢氧化钠高温熔融的方法制得钠蒸气,同时获得Fe3O4和氢气。写出该反应的化学方程式
(3)漂白粉常用于饮水、污水、排泄物及被污染的环境消毒,其主要成分是氯化钙和次氯酸钙[Ca(ClO)2],有效成分为次氯酸钙。为测得某漂白粉的有效成分含量,称取A g漂白粉样品溶解,往所得溶液中通入CO2至不再产生沉淀为止,反应的化学方程式为Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,若反应生成次氯酸(HClO)的物质的量为Kmol,则该漂白粉中有效成分的质量分数为
您最近一年使用:0次



