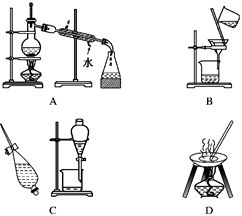
下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D 填入适当的空格中。
(1)除去Ca(OH)2溶液中悬浮的CaCO3______________________________ ;
(2)从碘水中提取碘___________________________________________ ;
(3)用自来水制取蒸馏水_______________________________________ ;
(4)分离植物油和水___________________________________________ ;
(5)除去粗盐中的泥沙__________________________________________ ;
(6)与海水晒盐原理相符的是__________________________________ 。
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D 填入适当的空格中。
(1)除去Ca(OH)2溶液中悬浮的CaCO3
(2)从碘水中提取碘
(3)用自来水制取蒸馏水
(4)分离植物油和水
(5)除去粗盐中的泥沙
(6)与海水晒盐原理相符的是
11-12高三·辽宁盘锦·阶段练习 查看更多[8]
(已下线)【南昌新东方】11. 南昌一中 直升班 项金辉.河北省邢台市第八中学2019-2020学年高一上学期第二次月考化学试题湖南省双峰县第一中学2019-2020学年高一上学期第一次月考化学试题2018-2019学年高一人教版化学必修1:第一章从实验学化学练习题辽宁省大连市普兰店区第二中学2017-2018学年高一上学期期末考试化学试题山西省实验中学2017-2018学年高一上学期10月月考化学试题2015-2016学年云南省保山市腾冲六中高一上学期期末化学试卷(已下线)2013届辽宁省盘锦市二中高三第一次阶段考试化学试卷
更新时间:2017-10-21 14:28:29
|
【知识点】 物质分离、提纯的常见物理方法
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室以软锰矿粉(含 及少量Fe、Al、Si、Mg等的氧化物)为原料制备
及少量Fe、Al、Si、Mg等的氧化物)为原料制备 ,其实验过程可表示为
,其实验过程可表示为

(1)浸取。在如图的实验装置中,搅拌下,使一定量软锰矿粉与 溶液、
溶液、 溶液充分反应,
溶液充分反应, 转化为
转化为 的化学方程式为
的化学方程式为___________ 。软锰矿粉与 、
、 溶液的加料方式是
溶液的加料方式是___________ ;加料完成后,以一定速率搅拌反应,提高锰元素浸出率的方法还有___________ 。

(2)除杂。对已经除去Fe、Al、Si的 溶液,可通过萃取、反萃取等过程除去溶液中的
溶液,可通过萃取、反萃取等过程除去溶液中的 、
、 。已知:
。已知: 被萃取剂HA萃取的原理可表示为
被萃取剂HA萃取的原理可表示为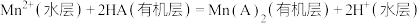 ;
; 的萃取率(
的萃取率( )
) 。
。
①萃取时,在一定温度和pH下, 在有机层和水层中的浓度之比称为分配比(用D表示,为常数)。若25℃、
在有机层和水层中的浓度之比称为分配比(用D表示,为常数)。若25℃、 时,分配比
时,分配比 ,现用20mLHA萃取100mL含
,现用20mLHA萃取100mL含 溶液,按两种方法进行萃取:Ⅰ.用20mLHA萃取一次;Ⅱ.分两次萃取,每次用10mLHA,试通过计算说明哪种方法更好?
溶液,按两种方法进行萃取:Ⅰ.用20mLHA萃取一次;Ⅱ.分两次萃取,每次用10mLHA,试通过计算说明哪种方法更好?_______ (写出计算过程)
②反萃取是利用稀硫酸将有机层中的 转移到水层,需将稀硫酸和有机层共同加入到
转移到水层,需将稀硫酸和有机层共同加入到_______ (填仪器名称)中进行实验操作。为使 尽可能多地发生上述转移,应选择的实验条件或采取的操作有
尽可能多地发生上述转移,应选择的实验条件或采取的操作有_______ (填序号)。
A.适当提高 浓度B.加足量蒸馏水C.用适量稀硫酸分多次反萃取D.充分振荡
浓度B.加足量蒸馏水C.用适量稀硫酸分多次反萃取D.充分振荡
(3)制取 晶体。补充完整制取
晶体。补充完整制取 晶体的实验方案:向含有少量
晶体的实验方案:向含有少量 、
、 的
的 溶液中,
溶液中,_______ ,在真空干燥箱中低温干燥,得到 。(已知:
。(已知: 、
、 在
在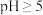 时完全转化为氢氧化物沉淀:
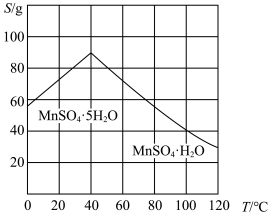
时完全转化为氢氧化物沉淀: 的溶解度曲线如图所示;实验中须使用的试剂有:
的溶解度曲线如图所示;实验中须使用的试剂有: 粉末、无水乙醇)
粉末、无水乙醇)
 及少量Fe、Al、Si、Mg等的氧化物)为原料制备
及少量Fe、Al、Si、Mg等的氧化物)为原料制备 ,其实验过程可表示为
,其实验过程可表示为
(1)浸取。在如图的实验装置中,搅拌下,使一定量软锰矿粉与
 溶液、
溶液、 溶液充分反应,
溶液充分反应, 转化为
转化为 的化学方程式为
的化学方程式为 、
、 溶液的加料方式是
溶液的加料方式是
(2)除杂。对已经除去Fe、Al、Si的
 溶液,可通过萃取、反萃取等过程除去溶液中的
溶液,可通过萃取、反萃取等过程除去溶液中的 、
、 。已知:
。已知: 被萃取剂HA萃取的原理可表示为
被萃取剂HA萃取的原理可表示为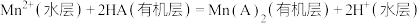 ;
; 的萃取率(
的萃取率( )
) 。
。①萃取时,在一定温度和pH下,
 在有机层和水层中的浓度之比称为分配比(用D表示,为常数)。若25℃、
在有机层和水层中的浓度之比称为分配比(用D表示,为常数)。若25℃、 时,分配比
时,分配比 ,现用20mLHA萃取100mL含
,现用20mLHA萃取100mL含 溶液,按两种方法进行萃取:Ⅰ.用20mLHA萃取一次;Ⅱ.分两次萃取,每次用10mLHA,试通过计算说明哪种方法更好?
溶液,按两种方法进行萃取:Ⅰ.用20mLHA萃取一次;Ⅱ.分两次萃取,每次用10mLHA,试通过计算说明哪种方法更好?②反萃取是利用稀硫酸将有机层中的
 转移到水层,需将稀硫酸和有机层共同加入到
转移到水层,需将稀硫酸和有机层共同加入到 尽可能多地发生上述转移,应选择的实验条件或采取的操作有
尽可能多地发生上述转移,应选择的实验条件或采取的操作有A.适当提高
 浓度B.加足量蒸馏水C.用适量稀硫酸分多次反萃取D.充分振荡
浓度B.加足量蒸馏水C.用适量稀硫酸分多次反萃取D.充分振荡(3)制取
 晶体。补充完整制取
晶体。补充完整制取 晶体的实验方案:向含有少量
晶体的实验方案:向含有少量 、
、 的
的 溶液中,
溶液中, 。(已知:
。(已知: 、
、 在
在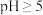 时完全转化为氢氧化物沉淀:
时完全转化为氢氧化物沉淀: 的溶解度曲线如图所示;实验中须使用的试剂有:
的溶解度曲线如图所示;实验中须使用的试剂有: 粉末、无水乙醇)
粉末、无水乙醇)
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室模拟合成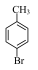 和CH3CH2CH2Br的方法如图1。
和CH3CH2CH2Br的方法如图1。
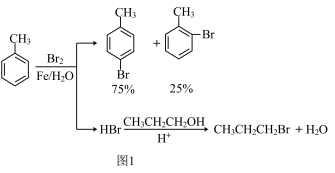
已知:甲苯和液溴在有少量水存在时也能反应(如图2):
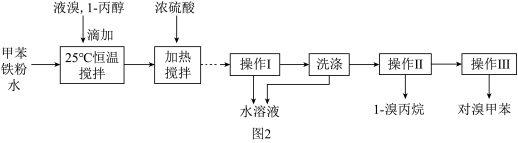
实验室模拟合成对溴甲苯和1-溴丙烷的流程和相关数据如表:
(1)实验室存放液溴的试剂瓶需密闭,同时瓶中要加入____ ,以减少溴的挥发.写出甲苯和液溴反应生成对溴甲苯的化学方程式___ 。
(2)反应装置如图3所示:
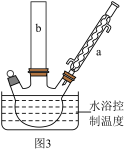
①图中玻璃仪器a的名称是____ ,方块b中为某玻璃仪器,其名称是___ 。
②三颈烧瓶中开始加入了甲苯、铁粉和水。加入的适量水的作用是:易于控制温度和____ ,加热搅拌操作中加入浓硫酸,完成1-丙醇的取代反应,浓硫酸的作用是____ 。
(3)操作I的名称是___ ,操作Ⅲ的名称是___ 。
 和CH3CH2CH2Br的方法如图1。
和CH3CH2CH2Br的方法如图1。
已知:甲苯和液溴在有少量水存在时也能反应(如图2):

实验室模拟合成对溴甲苯和1-溴丙烷的流程和相关数据如表:
| 物质 | 甲苯 | 1-丙醇 | 1-溴丙烷 | 对溴甲苯 | 邻溴甲苯 |
| 沸点(℃) | 110.8 | 97.2 | 71 | 184.3 | 181.7 |
(2)反应装置如图3所示:

①图中玻璃仪器a的名称是
②三颈烧瓶中开始加入了甲苯、铁粉和水。加入的适量水的作用是:易于控制温度和
(3)操作I的名称是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某小组同学利用下图装置(夹持仪器已省略)制备溴苯,并探究该反应原理。
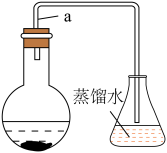
I.制备溴苯
(1)装置中长导管a的作用是_________ 、导出气体。
(2)本实验所获得的溴苯为褐色,是因为_____________ 。
II.分离提纯
已知,溴苯与苯互溶,液溴、苯、溴苯的沸点依次为59℃、80℃、156℃。同学们设计了如下流程:
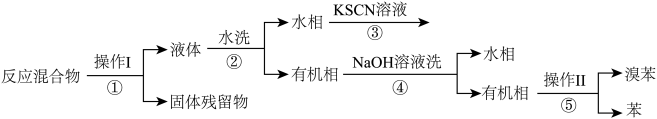
(3)操作Ⅱ为_______ 。
(4)流程②和④中,需要用到的玻璃仪器是烧杯、_________ ;流程③的现象为_______ ,流程④的作用是____________ 。
III.探究原理
(5)反应结束后,某同学取少量锥形瓶中的液体于试管中,再滴入几滴AgNO3溶液,出现浅黄色浑浊,从而判断反应一定生成了HBr。你认为该同学的判断_____ (填“合理”、“不合理”)。
(6)为探究锥形瓶中溶液的离子,请完成下表探究实验方案(限选试剂:镁粉、四氯化碳、氯水、溴水、蒸馏水)
根据上述结论推断,制备溴苯的反应属于_____ 反应,其反应方程式为___________ 。

I.制备溴苯
(1)装置中长导管a的作用是
(2)本实验所获得的溴苯为褐色,是因为
II.分离提纯
已知,溴苯与苯互溶,液溴、苯、溴苯的沸点依次为59℃、80℃、156℃。同学们设计了如下流程:

(3)操作Ⅱ为
(4)流程②和④中,需要用到的玻璃仪器是烧杯、
III.探究原理
(5)反应结束后,某同学取少量锥形瓶中的液体于试管中,再滴入几滴AgNO3溶液,出现浅黄色浑浊,从而判断反应一定生成了HBr。你认为该同学的判断
(6)为探究锥形瓶中溶液的离子,请完成下表探究实验方案(限选试剂:镁粉、四氯化碳、氯水、溴水、蒸馏水)
| 实验步骤 | 预期现象 | 结论 |
| 1.将锥形瓶中的液体转入分液漏斗,加足量 | ||
| 2.向试管A中加入少量 | 溶液分层,下层显 | 锥形瓶中液体含大量Br- |
| 3.向试管B中加入 | 有汽泡生成 | 锥形瓶中液体含大量 |
您最近半年使用:0次



