(1)计算下列物质的摩尔质量:NaOH_____________ 硫酸____________
(2)1.5mol Na2SO4·10H2O中所含的Na+的物质的量是__________ mol ,所含的SO42-的物质的量是________ mol,所含H2O分子的数目是________________
(3)标况下22.4L N2 的质量为_______ g
(2)1.5mol Na2SO4·10H2O中所含的Na+的物质的量是
(3)标况下22.4L N2 的质量为
更新时间:2017-10-30 09:32:21
|
【知识点】 物质的量有关计算
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】物质的量是高中化学常用的物理量,请完成以下有关计算(设NA为阿伏加德罗常数的值):
(1)2.3g乙醇含有___ 个H原子,所含共价键的物质的量为___ ,其中官能团羟基所含的电子数为___ 。
(2)9.5g某二价金属的氯化物中含有0.2molCl-,则此氯化物的摩尔质量为___ 。
(3)6.72LCO(标准状况)与一定量的Fe2O3恰好完全反应(生成Fe与CO2)后,生成Fe的质量为___ g,转移的电子数目为___ 。
(1)2.3g乙醇含有
(2)9.5g某二价金属的氯化物中含有0.2molCl-,则此氯化物的摩尔质量为
(3)6.72LCO(标准状况)与一定量的Fe2O3恰好完全反应(生成Fe与CO2)后,生成Fe的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】根据所学知识,回答下列问题:
(1)分类在化学学习中起着非常重要的作用,下列分类标准合理的是___________(填标号)。
(2)现有以下六种物质:①NaCl溶液,② ,③HCl,④蔗糖,⑤NaOH固体,⑥稀硫酸。其中,属于电解质的是
,③HCl,④蔗糖,⑤NaOH固体,⑥稀硫酸。其中,属于电解质的是___________ ,(填序号,下同),属于非电解质的是___________ 。
(3)化学计量是化学定量研究的基础。
①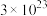 个
个 分子的物质的量为
分子的物质的量为___________ mol,质量为___________ g。
②将30mL 0.5 NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为
NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为___________  。
。
③等质量的 和
和 ,其分子个数比
,其分子个数比
___________ ,标准状况下气体的体积比
___________ 。
(1)分类在化学学习中起着非常重要的作用,下列分类标准合理的是___________(填标号)。
| A.根据物质溶于水后形成的溶液呈碱性,可将此类物质归类为碱 |
| B.根据物质能否导电,将物质分为电解质和非电解质 |
| C.根据反应中是否有电子的转移,将化学反应分为氧化还原反应和非氧化还原反应 |
| D.根据分散系中分散质粒子的直径大小,将分散系分为溶液、胶体和浊液 |
 ,③HCl,④蔗糖,⑤NaOH固体,⑥稀硫酸。其中,属于电解质的是
,③HCl,④蔗糖,⑤NaOH固体,⑥稀硫酸。其中,属于电解质的是(3)化学计量是化学定量研究的基础。
①
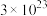 个
个 分子的物质的量为
分子的物质的量为②将30mL 0.5
 NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为
NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为 。
。③等质量的
 和
和 ,其分子个数比
,其分子个数比

您最近一年使用:0次
【推荐3】化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可以减少该有害物质向环境排放。例如

(1) 中
中 元素的化合价是
元素的化合价是___________ 。
(2)完成反应④的配平,并用单线桥 标出电子转移的方向和数目(化学计量系数若为1也请写出) ____ 。
反应④为:___ ___
___ ___
___ ____
____ ____
____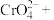 ____
____
(3)反应①中另一种反应物为盐酸溶液,用该反应制取氯气。写出发生反应的化学方程式:___________ ,盐酸的作用为___________ 。
(4)现需要制取标准状况下5.6L ,至少需要
,至少需要___________ g 。
。

(1)
 中
中 元素的化合价是
元素的化合价是(2)完成反应④的配平,并用
反应④为:___
 ___
___ ___
___ ____
____ ____
____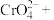 ____
____
(3)反应①中另一种反应物为盐酸溶液,用该反应制取氯气。写出发生反应的化学方程式:
(4)现需要制取标准状况下5.6L
 ,至少需要
,至少需要 。
。
您最近一年使用:0次



