一种海水电池的反应原理可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,有关反应的说法正确的是
| A.反应中MnO2是还原剂 |
| B.电池工作时,海水起导电作用,其中NaCl浓度保持不变 |
| C.Ag为负极,电极反应为Ag-e-+Cl-=AgCl |
| D.每生成1 mol Na2Mn5Ol0转移1mol电子 |
更新时间:2017-05-26 15:47:15
|
【知识点】 原电池原理的应用
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】已知活泼性Mg>Al,且Mg不与NaOH溶液反应,Fe遇浓HNO3会钝化。分析下图所示的四个原电池装置,其中结论正确的是
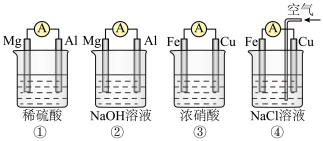

| A.①②中Mg作负极,③④中Fe作负极 |
| B.②中Mg作正极 |
| C.③中Fe作负极 |
| D.④中Cu作正极,电极反应式为2H++2e−=H2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验中,对应的现象以及解释或结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 解释或结论 |
| A | 向足量的浓硝酸中加入铁片,一段时间后加入铜粉 | 有气体生成,溶液呈蓝绿色 | 浓硝酸将Fe氧化为 ,生成 ,生成 ,Cu与 ,Cu与 反应生成 反应生成 、 、 |
| B | 分别向 、 、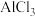 溶液中加入足量氨水 溶液中加入足量氨水 | 均有白色沉淀产生 | 金属性: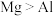 |
| C | 表面变黑的银器浸泡到盛有食盐水的铝制容器中,银器与铝接触 | 银器变得光亮如新 | 构成原电池,铝做负极,硫化银得电子被还原成单质银 |
| D | 向 稀溶液中滴入NaOH溶液至不再有沉淀生成,再滴加 稀溶液中滴入NaOH溶液至不再有沉淀生成,再滴加 稀溶液 稀溶液 | 白色沉淀逐渐变为浅蓝色 | 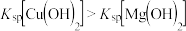 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次




