A是常见的有机物质,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平。有关物质的转化关系如图甲所示,请回答下列问题:



(1)B的结构式为____________ 。D物质的名称是_________ 。
(2)在①~④反应中,属于加成反应的是______________ (填反应序号);
(3)写出反应④的化学方程式:________________________ 。
(4)实验室用图乙所示装置进行反应③
a.反应③的化学方程式是___________ .反应类型为______ 。
b.乙中的导管不能伸入到液面下的原因是__________________ 。
c.实验完成后,从试管乙中分离出有机物C的方法是_____________ 。



(1)B的结构式为
(2)在①~④反应中,属于加成反应的是
(3)写出反应④的化学方程式:
(4)实验室用图乙所示装置进行反应③
a.反应③的化学方程式是
b.乙中的导管不能伸入到液面下的原因是
c.实验完成后,从试管乙中分离出有机物C的方法是
更新时间:2017-12-09 14:35:21
|
相似题推荐
解答题-有机推断题
|
较易
(0.85)
名校
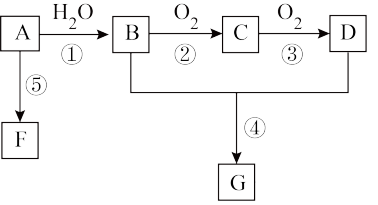
【推荐1】已知有机物A的产量是衡量一个国家石油化工发展水平的标志。B和D是生活中两种常见的有机物,F是高分子化合物。相互转化关系如图所示:
已知:RCHO RCOOH
RCOOH
(1)A分子的结构简式为___ ;D中官能团名称为___ 。
(2)在反应①~⑥中,属于加成反应的是__ 。(填序号)
(3)B和D反应生成G进行比较缓慢,提高该反应速率的方法主要有__ (写一种即可);分离提纯混合物中的G的实验操作名称为__ 。
(4)写出下列反应的化学方程式:
反应④:B+D→G:__ 。
反应⑥:A→F:___ 。
(5)下列说法正确的是___ 。
A.有机物B分子中的所有原子在同一平面上
B.有机物A能使酸性KMnO4溶液和溴水褪色,其原理相同
C.有机物B及其同系物均能与金属钠反应放出氢气
D.可用Na2CO3溶液鉴别有机物B和D
E.CH3COOH和HCOOCH3是同一种物质

已知:RCHO
 RCOOH
RCOOH(1)A分子的结构简式为
(2)在反应①~⑥中,属于加成反应的是
(3)B和D反应生成G进行比较缓慢,提高该反应速率的方法主要有
(4)写出下列反应的化学方程式:
反应④:B+D→G:
反应⑥:A→F:
(5)下列说法正确的是
A.有机物B分子中的所有原子在同一平面上
B.有机物A能使酸性KMnO4溶液和溴水褪色,其原理相同
C.有机物B及其同系物均能与金属钠反应放出氢气
D.可用Na2CO3溶液鉴别有机物B和D
E.CH3COOH和HCOOCH3是同一种物质
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某小组设计实验证明乙醇和钠反应产生氢气,并探究氧化铜的还原产物。
已知:① 。
。
②红色粉末 在酸性条件下发生歧化反应:
在酸性条件下发生歧化反应: 。
。
装置如图所示:
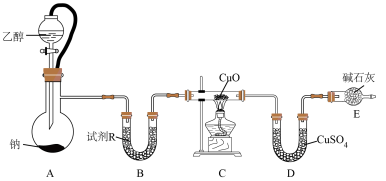
回答下列问题:
(1)试剂R最好选择__________(填字母)。
(2)装置E的作用是__________ 。
(3)实验完毕后,为了探究C中红色粉末是否含有 ,设计下列两种方案:
,设计下列两种方案:
方案1:取少量红色粉末于试管,加入足量溶液M,充分振荡,若溶液变蓝色,则红色粉末一定含 ;
;
方案2:取ag红色粉末,在加热条件下通入足量氢气,充分反应后,冷却、称重,红色固体质量为xg。
①方案1中M可能是__________ 。
A.稀硝酸 B.稀硫酸 C.浓硫酸 D.浓硝酸
②方案2中,当
__________ 时,红色粉末全部是 。
。
(4)分析与讨论。
①CuO被 、
、 、CO等还原可能生成
、CO等还原可能生成 或Cu,生成
或Cu,生成 的可能原因是
的可能原因是__________ 。
A.通入 量不足 B.
量不足 B. 与CuO接触充分
与CuO接触充分
C.温度较低 D.温度过高
②若缺少装置B,C中黑色粉末变红色,D中白色粉末变蓝色,不能肯定A中一定生成了 ,用化学方程式表达其理由
,用化学方程式表达其理由__________ 。
已知:①
 。
。②红色粉末
 在酸性条件下发生歧化反应:
在酸性条件下发生歧化反应: 。
。装置如图所示:

回答下列问题:
(1)试剂R最好选择__________(填字母)。
| A.碱石灰 | B.无水氯化钙 | C.五氧化二磷 | D.硫酸镁 |
(3)实验完毕后,为了探究C中红色粉末是否含有
 ,设计下列两种方案:
,设计下列两种方案:方案1:取少量红色粉末于试管,加入足量溶液M,充分振荡,若溶液变蓝色,则红色粉末一定含
 ;
;方案2:取ag红色粉末,在加热条件下通入足量氢气,充分反应后,冷却、称重,红色固体质量为xg。
①方案1中M可能是
A.稀硝酸 B.稀硫酸 C.浓硫酸 D.浓硝酸
②方案2中,当

 。
。(4)分析与讨论。
①CuO被
 、
、 、CO等还原可能生成
、CO等还原可能生成 或Cu,生成
或Cu,生成 的可能原因是
的可能原因是A.通入
 量不足 B.
量不足 B. 与CuO接触充分
与CuO接触充分C.温度较低 D.温度过高
②若缺少装置B,C中黑色粉末变红色,D中白色粉末变蓝色,不能肯定A中一定生成了
 ,用化学方程式表达其理由
,用化学方程式表达其理由
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题:
I.乳酸(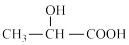 )、酒精、醋酸、淀粉等都是生活中常见的物质。
)、酒精、醋酸、淀粉等都是生活中常见的物质。
(1)在生活中,常选择上述物质中_______________ (填结构简式)清洗水壶里的水垢。
(2)生活中常选择_______________ 酒精 选择“75%”“95%”或“无水”
选择“75%”“95%”或“无水” 皮肤消毒。
皮肤消毒。
(3)上述物质中,属于天然高分子化合物的是_________________  填名称
填名称 。
。
(4)乳酸中发生如下变化: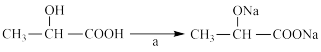 ,则所用的试剂a为
,则所用的试剂a为________ (写化学式)。
II.X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
(5)X在元素周期表中的位置为___________ ;Y元素的名称为________________ 。
(6)元素W的离子结构示意图是_______________ ;Z、Y形成的化合物为____________ (用化学式表示)。
I.乳酸(
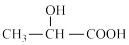 )、酒精、醋酸、淀粉等都是生活中常见的物质。
)、酒精、醋酸、淀粉等都是生活中常见的物质。(1)在生活中,常选择上述物质中
(2)生活中常选择
 选择“75%”“95%”或“无水”
选择“75%”“95%”或“无水” 皮肤消毒。
皮肤消毒。(3)上述物质中,属于天然高分子化合物的是
 填名称
填名称 。
。(4)乳酸中发生如下变化:
 ,则所用的试剂a为
,则所用的试剂a为II.X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的最外层电子数是次外层的2倍 |
| Y | M层上的电子数是K层的3倍 |
| Z | Z的一种核素的质量数为53,中子数为34 |
| W | W2+与氖原子具有相同核外电子排布 |
(5)X在元素周期表中的位置为
(6)元素W的离子结构示意图是
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐1】已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2RCHO+O2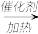 2RCOOH。现以A为主要原料合成乙酸乙酯,其合成路线如图1所示。
2RCOOH。现以A为主要原料合成乙酸乙酯,其合成路线如图1所示。

(1)B、D分子内含有的官能团分别是____ 、______ (填名称)。
(2)写出下列反应的反应类型:①______ ,④________ 。
(3)B→C的反应方程式为____________
(4)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制取的主要步骤如下:
①在甲试管(如图2)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液。
②按如图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热3~5min。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出有机层、洗涤、干燥。
a.若实验中用乙酸和含18O的乙醇作用,该反应的化学方程式是:______ ,此装置中采用了球形干燥管,其作用是_________ 。
b.欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器是_____ ;分离时,乙酸乙酯应该从仪器____ (填:“下口放” 或“上口倒”)出。
c.生成乙酸乙酯的反应是可逆反应,反应一段时间后,下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)______ 。
①混合物中各物质的浓度不再变化;
②单位时间里,生成1mol乙醇,同时生成1mol乙酸;
③单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
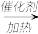 2RCOOH。现以A为主要原料合成乙酸乙酯,其合成路线如图1所示。
2RCOOH。现以A为主要原料合成乙酸乙酯,其合成路线如图1所示。
(1)B、D分子内含有的官能团分别是
(2)写出下列反应的反应类型:①
(3)B→C的反应方程式为
(4)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制取的主要步骤如下:
①在甲试管(如图2)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液。
②按如图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热3~5min。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出有机层、洗涤、干燥。
a.若实验中用乙酸和含18O的乙醇作用,该反应的化学方程式是:
b.欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器是
c.生成乙酸乙酯的反应是可逆反应,反应一段时间后,下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)
①混合物中各物质的浓度不再变化;
②单位时间里,生成1mol乙醇,同时生成1mol乙酸;
③单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】烃A是一种基础化工原料,标准状况下2.24L的A气体完全燃烧生成8.8gCO2和3.6gH2O。F是一种具有水果香味的油状液体。有关物质的转化关系如下图:
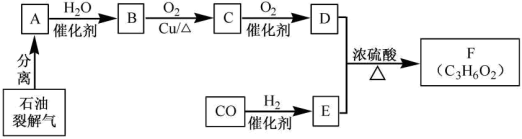
请回答:
(1)D+E→F的反应类型是__________________ 。
(2)B→C的化学方程式是___________________ 。
(3)下列说法不正确 的是__________________________ 。
A.物质C与银氨溶液在一定条件下能发生银镜反应
B.向装有2mLB的小试管中投入一小粒钠,钠浮于液面上,并产生大量气泡
C.可以用含D的溶液除去热水瓶中的水垢(主要成分是碳酸钙、氢氧化镁)
D.可以用饱和碳酸钠溶液鉴别B、D和F三种物质

请回答:
(1)D+E→F的反应类型是
(2)B→C的化学方程式是
(3)下列说法
A.物质C与银氨溶液在一定条件下能发生银镜反应
B.向装有2mLB的小试管中投入一小粒钠,钠浮于液面上,并产生大量气泡
C.可以用含D的溶液除去热水瓶中的水垢(主要成分是碳酸钙、氢氧化镁)
D.可以用饱和碳酸钠溶液鉴别B、D和F三种物质
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐3】A的产量是衡量一个国家石油化工发展水平的标志,B和D是生活中两种常见的有机物,都可以通过粮食进行发酵酿造,H是高分子化合物。相关转化关系如图所示。
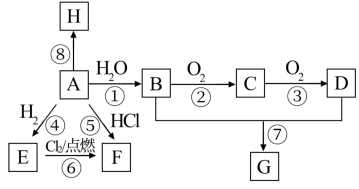
(1)A分子的电子式为___________ ;D中官能团的名称为___________ 。
(2)在反应①~⑧中,属于取代反应的是___________ (填序号)。
(3)写出下列反应的化学方程式:
反应②___________ 。
反应⑦___________ 。
(4)Ⅰ是A的一种同系物,但比A多一个碳原子,写出Ⅰ与氯化氢的反应产物的结构简式___________ 。
(5)F是一种速效局部冷冻麻醉剂,可由反应⑤或⑥制备,请指出哪一个反应制备较好?___________ (填序号),并说明理由___________ 。
(6)若148gB和120gD充分反应生成了88gG,该反应的产率为___________ 。

(1)A分子的电子式为
(2)在反应①~⑧中,属于取代反应的是
(3)写出下列反应的化学方程式:
反应②
反应⑦
(4)Ⅰ是A的一种同系物,但比A多一个碳原子,写出Ⅰ与氯化氢的反应产物的结构简式
(5)F是一种速效局部冷冻麻醉剂,可由反应⑤或⑥制备,请指出哪一个反应制备较好?
(6)若148gB和120gD充分反应生成了88gG,该反应的产率为
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐1】已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
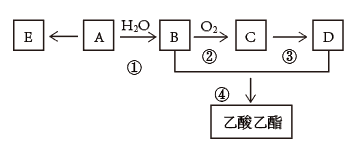
(1)A分子中官能团的名称是_______ ,D中官能团的名称是_______ ;反应①的反应类型是_______ 反应。
(2)反应②的化学方程式是_______ ,反应型:_______ ;反应④的化学方程式是_______ ,反应类型:_______ 。
(3)E是常见的高分子材料,合成E的化学方程式是_______ 。
(4)某同学用如图所示的实验装置制取少量乙酸乙酯,实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
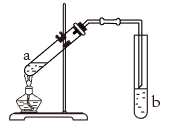
①装置中使用球形干燥管除起到冷凝作用外,另一重要作用是_______ ,b中分离乙酸乙酯必须使用的一种玻璃仪器是_______ 。
②b试管中饱和 溶液的作用是
溶液的作用是_______ (填字母)。
A.降低乙酸乙酯的溶解度
B.除去实验中挥发出来的硫酸
C.除去乙酸乙酯中混有的乙酸和乙醇

(1)A分子中官能团的名称是
(2)反应②的化学方程式是
(3)E是常见的高分子材料,合成E的化学方程式是
(4)某同学用如图所示的实验装置制取少量乙酸乙酯,实验结束后,试管甲中上层为透明的、不溶于水的油状液体。

①装置中使用球形干燥管除起到冷凝作用外,另一重要作用是
②b试管中饱和
 溶液的作用是
溶液的作用是A.降低乙酸乙酯的溶解度
B.除去实验中挥发出来的硫酸
C.除去乙酸乙酯中混有的乙酸和乙醇
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】用下图所示装置制备乙酸乙酯粗产品(加热和夹持装置等省略),有关数据如下表所示:
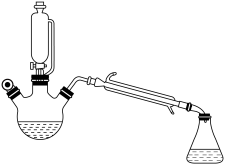
已知:乙醇可以和氯化钙反应生成微溶于水的CaC12·6C2H5OH。在三颈烧瓶内将过量的乙醇和少量的浓硫酸混合,然后经恒压分液斗边滴加酸,边加热蒸馏。得到含有乙醇、醋酸和水的乙酸乙酯粗产品。
(1)混合乙醇与浓硫酸时,应先加入的试剂是_______ ;浓硫酸的作用是__________ 。
(2)边滴加醋酸,边加热蒸馏的目的是_______ 。将粗产品再经下列步骤精制:
(3)为除去其中的醋酸,可向粗产品中加入______ (填序号)。
A.无水乙醇 B.碳酸钠粉末 C.无水醋酸钠
(4)向其中加入饱和氯化钙溶液。振荡、分离。其目的是______ 。
(5)然后再向其中加入无水硫酸钠,振荡,静置,以除去水分。最后,将经过上述处理后的液体放入一干燥的蒸馏烧瓶内。再蒸馏,弃去低沸点馏分,收集沸程76℃~____ ℃(填“78”或“118“)之间的馏分即得纯净的乙酸乙酯。
(6)在实验中原料用量:23.0mL乙醇、15.0mL冰醋酸,最终得到16.0mL乙酸乙酯,则本次实验中乙酸乙酯的产率为________ (百分数精确到0.1)。

物质 | C2H5OH | CH3COOH | CH3COOC2H5 |
| 密度g/cm3 | 0.79 | 1.05 | 0.90 |
| 沸点/℃ | 78.3 | 118 | 77.1 |
已知:乙醇可以和氯化钙反应生成微溶于水的CaC12·6C2H5OH。在三颈烧瓶内将过量的乙醇和少量的浓硫酸混合,然后经恒压分液斗边滴加酸,边加热蒸馏。得到含有乙醇、醋酸和水的乙酸乙酯粗产品。
(1)混合乙醇与浓硫酸时,应先加入的试剂是
(2)边滴加醋酸,边加热蒸馏的目的是
(3)为除去其中的醋酸,可向粗产品中加入
A.无水乙醇 B.碳酸钠粉末 C.无水醋酸钠
(4)向其中加入饱和氯化钙溶液。振荡、分离。其目的是
(5)然后再向其中加入无水硫酸钠,振荡,静置,以除去水分。最后,将经过上述处理后的液体放入一干燥的蒸馏烧瓶内。再蒸馏,弃去低沸点馏分,收集沸程76℃~
(6)在实验中原料用量:23.0mL乙醇、15.0mL冰醋酸,最终得到16.0mL乙酸乙酯,则本次实验中乙酸乙酯的产率为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某校化学探究小组学生进行如下实验,以验证乙酸的酸性比碳酸强,并利用乙醇和乙酸制备乙酸乙酯。
实验I:验证乙酸的酸性比碳酸强
某同学设计如下图所示的实验装置,验证乙酸的酸性强于碳酸。
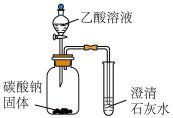
(1)题中涉及反应的离子方程式为_____________ 。
(2)根据实验现象__________ ,确定乙酸的酸性强于碳酸。
(3)另一同学对实验装置提出质疑,其理由是____________ ,应如何改进:__________ 。
实验Ⅱ:制备乙酸乙酯
该小组同学按图所示装置进行实验,以制取乙酸乙酯。
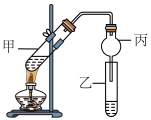
(4)试管甲中依次放入以下液体:①2mL乙醇;②3mL___________ ;③2mL乙酸。为防止试管甲中的液体在实验时暴沸,在加热前还应加入___________ 。
(5)试管乙中盛放的试剂是___________ ,其作用为______________________ 。
(6)装置丙的作用是_________________________________________________ 。
(7)若经分离得到纯乙酸乙酯8.8g,则理论上参加反应的乙醇的质量是___________ g。
实验I:验证乙酸的酸性比碳酸强
某同学设计如下图所示的实验装置,验证乙酸的酸性强于碳酸。

(1)题中涉及反应的离子方程式为
(2)根据实验现象
(3)另一同学对实验装置提出质疑,其理由是
实验Ⅱ:制备乙酸乙酯
该小组同学按图所示装置进行实验,以制取乙酸乙酯。

(4)试管甲中依次放入以下液体:①2mL乙醇;②3mL
(5)试管乙中盛放的试剂是
(6)装置丙的作用是
(7)若经分离得到纯乙酸乙酯8.8g,则理论上参加反应的乙醇的质量是
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐1】I.回答下列问题:
(1)A、B、C三种烃分子中均含有8个氢原子,其中A、B常温下呈气态,C呈液态。请回答:
①A是符合上述条件中相对分子质量最小的,则A的分子式为____ ;B属于链状单烯烃,且与HBr加成的产物只有一种,试写出B的结构简式____ 。
②C属于芳香烃,可用来制烈性炸药,试写出C制取烈性炸药的化学方程式____ 。
II.某芳香烃A的质谱图如图所示:
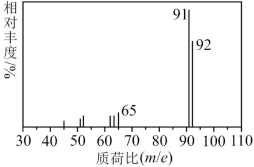
(2)A的名称为____ ,1molA完全燃烧消耗氧气的物质的量为____ 。
(3)A的二氯代物共有____ 种。
(4)A中最多有____ 个原子共平面。
(5)A分子的核磁共振氢谱峰面积之比为____ 。
(1)A、B、C三种烃分子中均含有8个氢原子,其中A、B常温下呈气态,C呈液态。请回答:
①A是符合上述条件中相对分子质量最小的,则A的分子式为
②C属于芳香烃,可用来制烈性炸药,试写出C制取烈性炸药的化学方程式
II.某芳香烃A的质谱图如图所示:

(2)A的名称为
(3)A的二氯代物共有
(4)A中最多有
(5)A分子的核磁共振氢谱峰面积之比为
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】有机物甲的分子式为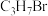 ,在适宜的条件下能发生如下转化关系:
,在适宜的条件下能发生如下转化关系:
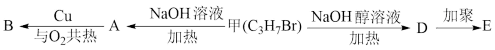
已知: 能与新制氢氧化铜悬浊液反应,试回答下列问题:
能与新制氢氧化铜悬浊液反应,试回答下列问题:
(1)甲的结构简式_______ 。
(2)甲与 溶液共热的化学方程式
溶液共热的化学方程式_______ 。
(3)甲与 醇溶液共热的化学方程式为
醇溶液共热的化学方程式为_______ 。
(4)A与氧气反应生成 的化学方程式
的化学方程式_______ 。
(5) 生成
生成 的化学方程式
的化学方程式_______ 。
(6)为检验甲中溴元素进行如下操作:①加热煮沸;②加入 溶液;③取少量该卤代烃;④加入足量稀硝酸酸化;⑤加入
溶液;③取少量该卤代烃;④加入足量稀硝酸酸化;⑤加入 溶液;⑥冷却。正确的操作顺序是
溶液;⑥冷却。正确的操作顺序是_______ 。
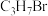 ,在适宜的条件下能发生如下转化关系:
,在适宜的条件下能发生如下转化关系: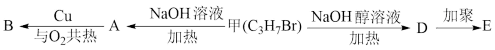
已知:
 能与新制氢氧化铜悬浊液反应,试回答下列问题:
能与新制氢氧化铜悬浊液反应,试回答下列问题:(1)甲的结构简式
(2)甲与
 溶液共热的化学方程式
溶液共热的化学方程式(3)甲与
 醇溶液共热的化学方程式为
醇溶液共热的化学方程式为(4)A与氧气反应生成
 的化学方程式
的化学方程式(5)
 生成
生成 的化学方程式
的化学方程式(6)为检验甲中溴元素进行如下操作:①加热煮沸;②加入
 溶液;③取少量该卤代烃;④加入足量稀硝酸酸化;⑤加入
溶液;③取少量该卤代烃;④加入足量稀硝酸酸化;⑤加入 溶液;⑥冷却。正确的操作顺序是
溶液;⑥冷却。正确的操作顺序是
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐3】已知:A(分子式为:C2H4)是来自石油的重要有机化工原料,B、D是厨房中的两种有机物,E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。
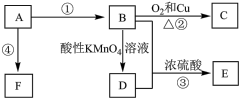
(1)A的电子式为________ ,官能团为:________ ;C的名称________ ,E的分子式为:________ 。
(2)B分子中的官能团名称是________ ,D分子中的官能团名称是________ .
(3)写出下列反应的化学方程式并指出反应类型:
①________ ,反应类型________ 。
②________ ,反应类型________ 。
④________ ,反应类型________ 。
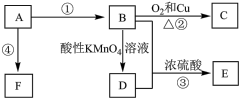
(1)A的电子式为
(2)B分子中的官能团名称是
(3)写出下列反应的化学方程式并指出反应类型:
①
②
④
您最近一年使用:0次



