已知:Fe3+溶液颜色为黄色,Fe2+溶液颜色为浅绿色,Fe(OH)3为红褐色。现将少量Fe2O3粉末加入适量稀盐酸,发生反应的离子方程式为____________________________________ ,用所得溶液进行以下实验:
(1)取少量溶液于试管中,滴入NaOH溶液,观察到有红褐色沉淀生成,反应的离子方程式为_________________________________________ 。
(2)取少量溶液于试管中,加入少量还原铁粉,振荡,铁粉逐渐溶解,溶液由黄色变为浅绿色,反应的离子方程式为_____________________________ 。
(3)在烧杯中加入25mL蒸馏水,加热至沸腾,向沸水中滴加几滴FeCl3饱和溶液,继续煮沸直到溶液呈__________ 色,即得到Fe(OH)3胶体。将该胶体置于暗处,用一束激光照射,在垂直于光线的方向观察,可以看到一条光的通路,此现象叫做_________________ ,是鉴别胶体和__________ 的方法。
(4)取少量Fe(OH)3胶体,逐滴加入盐酸至过量,可观察到的现象是:先_______ ,然后______ ,对前一现象的解释是_____________ ,对后一现象的解释是(用离子方程式表示)_________ 。
(1)取少量溶液于试管中,滴入NaOH溶液,观察到有红褐色沉淀生成,反应的离子方程式为
(2)取少量溶液于试管中,加入少量还原铁粉,振荡,铁粉逐渐溶解,溶液由黄色变为浅绿色,反应的离子方程式为
(3)在烧杯中加入25mL蒸馏水,加热至沸腾,向沸水中滴加几滴FeCl3饱和溶液,继续煮沸直到溶液呈
(4)取少量Fe(OH)3胶体,逐滴加入盐酸至过量,可观察到的现象是:先
更新时间:2017-12-14 19:57:46
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】实验室有如下物质:① 胶体②医用酒精③
胶体②医用酒精③ ④
④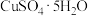 ⑤饱和氯化铁溶液⑥
⑤饱和氯化铁溶液⑥ ⑦
⑦ ⑧稀盐酸⑨
⑧稀盐酸⑨ ⑩
⑩ 。溶液回答下列问题:
。溶液回答下列问题:
(1)某同学将③④⑨归为一类,他的分类依据是_______ 。
A.都属于酸式盐B.都属于盐C.都易溶于水
(2)以上物质属于非电解质的有_______ (填编号,下同),能导电的有_______ 。
(3)写出⑦和⑨在水中的电离方程式_______ 、_______ 。
(4)区分物质①和⑤可用哪些方法_______ 。
A.观察颜色B.丁达尔效应C.观察颗粒大小
(5)向①中慢慢滴加⑧至过量,可观察到的现象是_______ ,写出反应的离子方程式_______ 。
(6)向 固体中滴加过量稀盐酸,写出反应的离子方程式
固体中滴加过量稀盐酸,写出反应的离子方程式_______ 。
(7)向 溶液中滴加
溶液中滴加 溶液至中性,写出反应的离子方程式
溶液至中性,写出反应的离子方程式_______ 。
 胶体②医用酒精③
胶体②医用酒精③ ④
④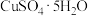 ⑤饱和氯化铁溶液⑥
⑤饱和氯化铁溶液⑥ ⑦
⑦ ⑧稀盐酸⑨
⑧稀盐酸⑨ ⑩
⑩ 。溶液回答下列问题:
。溶液回答下列问题:(1)某同学将③④⑨归为一类,他的分类依据是
A.都属于酸式盐B.都属于盐C.都易溶于水
(2)以上物质属于非电解质的有
(3)写出⑦和⑨在水中的电离方程式
(4)区分物质①和⑤可用哪些方法
A.观察颜色B.丁达尔效应C.观察颗粒大小
(5)向①中慢慢滴加⑧至过量,可观察到的现象是
(6)向
 固体中滴加过量稀盐酸,写出反应的离子方程式
固体中滴加过量稀盐酸,写出反应的离子方程式(7)向
 溶液中滴加
溶液中滴加 溶液至中性,写出反应的离子方程式
溶液至中性,写出反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有以下物质:①Cu ②澄清石灰水 ③液氨 ④ 晶体 ⑤液态HCl ⑥
晶体 ⑤液态HCl ⑥ 胶体 ⑦医用酒精 ⑧
胶体 ⑦医用酒精 ⑧ ⑨碳酸钡 ⑩
⑨碳酸钡 ⑩ 。回答下列问题(用相应物质的序号填写):
。回答下列问题(用相应物质的序号填写):
(1)属于电解质的有_______ ,属于非电解质的有_______ 。
(2)写出向⑨中加入⑤的水溶液发生反应的离子方程式_______ 。
(3)写出向②中滴加少量④的水溶液的离子方程式_______ 。
(4)向⑥中逐滴加入⑤的水溶液的现象是_______ ,产生这种现象的原因是_______ 。(请以文字结合离子方程式回答)
 晶体 ⑤液态HCl ⑥
晶体 ⑤液态HCl ⑥ 胶体 ⑦医用酒精 ⑧
胶体 ⑦医用酒精 ⑧ ⑨碳酸钡 ⑩
⑨碳酸钡 ⑩ 。回答下列问题(用相应物质的序号填写):
。回答下列问题(用相应物质的序号填写):(1)属于电解质的有
(2)写出向⑨中加入⑤的水溶液发生反应的离子方程式
(3)写出向②中滴加少量④的水溶液的离子方程式
(4)向⑥中逐滴加入⑤的水溶液的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列10种物质:①钠②纯醋酸③氨气④浓盐酸⑤NaOH溶液⑥ 固体⑦熔融的NaCl⑧
固体⑦熔融的NaCl⑧ 固体⑨高锰酸钾粉末⑩氢氧化铁胶体。回答下列问题:
固体⑨高锰酸钾粉末⑩氢氧化铁胶体。回答下列问题:
(1)上述物质中能导电的有___________ (填序号,下同);属于电解质的有___________ 。
(2)⑧属于___________ (填“酸”、“碱”或“盐”),⑧与⑤在溶液中反应的离子方程式为___________ 。
(3)④和⑨混合发生反应 (未配平),其中氧化剂与还原剂的个数比为
(未配平),其中氧化剂与还原剂的个数比为___________ 。
(4)写出制备⑩的离子方程式___________ 。
 固体⑦熔融的NaCl⑧
固体⑦熔融的NaCl⑧ 固体⑨高锰酸钾粉末⑩氢氧化铁胶体。回答下列问题:
固体⑨高锰酸钾粉末⑩氢氧化铁胶体。回答下列问题:(1)上述物质中能导电的有
(2)⑧属于
(3)④和⑨混合发生反应
 (未配平),其中氧化剂与还原剂的个数比为
(未配平),其中氧化剂与还原剂的个数比为(4)写出制备⑩的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.NaNO2和食盐外观很像,曾出现误把NaNO2当食盐而造成人员中毒的事情,在酸性溶液中它也是一种氧化剂,如NaNO2能把Fe2+氧化成Fe3+。已知NaNO2水溶液呈碱性,AgNO2是一种难溶于水白色固体。NaCl溶液呈中性。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐,如NaNO2,则导致血红蛋白中的Fe2+转化为Fe3+而中毒(FeCl2溶液为浅绿色,FeCl3溶液为棕黄色),可以服用维生素C解毒,维生素C在解毒的过程中表现出__________ (填“氧化”或“还原”)性。
(2)下列方法中,不能用来区分NaNO2和NaCl的是__________ 。
A.测溶液的酸碱性
B.加入AgNO3溶液观察是否有沉淀生成
C.分别在它们的酸性溶液中加入FeCl2溶液,观察溶液颜色变化
II.(3)H3PO2是精细磷化工产品。工业制备原理如下:
a.2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑
b.Ba(H2PO2)2+H2SO4=BaSO4↓+2H3PO2
下列推断正确的是__________
A.反应a是氧化还原反应,反应b是复分解反应
B.H3PO2中P化合价是+1
C.在反应a中发生氧化反应与还原反应的原子个数之比为1:1
(4)某离子反应涉及到H2O、ClO-、NH 、OH-、N2、Cl-等微粒,其中N2、ClO-的粒子数随时间变化的曲线如图所示,请写出反应的离子方程
、OH-、N2、Cl-等微粒,其中N2、ClO-的粒子数随时间变化的曲线如图所示,请写出反应的离子方程_______ ,ClO-表现出______ 性。

(5)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴滴入物质M的饱和水溶液,继续煮沸至液体呈红褐色,停止加热。写出该过程反应的化学方程式_______ 。
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐,如NaNO2,则导致血红蛋白中的Fe2+转化为Fe3+而中毒(FeCl2溶液为浅绿色,FeCl3溶液为棕黄色),可以服用维生素C解毒,维生素C在解毒的过程中表现出
(2)下列方法中,不能用来区分NaNO2和NaCl的是
A.测溶液的酸碱性
B.加入AgNO3溶液观察是否有沉淀生成
C.分别在它们的酸性溶液中加入FeCl2溶液,观察溶液颜色变化
II.(3)H3PO2是精细磷化工产品。工业制备原理如下:
a.2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑
b.Ba(H2PO2)2+H2SO4=BaSO4↓+2H3PO2
下列推断正确的是
A.反应a是氧化还原反应,反应b是复分解反应
B.H3PO2中P化合价是+1
C.在反应a中发生氧化反应与还原反应的原子个数之比为1:1
(4)某离子反应涉及到H2O、ClO-、NH
 、OH-、N2、Cl-等微粒,其中N2、ClO-的粒子数随时间变化的曲线如图所示,请写出反应的离子方程
、OH-、N2、Cl-等微粒,其中N2、ClO-的粒子数随时间变化的曲线如图所示,请写出反应的离子方程
(5)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴滴入物质M的饱和水溶液,继续煮沸至液体呈红褐色,停止加热。写出该过程反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】有个成语叫“物以类聚”,本意就是物质的分类。对物质进行分类,我们不仅能够根据类别通性预测物质的性质,还能探索各类物质的共性和特性。化学家根据需要将众多物质进行分类,现有下列几种物质:①冰水混合物 ②N2 ③CO ④Fe(OH)3胶体 ⑤Mg ⑥熔融Ca(OH)2 ⑦漂白粉 ⑧乙醇 ⑨盐酸。
(1)属于非电解质的是_______ (填序号,下同);属于强电解质的是_______ ;上述物质中弱电解质的电离方程式:_______ 。
(2)写出实验室制取④的化学方程式:_______ 。
(3)生活中“84”消毒液(有效成分为NaClO)和洁厕灵(主要成分是⑨ )不能混合使用,原因是_______ (用离子方程式表示)。
(4)新型陶瓷氮化铝可用氧化铝高温还原法制备: (未配平),若反应中共转移3.01×1023个电子,则产生CO气体的物质的量为
(未配平),若反应中共转移3.01×1023个电子,则产生CO气体的物质的量为_______ mol。
(1)属于非电解质的是
(2)写出实验室制取④的化学方程式:
(3)生活中“84”消毒液(有效成分为NaClO)和洁厕灵(主要成分是⑨ )不能混合使用,原因是
(4)新型陶瓷氮化铝可用氧化铝高温还原法制备:
 (未配平),若反应中共转移3.01×1023个电子,则产生CO气体的物质的量为
(未配平),若反应中共转移3.01×1023个电子,则产生CO气体的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈_________ 色,停止加热,可制得Fe(OH)3胶体。若向制得的胶体中加入过量稀硫酸,反应的离子方程式为____________________ 。
(2)现有下列物质:①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸 ⑤FeCl3溶液 ⑥铜 ⑦蔗糖 ⑧熔化的NaCl,其中能导电的物质有________________ (填序号),属于电解质的有____________ (填序号)。
(3)①标准状况下,11.2L NH3中含_____________ 个氨分子。
②12.4g Na2R含Na+ 0.4mol,则Na2R的摩尔质量为_____________ g/mol。
③10mL 3mol/L稀硫酸加水稀释到200mL,稀释后c(H+)=_____________ 。
(2)现有下列物质:①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸 ⑤FeCl3溶液 ⑥铜 ⑦蔗糖 ⑧熔化的NaCl,其中能导电的物质有
(3)①标准状况下,11.2L NH3中含
②12.4g Na2R含Na+ 0.4mol,则Na2R的摩尔质量为
③10mL 3mol/L稀硫酸加水稀释到200mL,稀释后c(H+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知:25℃时,①亚硫酸(H2SO3)的电离平衡常数为K1=1.6×10-2,K2=1.0×10-7;②次氨酸(HClO)的电离平衡常数为K1=4.0×10-8;③碳酸(H2CO3)的电离平衡常数为K1=4.0×10-7,K1=4.0×10-11。回答下列问题:
(1)HClO的电离方程式为____ 。
(2)上述三种酸由强到弱的顺序为(填分子式)____ 。
(3)向H2SO3溶液中加入Ba(OH)2溶液时,溶液中c(H+)____ (填“增大”、“减小”或“不变”,下同),c(SO )
)____ 。
(4)足量的H2SO3溶液和NaHCO3溶液发生反应的主要离子方程式为____ 。
(5)向0.1mol·L-1的HClO溶液中滴加等体积的一定浓度的稀硫酸,此时测得溶液中的c(H+)=0.05mol·L-1,则溶液中c(ClO-)____ mol·L-1。
(1)HClO的电离方程式为
(2)上述三种酸由强到弱的顺序为(填分子式)
(3)向H2SO3溶液中加入Ba(OH)2溶液时,溶液中c(H+)
 )
)(4)足量的H2SO3溶液和NaHCO3溶液发生反应的主要离子方程式为
(5)向0.1mol·L-1的HClO溶液中滴加等体积的一定浓度的稀硫酸,此时测得溶液中的c(H+)=0.05mol·L-1,则溶液中c(ClO-)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】高纯二氧化硅可用来制造光导纤维。某稻壳灰的成分为
通过如下流程可由稻壳灰制备较纯净的二氧化硅。

请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物最多有____ 类,其中SiO2属于____ 。
(2)步骤①中涉及SiO2反应的离子方程式为____ 。
(3)滤渣A的成分有____ (填化学式)。
(4)步骤③反应的化学方程式为____ 。
(5)步骤②中的过量盐酸是否可以用过量CO2来替代:____ 。(用文字简要描述原因)
| 组分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.61 |
通过如下流程可由稻壳灰制备较纯净的二氧化硅。

请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物最多有
(2)步骤①中涉及SiO2反应的离子方程式为
(3)滤渣A的成分有
(4)步骤③反应的化学方程式为
(5)步骤②中的过量盐酸是否可以用过量CO2来替代:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求完成下列填空
(1)检验铁离子(Fe3+):试剂____________ (填化学式);现象______________ 。有铁离子(Fe3+)的环境下检验是否含有亚铁离子(Fe2+):试剂:_________ (填化学式),现象_______________ 。
(2)用小苏打片治疗胃酸过多的离子方程式为____________ 。
(3)镁带着火时,不能用液态CO2灭火剂来灭火的原因是_____________ 。(用化学方程式表示).
(4)除去混入Fe2O3粉末中少量Al2O3杂质离子方程式为______________ 。
(5)将AlCl3溶液蒸干,灼烧,得到的固体产物是__________ 。AlCl3溶液和NaHCO3溶液混合时发生反应的离子方程式为_________________ 。
(1)检验铁离子(Fe3+):试剂
(2)用小苏打片治疗胃酸过多的离子方程式为
(3)镁带着火时,不能用液态CO2灭火剂来灭火的原因是
(4)除去混入Fe2O3粉末中少量Al2O3杂质离子方程式为
(5)将AlCl3溶液蒸干,灼烧,得到的固体产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】铁元素及其化合物在生活生产中有广泛的用途。回答下列问题:
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN- Fe(SCN)3
Fe(SCN)3
若溶液中含有Fe3+,则加入KSCN溶液后的现象为_________ 向加入KSCN后的混合溶液中再加入少量NaOH固体,观察到的现象是_____________ ,产生该现象的原因是________________ 。
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因__________________ 。
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生______ 、________ 两个反应(写离子方程式),若最后溶液中有固体剩余,则溶液中不可能含有的离子是____ 。
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为_____________ 若要验证该溶液中Fe2+未被完全氧化,则可以需要加入_____ 若出现_________ 现象,则证明Fe2+未被完全氧化。
(5)下列有关铁及其化合物的说法正确的是________
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN-
 Fe(SCN)3
Fe(SCN)3 若溶液中含有Fe3+,则加入KSCN溶液后的现象为
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为
(5)下列有关铁及其化合物的说法正确的是
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】钠、铝、铁是三种非常重要的常见金属。根据所学知识完成下列填空。
(1)将一小块金属钠投入足量水中,发生反应的离子方程式为_______ 。
(2)足量的Fe在Cl2中点燃,所得产物的化学式是_______ 。将该产物溶于水配成溶液,分装在两支试管中。
a.若向其中一支试管中滴加KSCN溶液,则溶液变成_______ 色。
b.向另一支试管中滴加NaOH溶液,现象为_______ 。
(3)纯铝片投入氢氧化钠溶液中产生气泡的化学方程式为_______ 。若2.7g纯铝片投入足量盐酸中产生氢气的物质的量为_______ mol。
(1)将一小块金属钠投入足量水中,发生反应的离子方程式为
(2)足量的Fe在Cl2中点燃,所得产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,现象为
(3)纯铝片投入氢氧化钠溶液中产生气泡的化学方程式为
您最近一年使用:0次



