下列叙述正确的是
| A.电解池将化学能转化为电能 |
| B.在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 |
| C.用惰性电极电解饱和NaCl溶液一段时间后,若 通入氯化氢气体,能使电解液恢复到原状态 |
| D.用惰性电极电解Na2SO4溶液,阴阳两极气体产物的物质的量之比为1:2 |
更新时间:2018-01-06 10:40:48
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)能自发进行,则△H<0 |
| B.铁片镀锌时,铁片与外电源的正极相连 |
| C.以熔融NaCl为电解质进行电解冶炼钠,熔融体中Na+向阳极移动 |
D.t℃时,恒容密闭容器中反应:NO2(g)+SO2(g) NO(g)+SO3(g),通入少量O2, NO(g)+SO3(g),通入少量O2, 的值及SO2转化率不变 的值及SO2转化率不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用电解氧化法可以在铝制品表面形成致密、耐腐蚀的氧化膜,电解质溶液一般为H2SO4 H2C2O4混合溶液。下列叙述正确的是
H2C2O4混合溶液。下列叙述正确的是
 H2C2O4混合溶液。下列叙述正确的是
H2C2O4混合溶液。下列叙述正确的是| A.待加工铝质工件作阳极 |
| B.可选用不锈钢网作为阳极 |
| C.阴极的电极反应式为Al-3e-=Al3+ |
| D.硫酸根离子在电解过程中向阴极移动 |
您最近一年使用:0次
【推荐3】下列说法正确的一组是
①按照纯净物、混合物、强电解质、弱电解质和非电解质顺序排列的是CuSO4·5H2O、漂白粉、苛性钠、次氯酸、氮气
②电解质溶液导电的原因是电解质在外界电源的作用下电离出能自由移动的阴阳离子
③Na与HCl反应是放热反应,而NaHCO3与HCl反应是吸热反应
④由于离子键作用力很强,所以离子晶体的熔点都很高
⑤马口铁(镀锡)表面出现破损时,腐蚀速率会加快
⑥电解精炼铜,阳极为纯铜,阴极为粗铜
①按照纯净物、混合物、强电解质、弱电解质和非电解质顺序排列的是CuSO4·5H2O、漂白粉、苛性钠、次氯酸、氮气
②电解质溶液导电的原因是电解质在外界电源的作用下电离出能自由移动的阴阳离子
③Na与HCl反应是放热反应,而NaHCO3与HCl反应是吸热反应
④由于离子键作用力很强,所以离子晶体的熔点都很高
⑤马口铁(镀锡)表面出现破损时,腐蚀速率会加快
⑥电解精炼铜,阳极为纯铜,阴极为粗铜
| A.①③⑤ | B.②④⑥ | C.③④⑤ | D.②③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】氢氧化锂(LiOH)可用作光谱分析的展开剂、润滑油,某兴趣小组利用三室电解法制备氢氧化锂,同时得到重要工业原料硫酸,其工作原理如图所示。下列说法正确的是
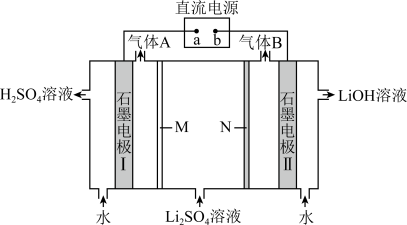

| A.a为负极 |
| B.N为阳离子交换膜 |
| C.石墨电极Ⅱ的电极反应式为:O2+4e-+2H2O=4OH- |
| D.制备2.4 g氢氧化锂,理论上生成气体A 1.12 L(标准状况下) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )| A.放电时负极反应:Zn-2e-+2H2O=Zn(OH)2+2H+ |
B.充电时阳极上反应:Fe(OH)3-3e-+5OH-= +4H2O +4H2O |
| C.充电时每转移3 mol电子,阴极有1 mol K2FeO4生成 |
| D.放电时负极附近溶液的碱性增强 |
您最近一年使用:0次

 为电解质,以Mg-Al-Si合金为某一电极进行电解,实现合金中Mg与Al的分离。下列说法正确的是
为电解质,以Mg-Al-Si合金为某一电极进行电解,实现合金中Mg与Al的分离。下列说法正确的是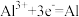
 的物质的量始终不变
的物质的量始终不变