将铁粉、铜粉加入到盛有FeCl3、FeCl2、CuCl2的混合液的烧杯中,判断下列情况烧杯中的固体及金属阳离子(用化学式表示):
(1)若反应后铁粉有剩余,则一定有______________ 。
(2)若反应后有Cu2+和Cu,则不可能有_________ 。
(3)若反应后有Cu2+和Fe3+,则一定有_______________ 。
(1)若反应后铁粉有剩余,则一定有
(2)若反应后有Cu2+和Cu,则不可能有
(3)若反应后有Cu2+和Fe3+,则一定有
17-18高一上·山东泰安·期末 查看更多[4]
山东省泰安市2017-2018学年高一上学期期末考试化学试题【全国百强校】江西省高安中学2017-2018学年高二下学期期末考试化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》 第三单元 金属及其化合物单元测试 A卷江西省会昌中学2020-2021学年高一上学期第二次月考化学试题
更新时间:2018-03-04 16:39:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求正确书写方程式:
(1)过氧化钠与水反应的化学方程式:________ 。
(2)泡沫灭火器灭火原理的离子方程式:________ 。
(3)铝单质与氢氧化钠溶液反应的离子方程式:________ 。
(4)将H2S气体通入FeCl3溶液中产生淡黄色沉淀的离子方程式:________ 。
(5)四氧化三铁溶于足量氢碘酸溶液的离子方程式:________ 。
(1)过氧化钠与水反应的化学方程式:
(2)泡沫灭火器灭火原理的离子方程式:
(3)铝单质与氢氧化钠溶液反应的离子方程式:
(4)将H2S气体通入FeCl3溶液中产生淡黄色沉淀的离子方程式:
(5)四氧化三铁溶于足量氢碘酸溶液的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】过去电子工业常用30%的FeCl3溶液腐蚀敷有铜箔的绝缘板,制成印刷线路板,发生反应的化学方程式为:2FeCl3+Cu=2FeCl2+CuCl2。
(1)检验腐蚀后的溶液中是否含有Fe3+应选用的试剂是_________ ,该反应说明Fe3+氧化性比Cu2+氧化性_________ (填“强”或“弱” )。
(2)采用下列实验步骤从使用过的腐蚀废液中回收铜,并重新制得纯净的FeCl3溶液,其中步骤①中加过量的铁粉,③中加过量的盐酸,⑤中通入过量的氯气,请按要求填空。

C处物质的化学式为________ 分别写出步骤①、⑤中反应的离子方程式①_________ 、______ ⑤____
(1)检验腐蚀后的溶液中是否含有Fe3+应选用的试剂是
(2)采用下列实验步骤从使用过的腐蚀废液中回收铜,并重新制得纯净的FeCl3溶液,其中步骤①中加过量的铁粉,③中加过量的盐酸,⑤中通入过量的氯气,请按要求填空。

C处物质的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铁、钴(Co)、镍(Ni)是同族元素,主要化合价均为+2、+3价,都是较活泼的金属,它们的化合物在工业上有重要的应用。完成下列填空:
(1)Co2+和Fe3+均可与KSCN溶液发生相似的反应。向CoCl2溶液中加入KSCN溶液,生成某种带有两个单位负电荷的蓝色离子,其化学式为_______________________ 。
(2)碳酸镍可用于电镀、陶瓷器着色等。镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS,从镍矿渣出发制备碳酸镍的反应如下:
第一步:向镍矿渣中加入稀硫酸和NaClO3浸取出Ni2+。
反应的离子方程式有:
①__________ ;
②___NiS+___ +___H+→___Ni2++___S+___Cl-+___H2O
+___H+→___Ni2++___S+___Cl-+___H2O
配平反应②。__________
第二步:再加入Na2CO3溶液,产生的沉淀即为碳酸镍。
检验Ni2+是否沉淀完全的方法是_____________________________________ 。
(1)Co2+和Fe3+均可与KSCN溶液发生相似的反应。向CoCl2溶液中加入KSCN溶液,生成某种带有两个单位负电荷的蓝色离子,其化学式为
(2)碳酸镍可用于电镀、陶瓷器着色等。镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS,从镍矿渣出发制备碳酸镍的反应如下:
第一步:向镍矿渣中加入稀硫酸和NaClO3浸取出Ni2+。
反应的离子方程式有:
①
②___NiS+___
 +___H+→___Ni2++___S+___Cl-+___H2O
+___H+→___Ni2++___S+___Cl-+___H2O配平反应②。
第二步:再加入Na2CO3溶液,产生的沉淀即为碳酸镍。
检验Ni2+是否沉淀完全的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知电子工业上常用FeCl3溶液来溶解电路板中的铜。某一反应体系有反应物和生成物共三种物质:FeCl3、FeCl2、Fe。完成下列问题:
(1)该反应中的还原产物的化学式是____________ ,氧化产物的化学式是____________ 。
(2)该反应中,发生还原反应的过程是(填化学式)_______ →__________ 。
(3)该反应的离子方程式为:_____________________________ 。
(4)标出该反应电子转移的方向和数目______________________________
(5)如反应转移了0.3mol电子,则_______ (填“溶解”或“生成”)的铁的质量为_________ 。
(1)该反应中的还原产物的化学式是
(2)该反应中,发生还原反应的过程是(填化学式)
(3)该反应的离子方程式为:
(4)标出该反应电子转移的方向和数目
(5)如反应转移了0.3mol电子,则
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】纳米磁性流体材料广泛应用于减震、医疗器械、声音调节等高科技领域。下图是制备纳米Fe3O4磁流体的两种流程:
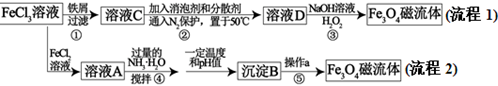
(1)分析流程图中的两种流程,其中_________ (填“流程1”、“流程2”)所有反应不涉及氧化还原反应。步骤①反应的离子方程式为____________ 。
(2)步骤②保持50℃的做法是_________ 。
(3)步骤③中加入的H2O2电子式是_______ ,步骤③制备Fe3O4磁流体的化学方程式为________ 。
(4)流程2中FeCl3和FeCl2制备Fe3O4磁流体,理论上FeCl3和FeCl2物质的量之比为_________ 。已知沉淀B为四氧化三铁,步骤⑤中操作a具体的步骤是_____________ 。
(5)利用K2Cr2O7可测定Fe3O4磁流体中的Fe2+含量。若Fe3O4磁流体与K2Cr2O7充分反应消耗了0.01 mol·L-1的K2Cr2O7标准溶液100 mL,则磁流体中含有Fe2+的物质的量为_____ mol。若配制的K2Cr2O7标准溶液装在__________ (填“酸式滴定管”或“碱式滴定管”)时,滴定前平视刻度线,滴定后仰视刻度线,则测定结果是Fe3O4磁流体中的Fe2+含量_____ (填“偏大”、“偏小”或“不变”)。

(1)分析流程图中的两种流程,其中
(2)步骤②保持50℃的做法是
(3)步骤③中加入的H2O2电子式是
(4)流程2中FeCl3和FeCl2制备Fe3O4磁流体,理论上FeCl3和FeCl2物质的量之比为
(5)利用K2Cr2O7可测定Fe3O4磁流体中的Fe2+含量。若Fe3O4磁流体与K2Cr2O7充分反应消耗了0.01 mol·L-1的K2Cr2O7标准溶液100 mL,则磁流体中含有Fe2+的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】FeCl3是一种重要的化工产品:
(1)电子工业用FeCl3腐蚀铜的原理制造印刷电路板,写出FeCl3与Cu反应的离子方程式: 。
(2)某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
首先取少量待测溶液,滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是 ;在此基础上,又进行了定量组成的测定:
①取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为43.05 g.溶液中c(Cl-)= mol/L。
②再取50.0 mL待测溶液,向其中加入过量稀硝酸,得到0.448 L(标准状况下)一种无色气体.写出反应的离子方程式: ,待测溶液中c(Cu2+)= mol/L。
(1)电子工业用FeCl3腐蚀铜的原理制造印刷电路板,写出FeCl3与Cu反应的离子方程式: 。
(2)某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
首先取少量待测溶液,滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是 ;在此基础上,又进行了定量组成的测定:
①取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为43.05 g.溶液中c(Cl-)= mol/L。
②再取50.0 mL待测溶液,向其中加入过量稀硝酸,得到0.448 L(标准状况下)一种无色气体.写出反应的离子方程式: ,待测溶液中c(Cu2+)= mol/L。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁在工农业生产、生活等方面都有重要的应用。
(1)正常人体内铁元素以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收。在人体中进行Fe3+→Fe2+的转化时,Fe3+作___ 剂,发生___ 反应。
(2)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的化学方程式并用双线桥表明电子得失情况___ 。
(3)将单质Fe、Cu与FeCl3溶液、FeCl2溶液、CuCl2溶液(已知:氧化性Fe3+﹥Cu2+)混合于某容器内充分反应(假定容器不参加反应)。根据下述不同情况,填写金属单质或溶液中存在的金属离子。
①若Fe有剩余,则容器内不可能有的离子是:___ ;铜单质___ (填“一定”或“可能”)存在。
②若容器内有较多Cu2+和Cu,则容器内不可能有___ 。
③若容器内有大量的Fe3+,则容器内一定还有___ 。证明该溶液中Fe3+存在的试剂是___ ,现象为___ 。
(1)正常人体内铁元素以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收。在人体中进行Fe3+→Fe2+的转化时,Fe3+作
(2)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的化学方程式并用双线桥表明电子得失情况
(3)将单质Fe、Cu与FeCl3溶液、FeCl2溶液、CuCl2溶液(已知:氧化性Fe3+﹥Cu2+)混合于某容器内充分反应(假定容器不参加反应)。根据下述不同情况,填写金属单质或溶液中存在的金属离子。
①若Fe有剩余,则容器内不可能有的离子是:
②若容器内有较多Cu2+和Cu,则容器内不可能有
③若容器内有大量的Fe3+,则容器内一定还有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学与人类生活密切相关。请按要求,回答下列问题:
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是_____ ,当反应中有1mol K2FeO4生成时,消耗Cl2在标况下的体积为_________ L,转移电子的数目为_____ 。
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:_____________________________________________ 。
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:___________ 。
(4)工业上制漂白粉的化学方程式为_______________________________ ,新制氯水在阳光照射下产生无色气体,该反应的化学方程式是______ 。
(5)KA1(SO4)2•12H2O因其溶于水生成_____ (化学式)可以吸附杂质,从而达到净水作用。
(6)硅钢具有很高的_____ ,主要用作变压器的铁芯;硅酸钠水溶液的俗名为______ ,可作为木材________________ 的原料。
(7)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:________________________________ 。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是________ 。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH
 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:
(4)工业上制漂白粉的化学方程式为
(5)KA1(SO4)2•12H2O因其溶于水生成
(6)硅钢具有很高的
(7)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某固体化合物X由5种元素组成。某学习小组进行了如图实验:

已知气体B能使湿润红色石蕊试纸变蓝。请回答:
(1)X中含有的元素有___ ,气体B的电子式___ 。
(2)X的化学式__ 。
(3)X的水溶液可以与纤维素作用,工业上利用此性质得到产物名称__ 。
(4)写出X隔绝空气强热生成A、D、E的化学方程式___ 。

已知气体B能使湿润红色石蕊试纸变蓝。请回答:
(1)X中含有的元素有
(2)X的化学式
(3)X的水溶液可以与纤维素作用,工业上利用此性质得到产物名称
(4)写出X隔绝空气强热生成A、D、E的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】由两种元素组成的矿物A,测定A的组成及制取化合物D的流程如下:请回答:
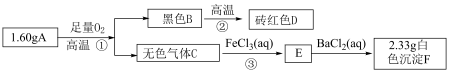
⑴D的化学式为________________________ ;
⑵写出③的离子方程式:___________________________ ;
⑶A的化学式为:______________________ 。

⑴D的化学式为
⑵写出③的离子方程式:
⑶A的化学式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】地球上的金属矿物资源是有限的,应合理开发利用。
(1)金属冶炼的实质是金属离子被______ (填“氧化”或“还原”)生成金属单质。
(2)铜在自然界存在于多种矿石中,如:
请回答下列问题:
① 上表所列铜化合物中,推断铜的质量百分含量最高的是______ 。
② CuFeS2其中 Cu 为+1 价、Fe 为+3 价,高温焙烧时发生的反应是CuFeS2 + O2 SO2 +FeS +Cu,焙烧过程中被还原的元素有
SO2 +FeS +Cu,焙烧过程中被还原的元素有______ 。
③ 工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:Cu2S+O2 2Cu+SO2,该反应中氧化剂是
2Cu+SO2,该反应中氧化剂是______ 。
④ Cu2(OH)2 CO3 与稀硫酸反应的离子方程式为______ 。
(1)金属冶炼的实质是金属离子被
(2)铜在自然界存在于多种矿石中,如:
| 矿石名称 | 黄铜矿 | 辉铜矿 | 孔雀石 |
| 主要成分 | CuFeS2 | Cu2S | Cu2(OH)2 CO3 |
请回答下列问题:
① 上表所列铜化合物中,推断铜的质量百分含量最高的是
② CuFeS2其中 Cu 为+1 价、Fe 为+3 价,高温焙烧时发生的反应是CuFeS2 + O2
 SO2 +FeS +Cu,焙烧过程中被还原的元素有
SO2 +FeS +Cu,焙烧过程中被还原的元素有③ 工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:Cu2S+O2
 2Cu+SO2,该反应中氧化剂是
2Cu+SO2,该反应中氧化剂是④ Cu2(OH)2 CO3 与稀硫酸反应的离子方程式为
您最近一年使用:0次



