某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究。
查阅资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O
探究一:用如图所示装置进行实验,回答下列问题:_____ ,则说明装置A的气密性良好.
(2)装置A是氢气的发生装置,可以选用的药品是________ (填选项)
A.稀硫酸和锌片 B.稀硝酸和铁片 C.氢氧化钠溶液和铝片 D.浓硫酸和镁片
(3)从下列实验步骤中,选择正确的操作顺序:①________ ③(填序号).
①打开止水夹 ②熄灭C处的酒精喷灯 ③C处冷却至室温后,关闭止水夹
④点燃C处的酒精喷灯 ⑤收集氢气并验纯 ⑥通入气体一段时间,排尽装置内的空气
探究二:
(4)甲同学取少量样品于试管中,加入适量的稀硫酸,若无红色物质生成,则说明样品中不含Cu2O;乙同学认为观点不正确,其原因是_____________ ;丙同学另取少量样品于试管中,加入适量的浓硝酸,产生红棕色的气体.证明样品中一定含有________ ,其反应的离子方程式为_____ ;丁同学预设计实验证明另一种物质是否存在,其方案为__________ 。
(5)取一定量样品于烧杯中,加入足量的稀硫酸,若反应后经过滤得到固体3.2g,滤液中Fe2+有1.0mol,则样品中n(Cu2O)=_________ mol.
查阅资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O
探究一:用如图所示装置进行实验,回答下列问题:
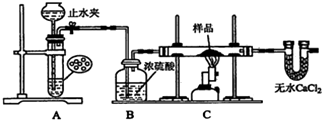
(2)装置A是氢气的发生装置,可以选用的药品是
A.稀硫酸和锌片 B.稀硝酸和铁片 C.氢氧化钠溶液和铝片 D.浓硫酸和镁片
(3)从下列实验步骤中,选择正确的操作顺序:①
①打开止水夹 ②熄灭C处的酒精喷灯 ③C处冷却至室温后,关闭止水夹
④点燃C处的酒精喷灯 ⑤收集氢气并验纯 ⑥通入气体一段时间,排尽装置内的空气
探究二:
(4)甲同学取少量样品于试管中,加入适量的稀硫酸,若无红色物质生成,则说明样品中不含Cu2O;乙同学认为观点不正确,其原因是
(5)取一定量样品于烧杯中,加入足量的稀硫酸,若反应后经过滤得到固体3.2g,滤液中Fe2+有1.0mol,则样品中n(Cu2O)=
更新时间:2018/03/31 21:58:54
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】氧化亚铜(Cu2O)是一种用途广泛的光电材料,某工厂以硫化铜矿石(含CuFeS2、Cu2S等)为原料制取Cu2O的工艺流程如下:
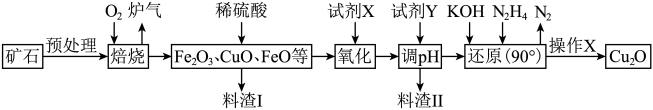
常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
(1)炉气中的有害气体成分是__________ ,Cu2S与O2反应时,氧化剂与还原剂的物质的量之比为__________ 。
(2)若试剂X是H2O2溶液,写出相应反应的离子方程式:__________ 。并写出H2O2的电子式__________ ,Fe(铁)在元素周期表中的位置:__________ ;当试剂X是__________ 时,更有利于降低生产成本。
(3)加入试剂Y调pH时,pH的调控范围是__________ 。
(4)操作X包括__________ 、洗涤、烘干,其中烘干时要隔绝空气,其目的是__________ 。
(5)以铜与石墨作电极,电解浓的强碱性溶液可制得纳米级Cu2O,写出阳极上生成Cu2O的电极反应式:__________ 。

常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
| Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀 | 7.5 | 2.7 | 4.8 |
| 完全沉淀 | 9.0 | 3.7 | 6.4 |
(1)炉气中的有害气体成分是
(2)若试剂X是H2O2溶液,写出相应反应的离子方程式:
(3)加入试剂Y调pH时,pH的调控范围是
(4)操作X包括
(5)以铜与石墨作电极,电解浓的强碱性溶液可制得纳米级Cu2O,写出阳极上生成Cu2O的电极反应式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】氧化亚铜(Cu2O)是一种用途广泛的光电材料,某工厂以硫化铜矿石(含 CuFeS2、Cu2S等)为原料制取Cu2O的工艺流程如下:
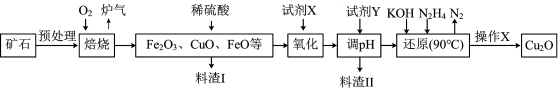
(1) “焙烧”时,提高反应速率的措施有____________ (写一条)。
(2)炉气中的有害气体成分是__________ 。
(3)若试剂X是H2O2溶液,写出相应反应的离子方程式:_________ 。

(1) “焙烧”时,提高反应速率的措施有
(2)炉气中的有害气体成分是
(3)若试剂X是H2O2溶液,写出相应反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某化学研究性学习小组探究与铜有关的物质的性质,过程设计如下:
(提出猜想)
问题1:在周期表中,铜与铝的位置很接近,氢氧化铝具有两性,氢氧化铜有两性码?
问题2:铁和铜都有变价,一般情况下,Fe2+的稳定性小于的Fe3+,Cu+的稳定性也小于Cu2+吗?
问题3:硫酸铜溶液呈蓝色,铜与浓硝酸常温下反应生成的溶液也是蓝色吗?
(实验探究)
I. 解决问题1:
(1)实验需配制100mL 0.50mol·L-1 CuSO4溶液,除了天平、烧杯、玻璃棒、胶头滴管以外必需的玻璃仪器是______ 。
(2)为达到目的,某同学认为只要进行两次实验即可得出结论。请写出实验②的具体内容。
①向盛有CuSO4溶液的试管中滴加NaOH溶液至过量,观察生成的Cu(OH)2沉淀是否溶解;
②_______ 。
II. 解决问题2的实验步骤和现象如下:
①取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80ºC~100ºC得到黑色固体粉末;继续加热至1000ºC以上,黑色粉末全部变成红色粉末氧化亚铜(Cu2O);
②取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸,得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验及现象:
(3)写出氧化亚铜与稀硫酸反应的离子方程式____________________________ 。
(4)从实验中可得出的结论是:当温度在1000ºC以上时________ (填:Cu2+或Cu+,下同)稳定,在酸性溶液中________ 稳定。
III. 解决问题3,某同学设计的实验如下:取一铜片装入试管,加入适量的浓硝酸,观察溶液的颜色变化。
(5)另一同学认为此同学设计的实验有缺陷,原因是__________________________ 。
(6)铜与浓硝酸反应溶液呈绿色,有同学认为这是生成的NO2溶于其中的原因,并试图设计实验排除这种干扰。提出实验方案:向反应后的溶液中通入足量空气。试用化学反应方程式解释其原理:___________________________
(提出猜想)
问题1:在周期表中,铜与铝的位置很接近,氢氧化铝具有两性,氢氧化铜有两性码?
问题2:铁和铜都有变价,一般情况下,Fe2+的稳定性小于的Fe3+,Cu+的稳定性也小于Cu2+吗?
问题3:硫酸铜溶液呈蓝色,铜与浓硝酸常温下反应生成的溶液也是蓝色吗?
(实验探究)
I. 解决问题1:
(1)实验需配制100mL 0.50mol·L-1 CuSO4溶液,除了天平、烧杯、玻璃棒、胶头滴管以外必需的玻璃仪器是
(2)为达到目的,某同学认为只要进行两次实验即可得出结论。请写出实验②的具体内容。
①向盛有CuSO4溶液的试管中滴加NaOH溶液至过量,观察生成的Cu(OH)2沉淀是否溶解;
②
II. 解决问题2的实验步骤和现象如下:
①取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80ºC~100ºC得到黑色固体粉末;继续加热至1000ºC以上,黑色粉末全部变成红色粉末氧化亚铜(Cu2O);
②取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸,得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验及现象:
(3)写出氧化亚铜与稀硫酸反应的离子方程式
(4)从实验中可得出的结论是:当温度在1000ºC以上时
III. 解决问题3,某同学设计的实验如下:取一铜片装入试管,加入适量的浓硝酸,观察溶液的颜色变化。
(5)另一同学认为此同学设计的实验有缺陷,原因是
(6)铜与浓硝酸反应溶液呈绿色,有同学认为这是生成的NO2溶于其中的原因,并试图设计实验排除这种干扰。提出实验方案:向反应后的溶液中通入足量空气。试用化学反应方程式解释其原理:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】 的防治与利用对于环境保护意义重大。某小组在实验室中对
的防治与利用对于环境保护意义重大。某小组在实验室中对 的性质及回收利用等相关问题进行探究。
的性质及回收利用等相关问题进行探究。
(1)用如图装置制备纯净的 ,装置中盛放
,装置中盛放 的仪器名称为
的仪器名称为_______ 。

(2)装置中发生反应的化学方程式为_______ ,装置的连接顺序为:a→_______ (按气流方向,用小写字母表示)。
(3)用如图装置探究 的性质。限选试剂:NaOH溶液、稀
的性质。限选试剂:NaOH溶液、稀 、
、 溶液、
溶液、 溶液、
溶液、 溶液、酸性高锰酸钾溶液、淀粉-KI溶液、新制
溶液、酸性高锰酸钾溶液、淀粉-KI溶液、新制 溶液和品红溶液。小组同学设计方案并进行实验。请完成下表中的内容。
溶液和品红溶液。小组同学设计方案并进行实验。请完成下表中的内容。

(4)若向实验三所得溶液中通入_______(填选项字母),可观察到有白色沉淀生成。
(5)小组同学为探究 对品红漂白作用的可逆性,需进行的实验操作及现象为
对品红漂白作用的可逆性,需进行的实验操作及现象为_______ 。
 的防治与利用对于环境保护意义重大。某小组在实验室中对
的防治与利用对于环境保护意义重大。某小组在实验室中对 的性质及回收利用等相关问题进行探究。
的性质及回收利用等相关问题进行探究。(1)用如图装置制备纯净的
 ,装置中盛放
,装置中盛放 的仪器名称为
的仪器名称为
(2)装置中发生反应的化学方程式为
(3)用如图装置探究
 的性质。限选试剂:NaOH溶液、稀
的性质。限选试剂:NaOH溶液、稀 、
、 溶液、
溶液、 溶液、
溶液、 溶液、酸性高锰酸钾溶液、淀粉-KI溶液、新制
溶液、酸性高锰酸钾溶液、淀粉-KI溶液、新制 溶液和品红溶液。小组同学设计方案并进行实验。请完成下表中的内容。
溶液和品红溶液。小组同学设计方案并进行实验。请完成下表中的内容。
| 操作步骤 | 实验现象 | 解释原因 | |
| 实验一 | 用注射器将新制 溶液注入充满 溶液注入充满 的烧瓶中 的烧瓶中 | 出现淡黄色浑浊 |  具有 具有 |
| 实验二 | 用注射器将 的烧瓶中 的烧瓶中 |  具有还原性,反应的离子方程式为 具有还原性,反应的离子方程式为 | |
| 实验三 | 用注射器将 溶液注入充满 溶液注入充满 的烧瓶中 的烧瓶中 | 无明显现象 | …… |
| 实验四 | 用注射器将品红溶液注入充满 的烧瓶中 的烧瓶中 | 品红溶液褪色 |  具有漂白性 具有漂白性 |
A. | B. | C. | D.HCl |
 对品红漂白作用的可逆性,需进行的实验操作及现象为
对品红漂白作用的可逆性,需进行的实验操作及现象为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某同学设计实验制备 并探究其性质。
并探究其性质。
①仪器X的名称为_______ ;氨气的发生装置可选用上图中的________ ,反应的化学方程式为__________ 。
②欲收集一瓶干燥的氨气,选用上图中的装置,其连接顺序为:发生装置→________ (按气流方向,用小写字母表示)。
(2)氨气的性质实验。已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,装置如图所示。实验时H中出现无色液体。_________ ,G中的现象为__________ 。
②向H中的无色液体中滴入紫色石蕊试液的现象为_________ ,原因是___________ 。(用方程式表示)
 并探究其性质。
并探究其性质。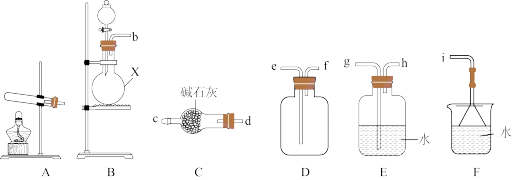
①仪器X的名称为
②欲收集一瓶干燥的氨气,选用上图中的装置,其连接顺序为:发生装置→
(2)氨气的性质实验。已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,装置如图所示。实验时H中出现无色液体。

②向H中的无色液体中滴入紫色石蕊试液的现象为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】84消毒液是杀菌性强、杀菌范围广的产品,以次氯酸钠为主要成分。
I.84消毒液有效氯是指单位体积消毒液含与NaClO消毒能力相当的氯气的质量(1molNaClO消毒能力与1mol氯气相当),一般市售84消毒液有效氯为55-60g/L。

(1)某兴趣小组通过实验测得某品牌84消毒液有效氯为56.8g/L,假设有效氯都来自次氯酸钠,则该消毒液中NaClO的物质的量浓度为_______ 。
(2)将该品牌消毒液准确稀释成有效氯为568mg/L的稀溶液500mL,用于餐具消毒。
①实验中需要的玻璃仪器除量筒、胶头滴管、烧杯外还要_______ ;
②下列操作会导致有效氯偏低的是_______ (填字母序号);
A.容量瓶用蒸馏水洗涤后未干燥 B.用量筒量取84消毒液时仰视读数
C.移液时有少量液体溅出 D.加水定容时仰视刻度线
II.该小组继续探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售84消毒液稀释至100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用H2SO4溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计);
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
HClO和ClO-物质的量分数(a)随溶液pH变化的关系如图所示:
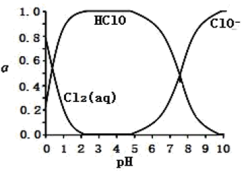
(3)①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色_______ 。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是_______ 。
I.84消毒液有效氯是指单位体积消毒液含与NaClO消毒能力相当的氯气的质量(1molNaClO消毒能力与1mol氯气相当),一般市售84消毒液有效氯为55-60g/L。

(1)某兴趣小组通过实验测得某品牌84消毒液有效氯为56.8g/L,假设有效氯都来自次氯酸钠,则该消毒液中NaClO的物质的量浓度为
(2)将该品牌消毒液准确稀释成有效氯为568mg/L的稀溶液500mL,用于餐具消毒。
①实验中需要的玻璃仪器除量筒、胶头滴管、烧杯外还要
②下列操作会导致有效氯偏低的是
A.容量瓶用蒸馏水洗涤后未干燥 B.用量筒量取84消毒液时仰视读数
C.移液时有少量液体溅出 D.加水定容时仰视刻度线
II.该小组继续探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售84消毒液稀释至100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用H2SO4溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计);
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
| 烧杯 | 溶液的pH | 现象 |
| a | 10 | 10min后,红纸基本不褪色 |
| b | 7 | 10min后,红纸颜色变浅 |
| c | 4 | 10min后,红纸基本褪色 |

(3)①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是
您最近一年使用:0次



