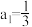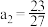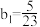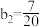将一铁、铜混合物粉末平均分成三等份,分别加入到同浓度、不同体积的稀硝酸中,充分反应后,收集到NO气体的体积及剩余固体的质量如表 (设反应前后溶液的体积不变,气体体积已换算为标准状况时的体积):
下列说法正确的是( )
| 实验序号 | 稀硝酸的体积/mL | 剩余固体的质量/g | NO的体积/L |
| 1 | 100 | 17.2 | 2.24 |
| 2 | 200 | 8.00 | 4.48 |
| 3 | 400 | 0 | V |
| A.表中V=7.84L |
| B.原混合物粉末的质量为25.6g |
| C.原混合物粉未中铁和铜的物质的量之比为2:3 |
| D.实验3所得溶液中硝酸的物质的量浓度为0.875 mol•L﹣1 |
更新时间:2018-05-09 13:46:07
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】取一定质量的Cu、Cu2O、CuO的固体混合物,将其分成两等份。其中一份通入足量的氢气充分反应后固体质量为25.6g,另一份加入到500mL稀硝酸中固体恰好完全溶解并产生标准状况下的NO气体4.48L。已知Cu2O+2H+═Cu+Cu2++H2O。则稀硝酸的浓度为
| A.2 mol/L | B.1.6 mol/L | C.0.8 mol/L | D.0.4 mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在 的
的 溶液中,加入
溶液中,加入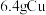 ,
, 全部溶解,假设还原产物只有
全部溶解,假设还原产物只有 和
和 ,将反应后的溶液用蒸馏水稀释至
,将反应后的溶液用蒸馏水稀释至 时,测得
时,测得 的浓度为
的浓度为 ,下列说法错误的是
,下列说法错误的是
 的
的 溶液中,加入
溶液中,加入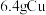 ,
, 全部溶解,假设还原产物只有
全部溶解,假设还原产物只有 和
和 ,将反应后的溶液用蒸馏水稀释至
,将反应后的溶液用蒸馏水稀释至 时,测得
时,测得 的浓度为
的浓度为 ,下列说法错误的是
,下列说法错误的是A.反应中,体现 的酸性和氧化性 的酸性和氧化性 |
B.当 时,生成 时,生成 的物质的量为 的物质的量为 |
C.反应后的溶液稀释后, 为 为 |
D.若a的值增大,则产生 和 和 的体积比增大 的体积比增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】常温时,将0.1 mol Fe(NO3)3和2 mol HCl溶于水得2L混合溶液,然后向该溶液投入mg铁粉使其充分反应后,滴加KSCN溶液不变红色。下列有关说法正确的是
| A.由于氧化性Fe3+> H+,首先发生的反应是:Fe+2Fe3+= 3Fe2+ |
| B.当加入16.8 g铁粉时,可生成标准状况下6.72 L气体 |
| C.在铁粉充分反应后的溶液中,铁元素以Fe2+和Fe3+的形式存在 |
| D.充分反应后,至少耗铁56g |
您最近一年使用:0次
单选题
|
较难
(0.4)
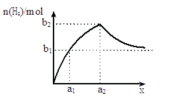
【推荐2】研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法表示更便于理解。下列表达正确的是
A.Na2CO3溶液和盐酸反应后溶液中的钠盐: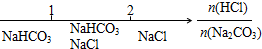 |
B.NaOH溶液与CO2反应后溶液中的钠盐: |
C.Fe与稀硝酸反应的氧化产物: |
D.AlCl3溶液中滴加氨水后铝元素的存在形式: |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两等份。向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析结果错误的是


| A.OA段产生的是NO,AB段发生的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
B.原混合酸中 物质的量为0.4mol 物质的量为0.4mol |
| C.第二份溶液中最终溶质为FeSO4 |
| D.取20mL原混合酸加水稀释至1L,溶液中c(H+)=0.1mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体,这些气体与11.2 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。则消耗铜的质量为
| A.32 g | B.48 g | C.64 g | D.96 g |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】为探究某铜的硫化物组成,取一定量硫化物在氧气中充分灼烧,将生成的气体全部通入盛有足量的H2O2和BaCl2的混合液中,得到白色沉淀 4.66 g;将灼烧后的固体(仅含铜与氧2种元素)完全溶于100 mL 1 mol/LH2SO4中,过滤,得到0.64 g 红色固体,将滤液稀释至 200 mL,测得c(Cu2+)=0.1 mol/L。已知:Cu2O+ H2SO4 =CuSO4+Cu+H2O。
下列说法正确的是
下列说法正确的是
| A.得到白色沉淀亚硫酸钡 |
| B.原铜的硫化物中n(Cu)∶n(S)=2∶3 |
| C.最后所得的溶液最多可以溶解铁1.12 g |
| D.灼烧后的固体中n(Cu2O)∶n(CuO)=1∶1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某红色固体粉末可能是Cu、Cu2O、Fe2O3中的一种或几种。为探究其组成,称取a g该固体粉末样品,用过量的稀硫酸充分反应后(已知:Cu2O+2H+=Cu2++Cu+H2O),称得固体质量为b g。则下列推断不合理的是
| A.反应后溶液中大量存在的阳离子最多有3种 |
| B.向反应后的溶液中加入一定量的NaNO3,可能使b g固体完全溶解 |
C.若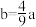 ,则红色固体粉末一定为纯净物 ,则红色固体粉末一定为纯净物 |
| D.b的取值范围:0≤b≤a |
您最近一年使用:0次

 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是 共
共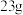 ,则铜失去的电子数大于
,则铜失去的电子数大于 、小于
、小于 (
(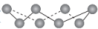 )分子中所含共价键数为
)分子中所含共价键数为
 质量分数为
质量分数为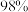 的
的 ,用水稀释至
,用水稀释至 ,
,
 钠与重水(
钠与重水( )充分反应产生
)充分反应产生