(1)硫酸被人们誉为“化学工业之母”,在国民生产中发挥着重要作用。硫酸的性质有:A.高沸点;B.强酸性;C.吸水性;D.脱水性;E.强氧化性。在下列硫酸的用途或化学反应中,硫酸可能表现上述的一个或者多个性质,试用字母填空:
①硫酸可用作气体干燥剂___________ ;
②往晶体硫酸铜中加液硫酸,晶体变白___________ ;
③浓硫酸使湿润蓝色石蕊试纸先变红后又变黑___________ ;
④浓硫酸使蔗糖变黑,且有刺激性气味的气体产生___________ ;
⑤浓硫酸与FeO反应____________ ;
⑥运用铁制槽车和铝制槽车送输浓硫酸___________ 。
(2)“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫、脱硝,效果非常好。
①完成下列对烟气脱硝过程的离子方程式
___ C1O2-+__NO+____=Cl-+____NO3-+______。
②SO2有多种处理方式,写出用过量氨水吸收尾气的离子方程式:_____________________ 。
①硫酸可用作气体干燥剂
②往晶体硫酸铜中加液硫酸,晶体变白
③浓硫酸使湿润蓝色石蕊试纸先变红后又变黑
④浓硫酸使蔗糖变黑,且有刺激性气味的气体产生
⑤浓硫酸与FeO反应
⑥运用铁制槽车和铝制槽车送输浓硫酸
(2)“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫、脱硝,效果非常好。
①完成下列对烟气脱硝过程的离子方程式
②SO2有多种处理方式,写出用过量氨水吸收尾气的离子方程式:
更新时间:2018-05-26 20:00:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】2021年7月,第32届奥运会在东京召开,我国运动健儿在奥运会上取得了非凡的成绩。
(1)东京奥运会火炬的燃料是氢气,写出氢气燃烧的化学方程式_______ 。
(2)杨倩在10米气步枪比赛中获得了奥运会首金,气步枪的子弹是铅弹,构成铅的微粒是_______ (填序号)。
A.原子 B.分子 C.离子
(3)14岁的全红婵在跳水10米台的赛事中夺冠,震撼全场。下列物质中,使用的主要材料属于合成材料的是_______ (填序号)。
A.航空级铝合金跳板 B.聚酯纤维泳衣 C.金牌
(4)苏炳添在田径男子百米半决赛中以9.83秒的成绩打破了亚洲纪录。发令枪内的药粉中含有氯酸钾和红磷,扣动扳机,发生两个化学反应:①氯酸钾受撞击迅速分解产生氧气;②红磷燃烧产生白烟。写出其中任意一个化学反应的化学方程式_______ 。
(1)东京奥运会火炬的燃料是氢气,写出氢气燃烧的化学方程式
(2)杨倩在10米气步枪比赛中获得了奥运会首金,气步枪的子弹是铅弹,构成铅的微粒是
A.原子 B.分子 C.离子
(3)14岁的全红婵在跳水10米台的赛事中夺冠,震撼全场。下列物质中,使用的主要材料属于合成材料的是
A.航空级铝合金跳板 B.聚酯纤维泳衣 C.金牌
(4)苏炳添在田径男子百米半决赛中以9.83秒的成绩打破了亚洲纪录。发令枪内的药粉中含有氯酸钾和红磷,扣动扳机,发生两个化学反应:①氯酸钾受撞击迅速分解产生氧气;②红磷燃烧产生白烟。写出其中任意一个化学反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】硫元素广泛存在于自然界中,是植物生长不可缺少的元素。图1是自然界中硫元素的存在示意图,图2是硫及其化合物的“价—类”二维图。
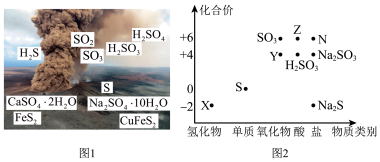
回答下列问题:
(1)图1中的 属于
属于_______ (填“纯净物”或“混合物”)。
(2)请写出图2中X和Y反应的化学方程式:_______ 。该反应中氧化产物和还原产物的质量之比为_______ 。
(3) 溶液很容易变质,请设计实验证明其已变质:
溶液很容易变质,请设计实验证明其已变质:_______ 。
(4)若N是 ,某同学设计了甲和乙两种方法制备:
,某同学设计了甲和乙两种方法制备:
甲: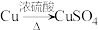
乙:
①写出甲方法反应的化学方程式:_______ 。
②甲和乙方法更合理的是_______ (填“甲”或“乙”),理由是_______ 。
(5)为测定硫酸工厂周围空气中 的含量,进行如下实验:取VL(标准状况)空气,缓慢通入碘水,充分反应后,向溶液中加入过量的
的含量,进行如下实验:取VL(标准状况)空气,缓慢通入碘水,充分反应后,向溶液中加入过量的 溶液,经过滤、洗涤、干燥,称重得白色沉淀mg。
溶液,经过滤、洗涤、干燥,称重得白色沉淀mg。
①写出 与碘水反应的离子方程式:
与碘水反应的离子方程式:_______ 。
②空气中 的体积分数是
的体积分数是_______ (用含V、m的代数式表示)。

回答下列问题:
(1)图1中的
 属于
属于(2)请写出图2中X和Y反应的化学方程式:
(3)
 溶液很容易变质,请设计实验证明其已变质:
溶液很容易变质,请设计实验证明其已变质:(4)若N是
 ,某同学设计了甲和乙两种方法制备:
,某同学设计了甲和乙两种方法制备:甲:
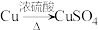
乙:

①写出甲方法反应的化学方程式:
②甲和乙方法更合理的是
(5)为测定硫酸工厂周围空气中
 的含量,进行如下实验:取VL(标准状况)空气,缓慢通入碘水,充分反应后,向溶液中加入过量的
的含量,进行如下实验:取VL(标准状况)空气,缓慢通入碘水,充分反应后,向溶液中加入过量的 溶液,经过滤、洗涤、干燥,称重得白色沉淀mg。
溶液,经过滤、洗涤、干燥,称重得白色沉淀mg。①写出
 与碘水反应的离子方程式:
与碘水反应的离子方程式:②空气中
 的体积分数是
的体积分数是
您最近半年使用:0次
【推荐3】按要求回答下列问题:
(1)①已知KMnO4与浓盐酸室温下可发生如下反应。用“双线桥法”标出反应的电子转移情况:_______
2KMnO4+16HCl(浓)=2KCl+2MnCl2+ 5Cl2↑+8H2O
②此反应中生成71 g C12时消耗的还原剂的质量为____________________ 。
(2)某反应中反应物与生成物有: AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、 H2O和一种未知物质X.。
①已知KBrO3在反应中得到电子,则该反应的还原剂是_____________________ 。
②已知0.2 mol KBrO3在反应中得到1 mol电子生成X,则X的化学式为_____________ 。
(3)NaBH4是一种重要的储氢载体, 能与水反应得到NaBO2和H2,且反应前后 B的化合价不变, 该反应的化学方程式为________ ,反应消耗1molNaBH4时转移的电子数目为_____________ ,该反应的氧化产物为_______________ 。
(1)①已知KMnO4与浓盐酸室温下可发生如下反应。用“双线桥法”标出反应的电子转移情况:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+ 5Cl2↑+8H2O
②此反应中生成71 g C12时消耗的还原剂的质量为
(2)某反应中反应物与生成物有: AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、 H2O和一种未知物质X.。
①已知KBrO3在反应中得到电子,则该反应的还原剂是
②已知0.2 mol KBrO3在反应中得到1 mol电子生成X,则X的化学式为
(3)NaBH4是一种重要的储氢载体, 能与水反应得到NaBO2和H2,且反应前后 B的化合价不变, 该反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硫酸是中学化学实验室的常见药品,其性质有①酸性 ②吸水性 ③脱水性 ④强氧化性,以下过程或反映体现了硫酸的什么性质,请将序号填在相应的横线上:
(1)锌和稀H2SO4制H2________ ;
(2)浓硫酸作干燥剂________ ;
(3)浓硫酸与碳单质的反应________ ;
(4)浓硫酸与铜的反应________ ;
(5)浓硫酸使湿润的蓝色石蕊试纸先变红后变黑________ ;
(6)常温下浓硫酸可用铁或铝制容器贮存________ 。
(1)锌和稀H2SO4制H2
(2)浓硫酸作干燥剂
(3)浓硫酸与碳单质的反应
(4)浓硫酸与铜的反应
(5)浓硫酸使湿润的蓝色石蕊试纸先变红后变黑
(6)常温下浓硫酸可用铁或铝制容器贮存
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有两支分别盛有相同体积浓硫酸和稀硫酸的试管,请用简单的方法区别它们._______
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据要求填空:
(1)硫酸有很多的性质,将下列性质对应的字母填入各小题后面对应的括号中:
A.脱水性 B.酸性 C.强氧化性 D.吸水性
①在化学实验中,浓硫酸可作SO2、CO2等气体的干燥剂__ 。
②Na2CO3与H2SO4反应,可生成Na2SO4和CO2__ 。
③向滤纸上滴加浓H2SO4,滤纸变黑__ 。
④在冷浓H2SO4中放入铁片没明显现象__ 。
(2)反应C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O中,有6g碳单质完全参与反应转移___ mol电子,还原产物是___ (填化学式)。
(1)硫酸有很多的性质,将下列性质对应的字母填入各小题后面对应的括号中:
A.脱水性 B.酸性 C.强氧化性 D.吸水性
①在化学实验中,浓硫酸可作SO2、CO2等气体的干燥剂
②Na2CO3与H2SO4反应,可生成Na2SO4和CO2
③向滤纸上滴加浓H2SO4,滤纸变黑
④在冷浓H2SO4中放入铁片没明显现象
(2)反应C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O中,有6g碳单质完全参与反应转移
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】浓硫酸具有:①难挥发性(高沸点);②酸性;③强氧化性;④吸水性;⑤脱水性。下列各项分别表现浓硫酸的什么性质,请将序号填于空白处:
(1)浓硫酸与食盐共热,浓硫酸表现的性质为__ 。
(2)浓硫酸与铜共热,化学方程式为__ ,浓硫酸表现的性质是__ 。
(3)浓硫酸与红热木炭反应,化学方程式为__ ,浓硫酸表现的性质是__ 。
(4)可用浓硫酸干燥H2、CO2、HCl等气体,浓硫酸表现的性质为__ 。
(5)蔗糖中倒入浓硫酸,蔗糖变黑,体积膨胀,且有刺激性气味的气体产生,浓硫酸表现的性质是__ 。
(1)浓硫酸与食盐共热,浓硫酸表现的性质为
(2)浓硫酸与铜共热,化学方程式为
(3)浓硫酸与红热木炭反应,化学方程式为
(4)可用浓硫酸干燥H2、CO2、HCl等气体,浓硫酸表现的性质为
(5)蔗糖中倒入浓硫酸,蔗糖变黑,体积膨胀,且有刺激性气味的气体产生,浓硫酸表现的性质是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列4种物质:①Cl2、② NH3.③浓H2SO4、④A12O3。其中,能与水反应生成两种酸的是__ (填序号,下同);与强酸、强碱溶液均可反应生成盐的是______ ;能使湿润的红色石蕊试纸变蓝的是___ ;能使蔗糖变黑并有气体生成的是_____ 。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.地壳中的硅元素在现代高科技产品中占有重要位置,足见化学对现代文明的重要作用。例如:
(1)计算机芯片的主要成分是___________ 。
(2)工业上制取粗硅的化学方程式为___________ ;光导纤维遇到强碱易被腐蚀,请写出该物质与氢氧化钠溶液反应的化学方程式___________ 。
(3)下列物质的主要成份不属于硅酸盐的是___________(填字母)。
Ⅱ.浓硫酸在常温下为黏稠状液体,且具有吸水性、脱水性和强氧化性。
(4)用蘸有浓硫酸的玻璃棒在木板上写字,字迹一会儿就变黑。浓硫酸表现出___________ 性。
(5)浓硫酸表现吸水性时,可作干燥剂,下列物质可用浓硫酸干燥的是___________ 。
A.NH3 B.H2S C.H2 D.SO2 E.O2 F.HI
(6)在加热条件下,浓硫酸能与Cu反应,表现___________ 。请写出这个化学反应的化学方程式___________ 。
(1)计算机芯片的主要成分是
(2)工业上制取粗硅的化学方程式为
(3)下列物质的主要成份不属于硅酸盐的是___________(填字母)。
| A.陶瓷 | B.玻璃 | C.水泥 | D.碳化硅陶瓷 |
Ⅱ.浓硫酸在常温下为黏稠状液体,且具有吸水性、脱水性和强氧化性。
(4)用蘸有浓硫酸的玻璃棒在木板上写字,字迹一会儿就变黑。浓硫酸表现出
(5)浓硫酸表现吸水性时,可作干燥剂,下列物质可用浓硫酸干燥的是
A.NH3 B.H2S C.H2 D.SO2 E.O2 F.HI
(6)在加热条件下,浓硫酸能与Cu反应,表现
您最近半年使用:0次
【推荐1】化学是一门实用性很强的科学,请根据题意填空:
(1)运输浓硫酸和浓硝酸常用铝罐车,试解释其原因:___________ 。
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是___________ (填化学式)。
(3)常用的打火机中充有丁烷,C4H10的一氯代物有___________ 种,分子式为C6H14的长链(无支链)有机物的名称为___________ 。
(4)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(5)葡萄糖、蔗糖、淀粉、油脂、蛋白质都属于营养物质,其中属于高分子化合物的是___________ (填名称),在加热条件下,葡萄糖与新制的氢氧化铜反应,可观察到的现象为___________ 。
(6)医院里用高温蒸煮、紫外线照射等方法进行消毒,其原因是___________ 。
(1)运输浓硫酸和浓硝酸常用铝罐车,试解释其原因:
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
(3)常用的打火机中充有丁烷,C4H10的一氯代物有
(4)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(5)葡萄糖、蔗糖、淀粉、油脂、蛋白质都属于营养物质,其中属于高分子化合物的是
(6)医院里用高温蒸煮、紫外线照射等方法进行消毒,其原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】如果用过量的锌代替铜与一定量的浓硫酸反应,生成气体的成分有哪些_____ ?
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】浓硫酸的特性
(1)吸水性
浓硫酸能吸收存在于周围环境中的水分(自由水和结晶水),常用作_______ 。
(2)脱水性
使有机物分子中的H和O以原子数2:1比例脱去,而使物质结构发生改变,生成新物质的性质
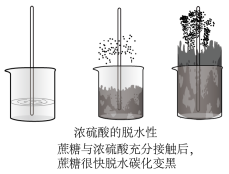
实验现象:向蔗糖中加入浓硫酸,搅拌,可观察到蔗糖_______ ,体积_______ ,变成疏松多孔的海绵状的炭,并放出有_______ 气味的气体。反应化学方程式_______ 。
(3)强氧化性
①浓硫酸与Cu反应
②浓硫酸与非金属反应
碳与浓硫酸反应_______ 。
③浓硫酸与金属反应
a.常温下,Fe、Al与浓H2SO4发生钝化,生成了致密的氧化膜。
b.氢前的活泼金属(如Zn):常温下与浓硫酸反应先产生_______ ,后产生_______ 。
c.氢后的活泼金属(如铜):加热下与浓硫酸反应先产生_______ ,后反应停止。
(1)吸水性
浓硫酸能吸收存在于周围环境中的水分(自由水和结晶水),常用作
(2)脱水性
使有机物分子中的H和O以原子数2:1比例脱去,而使物质结构发生改变,生成新物质的性质

实验现象:向蔗糖中加入浓硫酸,搅拌,可观察到蔗糖
(3)强氧化性
①浓硫酸与Cu反应
| 实验操作 | 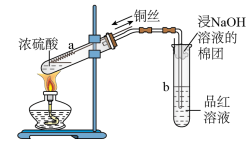 |
| 实验现象 | 铜丝表面 |
| 实验结论 | 在反应中,浓硫酸体现 |
| 化学方程式 |
碳与浓硫酸反应
③浓硫酸与金属反应
a.常温下,Fe、Al与浓H2SO4发生钝化,生成了致密的氧化膜。
b.氢前的活泼金属(如Zn):常温下与浓硫酸反应先产生
c.氢后的活泼金属(如铜):加热下与浓硫酸反应先产生
您最近半年使用:0次



